置换反应
比较SN1 SN2反应
最后更新:2023年6月9日|
比较的年代N1和年代N2反应
在亲核取代反应,碳和之间的一条纽带离去基团(C-LG)坏了,和碳之间的新债券亲核试剂(C-Nu)形成。
亲核取代反应烷基卤化物发生主要通过两种途径。关键的区别在于时机bond-forming和bond-breaking步骤。
- 的年代N1机制(年代ubstitution,Nucleophilic,大学分子速率决定步骤)通常通过两个步骤;首先,(慢,速度决定)打破C-LG债券的衬底上形成一个中间碳正离子,紧随其后的是(快速)的亲核试剂C-Nu碳正离子(形式)给替代产品(通常会有第三酸碱遵循的步骤取代反应当中性的亲核试剂H2使用O或卢武铉)
- 的年代N2机制(年代ubstitution,Nucleophilic,Bi发生在一个分子的速率决定步骤)单,共同步骤:攻击的亲核试剂背面的C-LG债券,途中经过一个短暂的五元过渡态四面体产品配置在碳已经倒了。
因为年代的速率决定步骤N1是形成碳正离子,它可以帮助把“大障碍”N第一反应是碳正离子的稳定性,任何因素导致增加稳定的碳正离子中间体将增加的速率N1。这就是为什么这个途径往往是由三级青睐烷基卤化物,因为碳正离子稳定性的顺序一般收益高等>二级>主(见文章:碳正离子的稳定性)
同样,因为年代的速率决定步骤N2的背后攻击亲核试剂在碳上,它可以帮助把“大障碍”N2的反应是位阻(见文章:位阻)。任何因素增加的困难亲核试剂可以访问的σ*轨道C-LG债券将导致较慢的反应,这有助于我们解释SN2与甲基和初级更快烷基比二、三级卤化物烷基卤化物。
由于这两个不同的机制,SN1和年代N2反应表现出差异的关键
- 观察到的速率定律(单分子的年代N1,双分子的年代N2)
- 的模式立体化学(保留+反演SN1,反演SN2)
- 相对利率反应为一级,二级,三级烷基卤化物(三级>二级>主要的年代N1,主要>二级>三级N2
此外,年代N1和年代N2反应敏感的身份溶剂和力量的参与亲核试剂。在下面更详细!

表的内容
- 但首先:猫的故事和舒服的椅子
- SN1通过逐步机制。SN2通过协同机制
- 反应坐标图SN1的SN2反应
- SN1和速率定律的SN2反应
- 一级,二级,三级烷基卤化物SN1 SN2反应
- 比较SN1和立体化学的SN2反应
- 溶剂和的亲核试剂——SN1反应
- 溶剂和的亲核试剂——SN2反应
- 回到猫
- 笔记
- (高级)引用和进一步阅读
1。但首先:猫和舒服的椅子
但首先,你听说过猫和舒服的椅子的故事吗?

猫# 1发现猫# 2在他舒服的椅子,想坐。他有两个选择。
- 他可以等待猫# 2离开,然后坐在舒服的椅子。
- 他可以踢猫# 2的舒服的椅子。
2。的年代N1通过逐步机制。的年代N2通过协同机制
让我们来比较一下机制的年代N1和年代N首先2反应,因为我们将观察其他区别是他们不同的机制的结果。(通常,提出只有机制后收集大量的实验证据(例如速率定律、立体化学、相对利率,等等),但是因为这并不是一个阿加莎·克里斯蒂的小说,我们首先给出结束)。
的年代N1通常通过一个两步”逐步”机制,
(在许多情况下,通常是一个涉及的去质子化的第三步亲核试剂给一个中立的产品,特别是在亲核试剂是中性的)
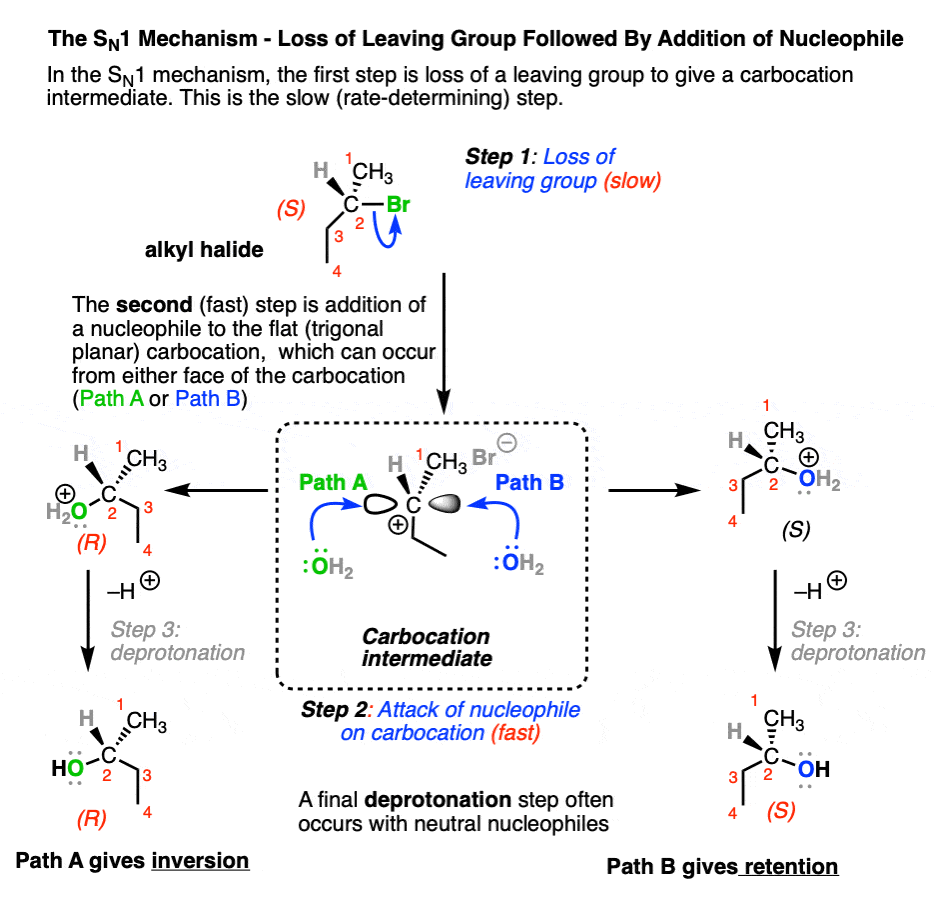
注意,在碳,碳正离子的中间有一个三角平面几何及其空的p轨道可以接受另外一个亲核试剂同样在要么的脸。在这种情况下,替换发生在一个手性碳(又名“手性碳”)这可能导致的混合物保留和反演立体化学的,相对于原来的配置烷基卤化物。(注1]
相比之下,SN2通过一步反应协调一致的相当于的机制亲核试剂增加了一个相当于衬底,导致形成的新债券亲核试剂的损失离去基团从碳。
这是通过捐赠的一对电子亲核试剂空,反键sigma星(σ*)轨道C-LG债券的背面。碳-亲核试剂债券(C-Nu)形式碳——在同一时间离去基团债券(C-LG)休息。
由于碳不能舒服地容纳超过四结合伙伴一次这两个债券被认为是部分结合角色过渡态(请注意下面的虚线,)碳采用几何三角双锥体。
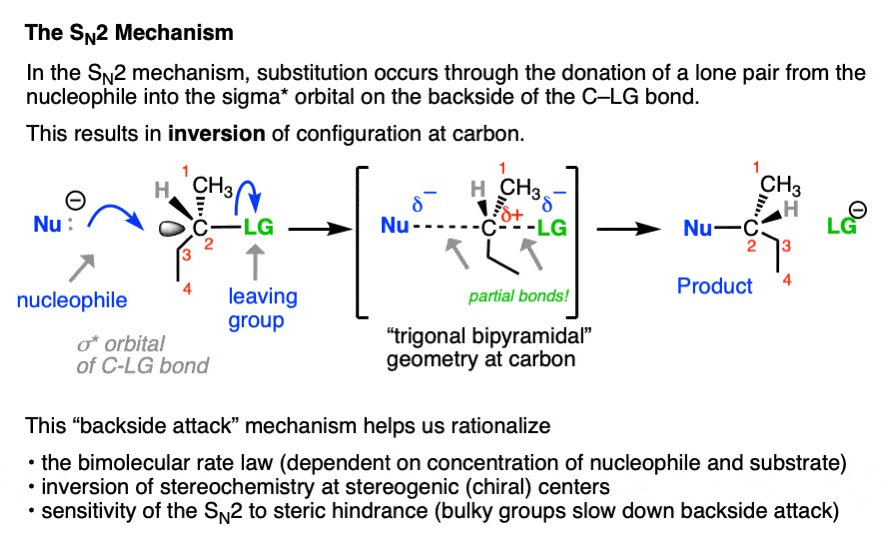
随着C-Nu债券形式和C-LG债券休息,取代基的三个“三方”的“赤道”碳四面体几何放松,他们是完全的不同倒从其原始位置(像经常引用的比喻“伞将由内而外大风”)。
3所示。反应坐标图的年代N1和年代N2反应
一种可视化之间的差异是勾勒出这两个机制反应坐标图,我们图势能的变化(垂直轴)的起始材料传递“反应坐标”向他们转换成产品(横轴)(这些图相似图形的变化高度(也势能!)经历了一个徒步旅行者导航两个目的地之间的山口。)
在这些图中“山峰”(最大值)表示过渡状态而“山谷”(局部最小值)表示中间体。(过渡态是一种瞬态物种部分债券。中间是一个潜在的可孤立的物种)。
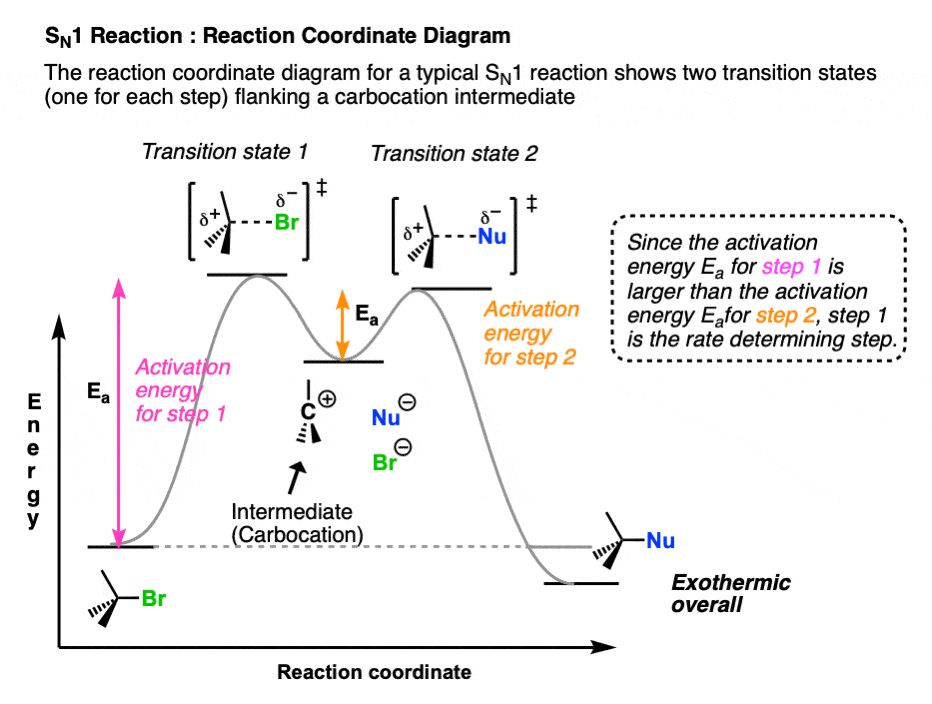
的反应坐标图N1反应有两座山峰,代表两个过渡状态(分别为步骤1和步骤2)在一个侧面“谷”代表碳正离子中间体。
每一步的过程活化能所代表的不同能量和反应物之间的过渡状态。
的速率决定步骤的反应是要求最高的一步活化能最大的变化,就是势能从反应物到过渡态。在这个年代N1反应速率决定步骤是(示粉红色)的损失离去基团从烷基卤化碳正离子。
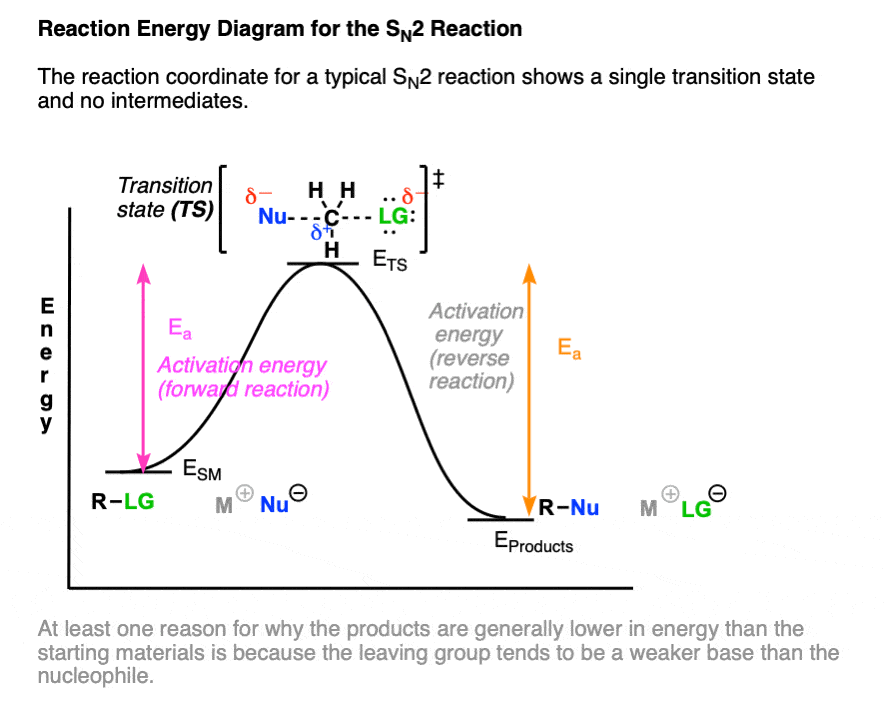
的反应坐标图N2反应显示了只有一个过渡态(一个“峰”)对应协调一致的C-LG C-Nu和破损的形成没有任何中间。(请注意2)
一个音符——之间的能量差异起始物料和产品反映了这一事实离去基团通常是一个较弱的基础比吗亲核试剂债券的优势,以及不同碳。(见文章:是什么让一个好的离去基团)
4所示。速率定律的年代N1和年代N2反应
探索一个给定的机制的一种方式取代反应是衡量的变化反应速率当两者的浓度亲核试剂和底物是多种多样的。
因为年代的速率决定步骤N1反应是失去离去基团从衬底单分子的反应产物的生成速率的年代N1应该只取决于基质的浓度。
率=k(浓度烷基卤)
两倍、三倍、四倍的浓度底物应该因此导致增加一倍,两倍,或翻两番的目标产物的生成速率,分别。
两倍、三倍、四倍的浓度亲核试剂另一方面应该没有以来对反应速率的影响亲核试剂不参与速率决定步骤。
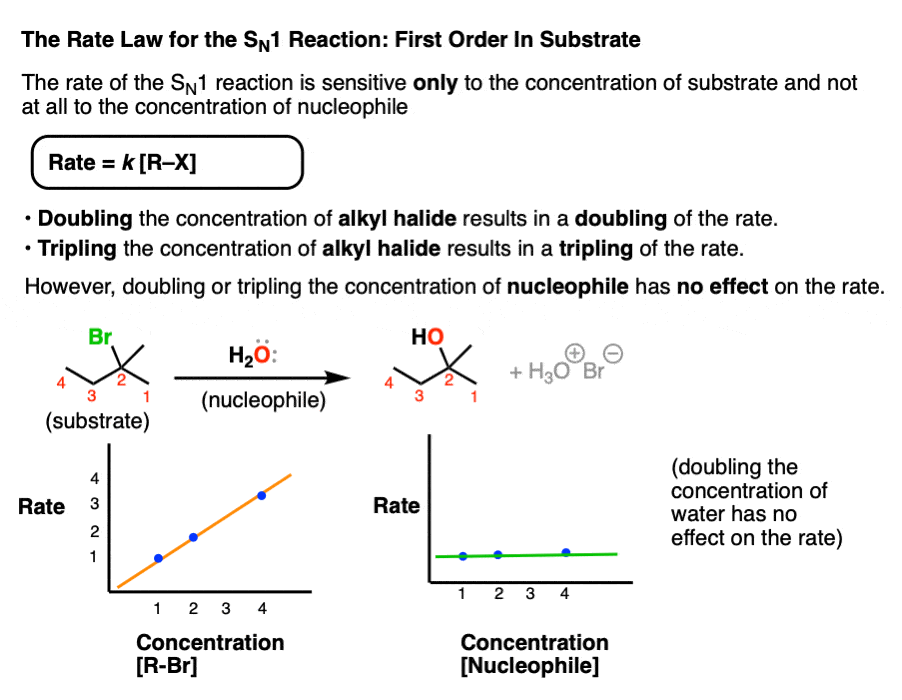
的年代N2的反应,相比之下,有一个双分子的相当于的速率决定步骤亲核试剂结合一个相当于衬底。
的整体速率定律N2是如此依赖于底物的浓度和浓度亲核试剂的形式:
我们说这是“一级”亲核试剂和“一阶”在衬底,或“二级”的整体。
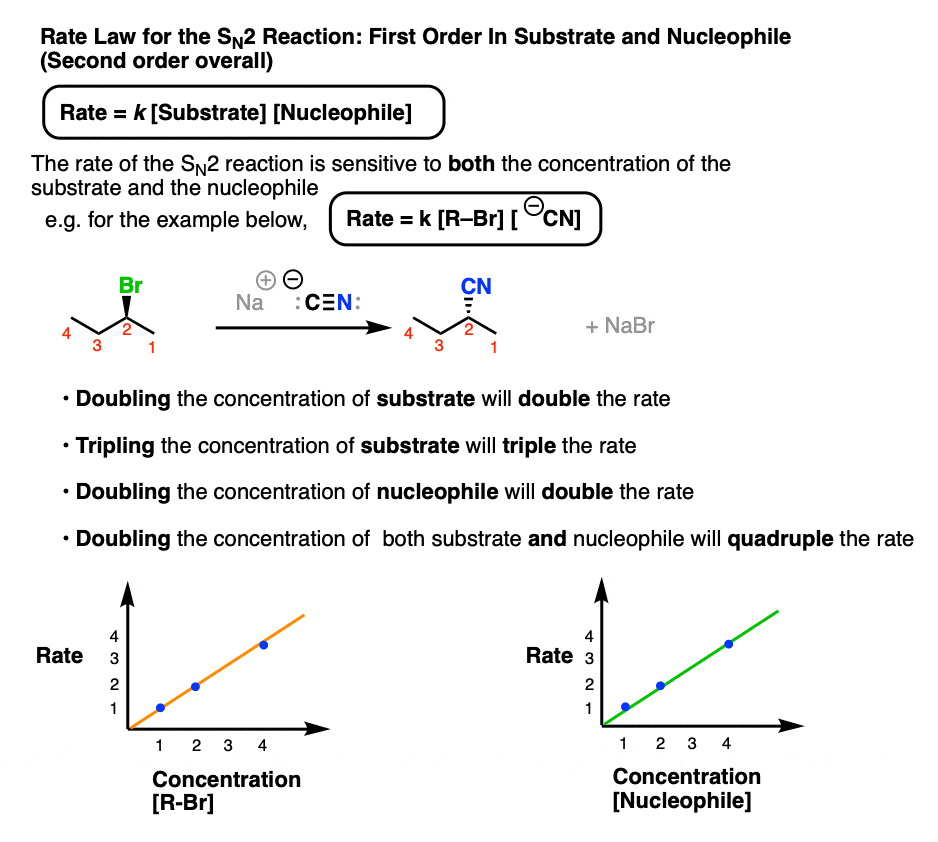
5。年代的基质对速率的影响N1和年代N2反应
年代的速率的依赖N1碳正离子的稳定性的速率N2位阻意味着他们的反应速率与主要的趋势,二级和三级烷基卤化物在相反的方向。
的速率决定步骤N1反应是形成碳正离子。自比二级三级碳正离子更稳定的碳正离子比初级反过来更加稳定和甲基碳正离子,我们应该观察到的速度N1反应最快三级烷基卤化物。
的确是这样,当不同烷基卤化物受到典型的年代雷竞技下载最新版N1条件(亲核差,极性质子溶剂如H2O) (裁判]
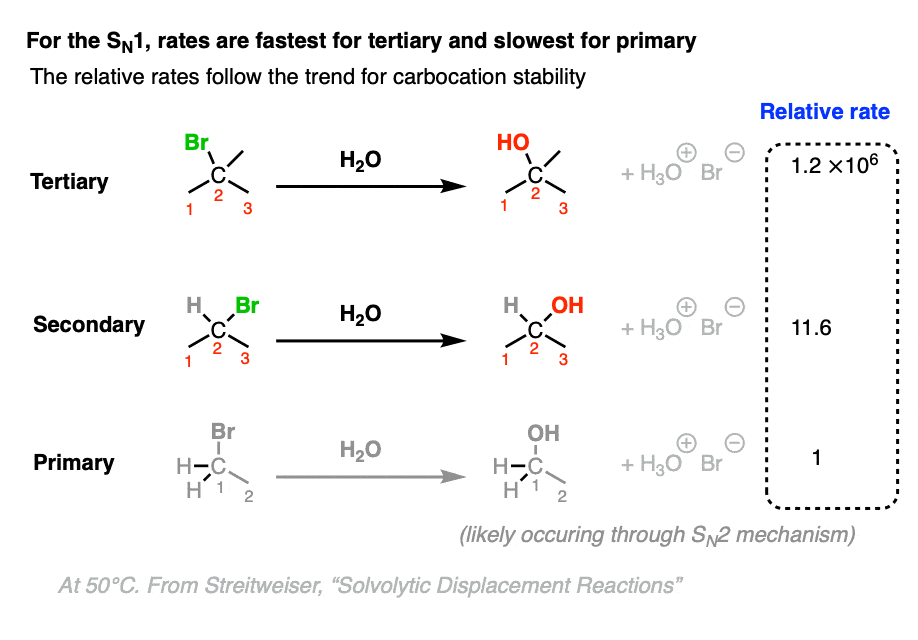
(注意,这些是相对的利率,叔丁基溴化的替换率1.2×106测量相对于溴乙烷的替换率(1))
的速率决定步骤N2是背后攻击的反应亲核试剂在一个烷基卤化物。由于氢原子小于碳原子,我们应该希望的年代N2甲基和主要反应最快烷基卤化物和三级最慢烷基卤化物。
这也同意实验中,当各种如下所示烷基卤化物与强烈的治疗亲核试剂NaCN。
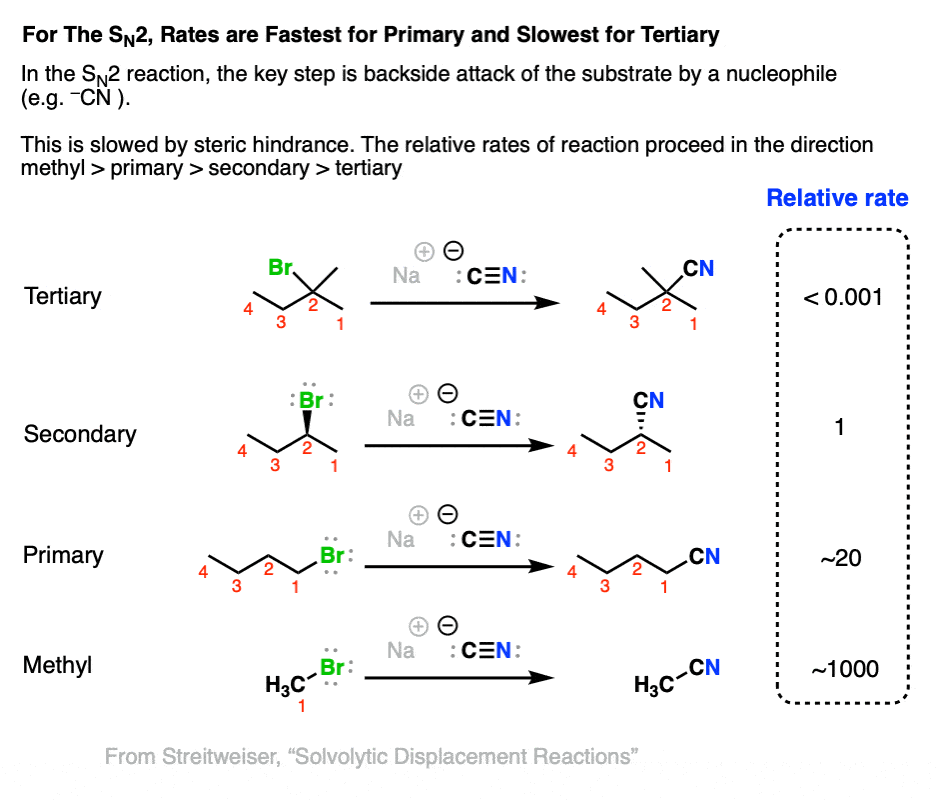
6。立体化学的比较N1和年代N2反应
的立体化学相对于这些产品的原料也是一个有用的探针的年代N1与SN2通路。
当失去一个手性中心离去基团成为一个三角平面碳正离子,失去手性。
由于生成的碳正离子可以攻击或者脸上的亲核试剂,由此产生的产品将保留和立体化学反转的混合物。
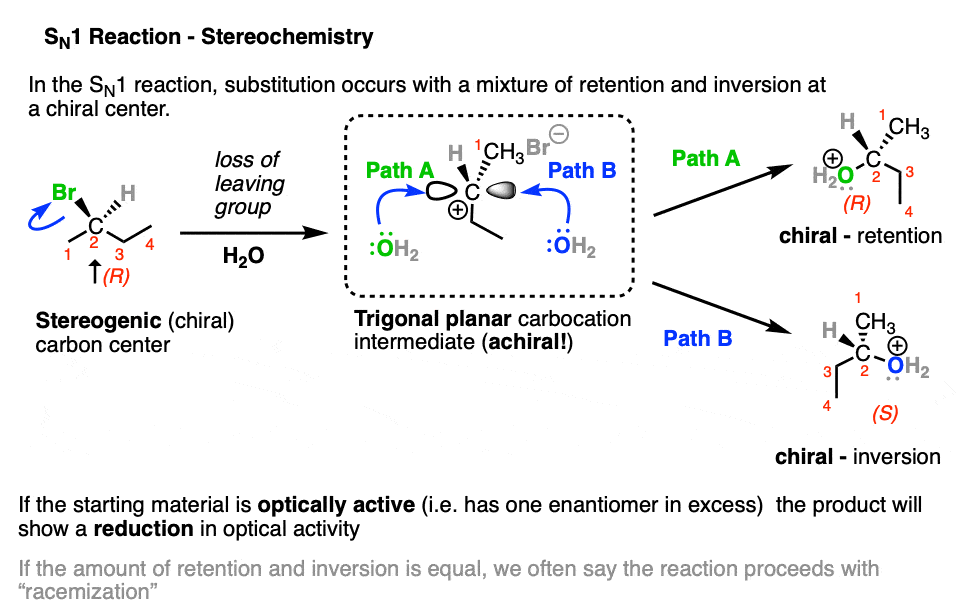
一个年代N2反应发生在一个手性碳会导致反演的配置,但是保留光学纯度。
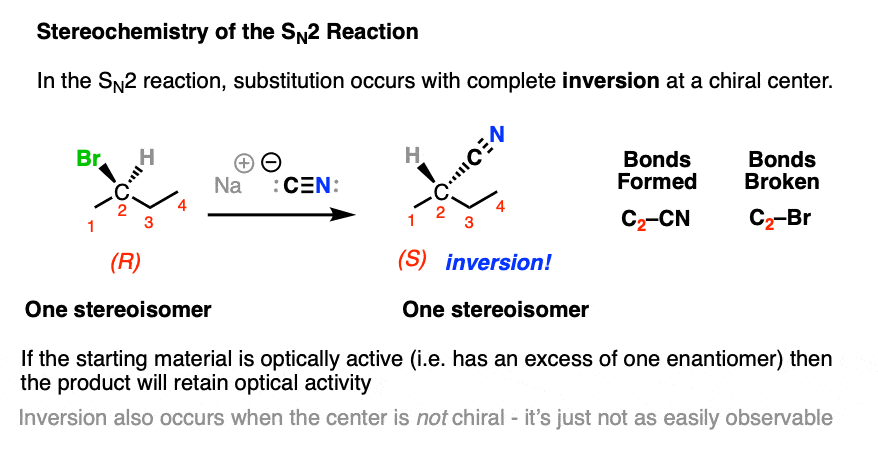
注意,反演仍发生起始物料是否是否手性;它不会是可观测的。
7所示。溶剂和的亲核试剂N1
的SN1反应时往往会发生烷基卤化物能形成合理稳定的碳正离子是溶解在极性质子溶剂,能够作为亲核试剂。
失去一个离去基团给一个碳正离子导致瞬态的形成离子对(即碳正离子和离去基团)从一个中立的物种(即烷基卤)
就像像氯化钠盐不溶于非极性溶剂如己烷(介电常数,ε= 2),形成碳正离子是更有利的极地溶剂与水(ε= 78)、醇类(ε~ 20 - 40)或羧酸(如甲酸、ε= 51),它可以稳定通过氢键或其他指控偶极相互作用。
碳正离子与中性硼的化合物(例如高炉3),他们是优秀的路易斯酸含有6个价电子和一个空的p轨道。一旦形成,碳正离子容易接受而且即使贫穷刘易斯基地给产品一个完整的八隅体周围的碳。
所以在实践中,这通常意味着溶剂是亲核试剂,因为它存在于更高的浓度相对于其他。(注3]

8。溶剂和的亲核试剂N2
年代N2反应可以进行在醇等极性质子溶剂,特别是在小学烷基卤化物。
但由于年代的速度N2不依赖碳正离子形成更广泛的(极)可以使用溶剂。
此外,烷基卤化物更穷比碳正离子的亲电试剂。这实际上是一件好事,因为它们是不太可能接受副反应如重排或消除,或与第一个反应路易斯碱他们看到。
出于实用目的,SN2的反应往往是进行(即带电)较强的亲核试剂。可以使用多种亲核合作伙伴,使SN2非常多才多艺,尤其是初级烷基卤化物。(见文章-为什么这个年代N2反应是强大的)
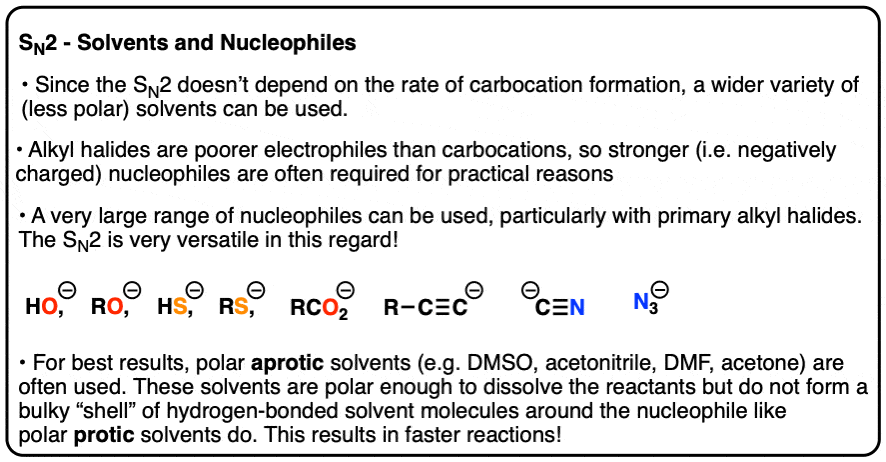
极地质子溶剂等DMSO溶液,丙酮,DMF和乙腈通常选择SN2的反应,因为他们足够极地溶解反应的伙伴,但不能形成氢键亲核试剂。这有实际效果的亲核试剂体积更小,因为亲核试剂不是到处都被溶剂分子的壳。
别忘了——你可以下载一个免费的准时上交汇总表的年代N1对SN2反应包含所有材料在这个博客:下载PDF SN1 vs SN2汇总表
笔记
猫说明我的才华横溢的表弟,政治漫画家格雷姆·麦凯
注1。(亲密离子对可以影响这个)。
注2。(如果亲核试剂是中性的,例如水,然后会有一个第二,低能的过渡态对应的去质子化的步骤)
注3。(是可能的陷阱与外部碳正离子的亲核试剂。)
更新。有史以来最完美的猫的视频。由于亚历克斯罗氏(罗格斯美国)发送。
测试自己
(测试)
(高级)引用和进一步阅读
溶剂离解作用位移反应由安德鲁·Streitweiser编译是一个陈旧的东西,但一个感伤的很多信息(特别是反应速率)的年代N1和年代N2反应。上可用的互联网档案馆小时贷款在这里。
- 反应动力学和瓦尔登湖反演。部分VI。空间方向关系在替换机制包括卤素原子和简单或取代羟基
w·a·Cowdrey e·d·休斯,c·k·英格尔德美国丈夫,公元斯科特
j .化学。Soc。1937年,1252 - 1271
DOI:10.1039 / JR9370001252
摘要中列出的点是了解影响年代值得一读N1和年代N2通道。 - 饱和碳原子的替代机制。第二十六章部分。位阻的作用。(部分)引言和甲基的反应动力学研究,乙,丙,异丁基,新戊基溴化物与乙醇钠乙干燥酒精
即Dostrovsky和e·d·休斯
j .化学。Soc。1946年,157 - 161
DOI:10.1039 / JR9460000157
表我在本文中展示了还原反应速率的年代N2反应与诗人R-Br——当R从甲基乙基- > - >n丙基- >异丁基- >t戊。这可以归因于位阻,作为替代碳的背后攻击变得越来越具有挑战性。 - 饱和碳原子的替代机制。第三部分。动力学退化的锍化合物
约翰·l·Gleave爱德华·d·休斯和克里斯托弗·k·英格尔德
j .化学。Soc。1935年,234 - 244
DOI:10.1039 / JR9350000236
这是一个有用的纸——开始条款”年代N1”和“SN2”介绍和定义,无花果。1和2描述两种机制如何竞争取决于基质的结构。 - 波兰人和极性连接对课程的影响所追求的消除反应。十六。第四纪的热分解机理铵化合物
e·d·休斯,c·k·英格尔德和c·s·帕特尔
j .化学。Soc。1933年,526 - 530
DOI:10.1039 / JR9330000526
在本文的最后,作者强调一个重要问题:“时,可以更充分地填充各种系列,被描述为一个“点”的机械的改变可能会表现为一个区域,因此,与反应(a)一样,我们现在推广的原始概念沉思反应(B)的一系列机制,(提单)——(B2),其中两个极端实验例证”。基本上,年代N1和年代N2机制作为教是统一体的两个极端,和在实践中大多数反应介于两者之间。 - 饱和碳原子的替代机制。第九部分。的一阶水解溶剂的作用烷基卤化物
莱斯利·c·贝特曼和爱德华·d·休斯
j .化学。Soc。1937年,1187 - 1192
DOI:10.1039 / JR9370001187 - 分子内重排的共同基础。VI.1新戊二碘化反应
弗兰克·c·惠特莫尔·e·l . Wittle和a . h . Popkin
美国化学学会杂志》上1939年,61年(6),1586 - 1590
DOI:1021 / ja01875a073
一纸证明年代N1反应可以通过反应的诱导烷基卤化银盐。在这种情况下,新戊基阳离子迅速将更稳定t戊基阳离子,这些产品。 - 反应动力学和瓦尔登湖反演。第一部分均匀水解和醇解β-n-octyl卤化物
爱德华·d·休斯,克里斯托弗·k·英格尔德和Standish家长
j .化学。Soc。1937年,1196 - 1201
DOI:10.1039 / JR9370001196 - 反应动力学和瓦尔登湖反演。第四部分。行动hydroxylic银盐的溶剂β-n-octyl溴和氯α-phenylethyl
爱德华·d·休斯,克里斯托弗·k·英格尔德和Standish家长
j .化学。Soc。1937年,1236 - 1243
DOI:10.1039 / JR9370001236
这两个文件检查仲辛卤化物的反应为了看纯粹的年代N1或年代N2通道在同一衬底可以支持仅仅通过改变反应条件。
啊,我很高兴它不是“流浪汉在板凳上”比喻了,感谢周到足以改变它的猫
我喜欢他们如何使用它们的尾巴平衡在视频!
你好,谢谢你的帖子。但这是问题。为什么更喜欢使用质子溶剂SN1反之亦然?
在SN1反应速率限制步骤是损失的离去基团碳正离子。极性质子溶剂介电常数较高,可以稳定生成的碳正离子物种电离的结果。其次,极性质子溶剂通常在这些反应的亲核试剂,可以中和通过去质子化。
的SN2反应速率限制步骤是亲核试剂的进攻烷基卤化物。使用一个极性非质子溶剂的结果在一个更自由的亲核试剂(免费从氢键)导致反应速率高于如果极性质子溶剂。
我应该做些什么当强和弱亲核试剂在反应中存在? ? ?我应该继续通过SN1或SN2 ? ? ?
如果主要基质,它将SN2,因为反应速度将会更快和更强的亲核试剂。
很好地解释了印象深刻…
* *现在,获得有机化学* *的信心
谢谢你!
plzz赚更多的博客上有机化学再次感谢…
酷,谢谢你让我知道圣彼得堡。什么网站可以更好呢?
为什么SN1反应活性成正比碳化的稳定性?以及如何?
请回应我。
精彩的描述。我是一个化学老师;我教我的学生这个话题/你的文章。我喜欢你的理解方式。感谢你分享你的这两个反应的信息。
你的博客是如此有用,请继续做你正在做的事情!也喜欢这个主题的汇总表,超级有用。雷竞技下载最新版
很高兴你发现它有用的肯塔基州!
哇。this is very useful site for everyone but please add reactions with mechanisms..
很高兴你找到网站有用Shailenda !
它是可能的反式复合反应的SN2反应?(如。trans -1-iodo-4-ethylcyclohexane and methoxide ion)
或者只是tehe cis的反应,因为它可能“碳连着离去基团受到亲核试剂的背面”?我们怎么知道如果它可能的混合2配置?
这是完全可能的。环己烷,重要的是要注意的是,离去基团一定轴向为了SN2发生。
你的网站是天赐之物。谢谢你!
谢谢布雷克!
这是非常令人印象深刻。我有一个Msc。应用有机化学。和我的学生帮我解释这个。猫是好的例子。谢谢你!
哈!谢谢Shiral !
只是想说,我已经买了所有你的备忘单,这是一个很大的帮助! !谢谢你清楚的解释:)
非常感谢您支持网站Cacia !
好解释。特别的猫的故事与反应的关系很好。谢谢你!
非常感谢你的观点关于Sn1和Sn2反应…………这将帮助我很多……
感谢你伟大的修订Sn1的Sn2反应。!
非常有用,尤其是卡通插图。谢谢你!
谢谢我的表弟格雷姆,哈!
我知道主要基质支持SN2和E2反应——但我的书谈到如何主要碳正离子可以形成SN1反应如果是伴随着同时rearrangment。这本书特别表示,它可能发生由于一个甲基的转变。我的问题是:它还能通过同时氢化物发生转变?或者只有通过甲基转移?我的老师给了我们一些问题通过工作,要求主要通过氢化碳正离子形成转变,我只是想确保是可行的。
是的,它可以通过同时氢化物发生转变。
SN1机制——反应的速率取决于减号。它是独立于亲核试剂。所以它可以展示是秩序机制(单分子)。它是机械超过一步。
最稳定的碳水化合物阳离子将支持sn1机甲。
极性质子溶剂将支持
溶剂分解能支持
更多的空间阻碍可以显示sn1机甲。
极性非质子溶剂的效果怎么样rxn率?这是一个有效的问题,不幸的是没有解决。
我想看看直接数据。目前我还没能找到任何将提供一个直接的比较。如果我做的话,我会把它放在。
的链接练习坏了:(
我已经拍了下来。ASU已经改变了他们的网站。
攻读我的DAT,这给了我需要的一切,我没有!谢谢你!
很高兴听到它,方面的!
谢谢你这是我能找到的最好的帮助在这个问题上,我在理解替换rxns ! !雷竞技下载最新版
为什么叔烷基卤化物喜欢亲核的反应更容易通过sn1机制?
碳正离子的稳定性是简短的答案。
就我个人而言,我认为立体效果也应该被考虑。
即使有帮助,我有困难与动力学可以用来区分SN1 SN2。
双底物的浓度、双亲核试剂的浓度。如果整个反应是一级反应,反应速率只会翻倍。如果二阶整体反应速率,反应速率将会翻两番。
伟大的解释. .简单、准确和容易理解。多谢:)
在SN1 recemized产品的原因是什么反应?精确的问题. .没有。正面和背面的攻击是一样的。为什么它不是不同?
伟大的类比和总结!谢谢你这么多!我肯定要阅读更多的你的工作!
但是我有点困惑趋势nucleophilisity卤素的极性非质子溶剂。
谢谢你!
谢谢桃子!
感谢这个伟大的解释!如果你不知道是否反应是Sn1或Sn2,什么物理性质可以用来区分它们吗?
如果是手性仲烷基卤化物,那么你可以使用旋光性来区分它们。
你是伟大的! !非常感谢你
哪一个允许更好地控制产品的配置SN1还是SN2 ?
当然,SN2因为它是立体定向。
这里是什么意思反演的配置。相对或绝对吗
相对的。
很不合时宜使用无家可归的人在这个比喻中,想象一下,如果你改变了类比在板凳上一个黑人和一个白人想要坐下来(进攻)。你有一个卡通的两只猫想坐在一篮子,为什么不直接用这个比喻;如何就两个人,一个坐在板凳上,另一个想要坐在板凳上,没有隐含的社会经济问题。除了形式非常有用的信息。
这个比喻很给力…那么聪明和容易记住!谢谢你…我利用我的牛津面试!
我非常喜欢这篇文章,但我提请贵方注意段落
“底物的依赖率”
鉴于Sn1反应最大的障碍是碳正离子的稳定性,也就是说
碳上的取代基碳正离子的稳定性增加而增加
(三级>二级> >主……而不是说共振是一个因素,
我想让这个清晰的说,第三组是EWG组
,因为他们是电子撤回他们更好的碳正离子
亲电试剂。这反过来使阳离子强大到足以与疲软的反应
亲核试剂。
请注意…。the above is not a correction ..just for clarity
嘿在SN1为什么三级反应虽然相对稳定
叔碳的稳定性使其成为一个更强的碳正离子主要碳相比,这是非常不稳定的,因为它形成的碳正离子会不稳定。如果不稳定的碳正离子然后可以反过来与离去基团反应,反应过程。所以SN1反应的反应性增加碳增加周围的组织
你好,我有一个问题关于位阻的Sn2反应。与环烷特别。我认为越高环烷碳的数量(角落越多),更有可能的是,从里面nucleofile攻击它。我的化学书中另一方面有表相对的反应。和它将环戊烷(反应)在环己烷。为什么不遵循这个规则吗?提前感谢!爱你的网站!
你好,不知道你到底是什么意思“内部”。在环戊烷、环己烷、环不够大的亲核试剂,以适应“内部”的戒指。
很难说re:环戊烷和环己烷。我无法想象有很大的区别。环己烷的障碍需要轴向的离去基团。
和角应变会有事情要做吗?增加角应变环戊烷可能导致更高的能源的原料,因此,较低的障碍交叉进行的SN2反应吗?
非常感谢。我喜欢有机化学但有时很难。我的教授会谈那样的太快所以我错过重要的细节。喜欢这段文字…
这绝对是很棒的资源!现在我明白了,没有我的讲师看起来那样复杂!
非常感谢!
很高兴你发现它有用的米甲!
很棒的解释一些简单而有效的知识思想! ! ! ! ! !……
流浪汉的故事怎么了啊?
是一个学生在有机化学肯雅塔University-Kenya,这样有助于我吗
非常感谢。
我需要和不同btween SN1 SN2示例
我需要例子SN1和SN2来区分它们
谢谢你的解释。我有一个问题关于Sn1反应的速率,将主要碳正离子,如何进行烷基转移成为三级融入,我知道一个主要碳正离子是低于二级,但这种转变会稳定。还是移花足够的时间,它不是最终的速度比二级?
如果谈论的速度形成碳正离子,自由的形成主要碳正离子是低于二级。然而,这是非常罕见的,主要碳正离子形式——主要碳烷基转移发生时,它通常是一个协调一致的重排机理并不严格经过自由碳正离子。很难严格比较利率,因为他们通过不同的机制发生。
感谢你的解释。你帮我解释几个难点了。
谢谢你的写。真正有帮助的。
所有的这些在我们测试出来。这是非常准确和解释(;
很高兴你是充分的准备!
从Clayden我学习有机化学,但是我真的很喜欢这个网站有一些额外的背景,助记符又好的总结。
我想检查练习这堂课结束时指出的那样,但给了一个错误的联系(404 -文件或目录未找到)。
噢,谢谢你!
这是如此有用的! !我爱你多么简单分解它。非常感谢! ! !
在普通化学,有一章关于动力学。如果你们感到困惑关于速率决定步骤,我将鼓励阅读这一章或彻底审查。我将尝试解释这一点。
1)SN1,
自从速率决定步骤取决于碳正离子,所以我们看一阶kinectic,可以发现的。
k =(亲电试剂),k是反应速率,作为亲电试剂的原丝下降,反应达到走向结束,或停止或减少,无论你认为是合适的亲电试剂的浓度。
2)SN2,你需要好的Nuceophile亲电试剂,因此中间阶段是5配体,并四,sp3 sp3,但是记住它有5配体,中间,这是垂直地震剖面理论,5配体,是三角双锥体。
K =[亲电试剂][nucelphile]
k是反应速度,取决于亲电试剂和时,这是二阶,1步,快速反应。
这样既增加反应率会上升,如果一个下降,它有点像试剂有限,第一排等,如果一个耗尽,并不重要,你有多少,反应不能进行。
所以我想说,这个总结结论,相关,普通化学,有机化学,它将更有意义,你将永远不会忘记:)
先生谢谢你,我正在寻找这篇文章。你会解释说它很好。甚至我的老师不能。
先生请您解释我为什么alpha-halocarbonyl化合物与Sn1没什么反应机制?
形成不稳定的碳正离子邻电子撤回C = O组,这一个非常不稳定的碳正离子。
谢谢你,先生,这是非常有用的。
哇,这么好的网站,能够很好地解释如此的感谢。更好的我的讲座:)
这是如此残暴地帮助。我肯定会使用这个网站的我今年orgo工作。
谢谢你,很高兴听到它。
问题10你提到烯丙基卤化反应和rxn SN2。烯丙基的系统因为共振反应更大,必须要有形式电荷SN1不是SN2中间。所以为什么没有任何指控中间左溴青睐。
非常感谢,这是一个伟大的主题!
嘿,只是一个问题。我知道基本的分支/亲核试剂将直接反应对E2或Sn2立体皇权的基地/ν:最有可能导致E2 rxn, b / c H +质子更加容易理解。
分支的基础/亲核试剂有影响在E1或Sn1吗?
我知道衬底有助于稳定的碳正离子的分支…
自从SN1和E1速率决定步骤反应是形成碳正离子,事件的独立的亲核试剂,分支基地/亲核试剂对这些反应没有显著影响。
实际上的分支基地/亲核试剂可以产生影响。让考虑碳正离子在过渡状态。它带正电,因此在一个理想世界中,将想要稳定,从而减少它的能量。如果有大型基地这个几乎可以保护过渡态,提供与稳定的阳离子混合效果好,坏时的空间位阻。
SN2,因为位阻减少我们从小学,中学到三级,反应的速率主要收益(最快)>二级> >三级(慢)。
*本不应该“位阻增加从*
固定的。谢谢你指出了其中的不足。
实际上立体hinderence增加我们从主要到次要的。希望这将帮助…。
我的一些学生向我挑战即将到来的类在俳句。自从fractonal蒸馏实验室很沉闷的监督每个人都启动并运行后,我把介绍SN1俳句格式。(每完成一个powerpoint幻灯片和一个漂亮的背景…)
离去基团脱落
形成碳正离子
SN1,第一步
非常被动
中间物种
他们需要电子
叔好
超共轭帮助
共振也
添加更多的ν吗?没有帮助。
率是独立的
动能的证明
爬两座山
反应坐标
C +是高通
你怎么决定?
SN1或SN2
有很多因素。
很好地完成了!
晶莹剔透。美丽的类比。来了詹姆斯,吓唬这个可怜的流浪汉所以他能容纳自己在板凳上。詹姆斯必须大,令人生畏。
我不能居功类比——我听过二手。但它是有效的,不是吗?
和谢谢你的理解。我和学生v已经覆盖这个但是我用这个来刷新一遍。
我有点困惑的类比。根据卢卡斯测试的目的(决定如果衬底小学、中学或大专)三级rxns接受sn1机制比二级rxns接受sn1 rxns然而速度比主基板进行sn2机制。在我看来像流浪汉踢替补(sn2)将比等待他离开快得多(sn1)。了翻天覆地的实际速度机制。你能详细说明类比。b / c我会rl喜欢用类似的东西去医学院成就测试通过。谢谢