碳水化合物
反应的糖:糖基化和保护
最后更新:2022年9月19日|
最后,一些反应的糖:糖基化和保护
在这篇文章里,我们介绍一些简单的糖反应,尤其是糖基化和保护:
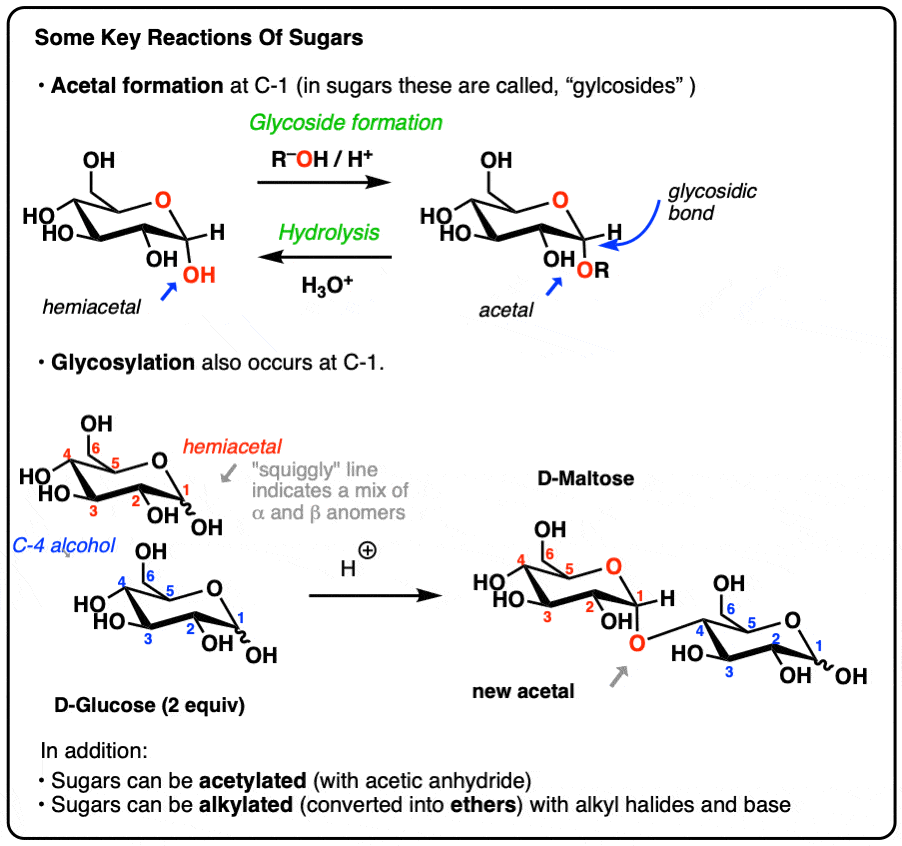
表的内容
- 碳水化合物和糖:最后,一些反应!
- 在半缩醛反应(异头碳):“苷”的形成和水解
- 苷酸溶液的水解
- 形成的二糖(理论上讲,如果不是在实践中)
- 水解糖苷键的二糖
- 酒精组糖的反应:选择性的问题
- 蛮力方法选择性:过量的试剂
- 醚在颈- 1(异头碳)可以选择性地分开
- 在选择性问题怎么走吗?一窥Org 3
- 笔记
- (高级)引用和进一步阅读
1。碳水化合物和糖:最后,一些反应!
如果反应是有机化学课程的肉,然后命名是包子,你会不假思索地认为这一章的内容对糖,呃,“carb-heavy”到目前为止。
很多术语和反应不是很多!

我们将尝试修复这个缺陷在我们今天的化学饮食的讨论糖的关键反应。
糖的反应我们将讨论归结为两大类。
第1部分:异头的反应(半缩醛)碳
的异头碳糖可以形成和破裂缩醛树脂。仅此而已。
第2部分:碳水化合物羟基的反应组(醇)
糖的羟基组可以执行所有醇的反应(如。醚形成)。关键是要有正确的反应!d
我们最后有几句话对碳水化合物的反应真的让我们的极限我们研究“Org 2”和“组织3”指明了方向。
2。半缩醛反应(“异头”):碳苷的形成
前几章,我们看到了如何醛和酮转化为缩醛,经半缩醛。前进的方向,这是通过治疗来实现的酮(或醛过度的酒精在酸的存在(如H2所以4)。
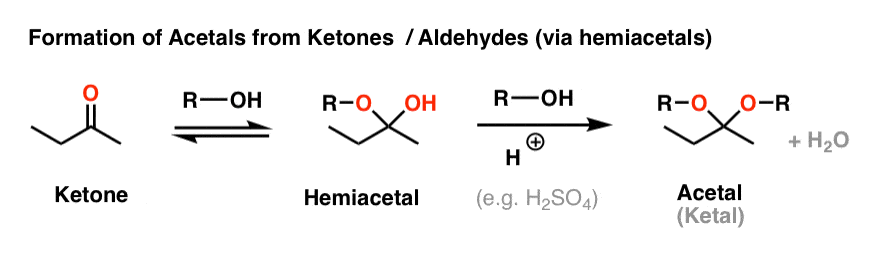
单糖(如葡萄糖)半缩醛官能团是因为5 - 6元环之间容易形成羰基碳和羟基,这一现象被称为“ring-chain互变现象”。
所以,半缩醛官能团在糖也可以转化为一个完整的缩醛用一种酒精在酸的存在。
在碳水化合物化学,这些缩醛树脂有一个特别的名字:“配糖体”。
这是一个例子。治疗与乙醇和葡萄糖酸提供一个称为乙-D-glucopyranoside的产品。
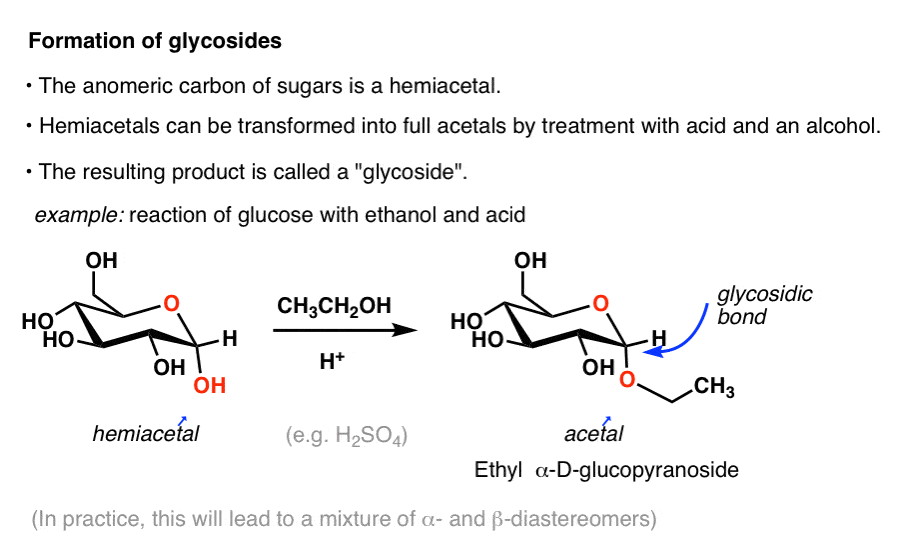
新切断债券被称为“糖苷键”。在上面的图中,我们只有一个异头物(α),但实际上都将形成。
形成的糖苷“锁”环关闭,它不再是平衡与开链形式,因此不再“还原糖”(参见:还原糖]。像所有的缩醛树脂,唯一的反应的重要性,它将接受水解回到起始物料与水酸。
3所示。苷酸溶液的水解
结果治疗与水和酸糖苷在最初的糖(异头物的混合物,我们可以描述“等号”)。
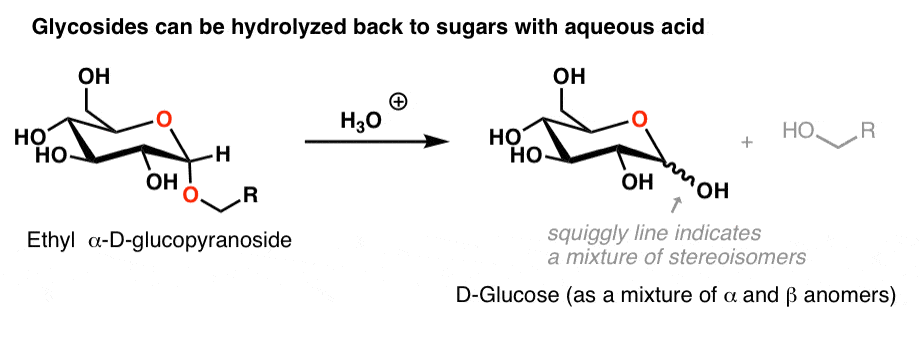
4所示。形成的二糖(理论上讲,如果不是在实践中)
一种特别重要的糖苷是由两个或两个以上的糖的结合。麦芽糖例如,缩醛颈- 1 C的葡萄糖反应时形成的4-哦,另一个葡萄糖分子形成α-糖苷键。
描述这个链接的快捷方式(α-1→4),在1和4的数字表明碳侧翼糖苷键,和“α”表明异头碳的立体化学。(α和β的快速回顾一下]
在理论上,可以进行这个反应治疗d -葡萄糖酸:
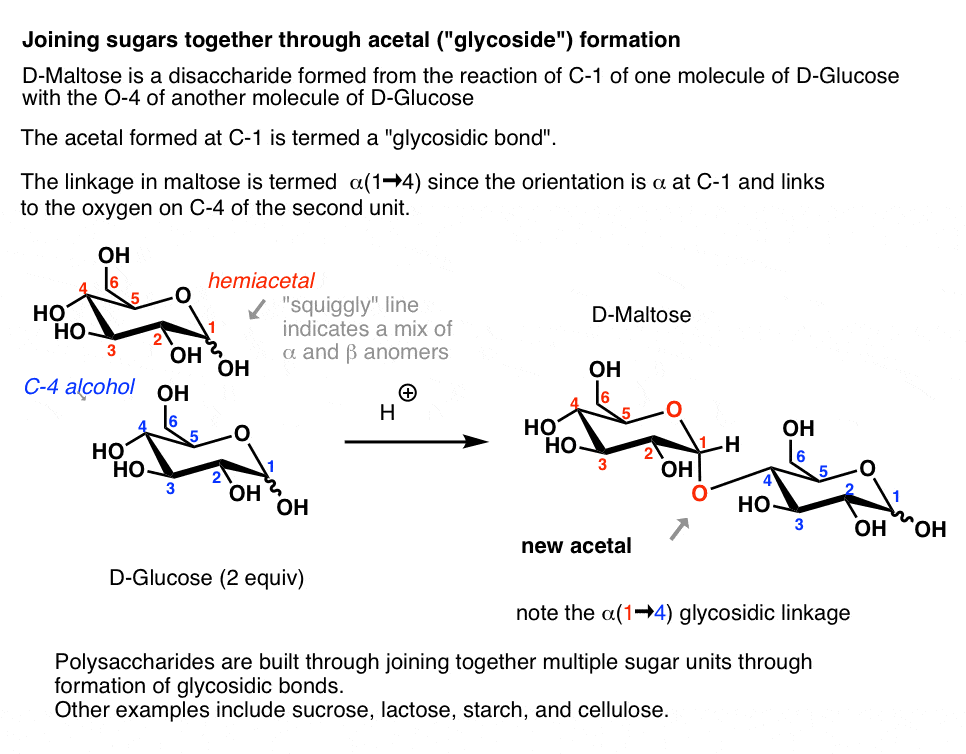
(看到的机制徘徊在一个弹出的形象或点击链接的形象。
在实践中?好了,上面的画是有点误导。
在实验室里,添加葡萄糖酸可能让你一些麦芽糖,但它也将提供大量的其他对象从其他羟基组的反应(C1-OH, C2-OH等)颈- 1碳。(这是一种反应我的朋友杰夫会写在他的实验室笔记本“BFM”,“M”代表“烂摊子”)。
在自然界中,特定的酶结合糖一起进化精致site-selectivity(“区域选择性”C4-哦在这种情况下,与其他可能的醇作为亲核试剂)和立体选择性(α-麦芽糖)。
(例如,它是非常重要的颈- 1的取向缩醛绘制阿尔法(α)麦芽糖。贝塔(β)立体异构体完全是另一种二糖(纤维二糖)。]
类似的:
- 蔗糖(蔗糖)是一种二糖组成缩醛颈- 1之间形成的葡萄糖和果糖的c - 2(α-1→β-2链接)
- 乳糖是二糖半乳糖和C颈- 1之间形成4葡萄糖-哦(β-1→4链接)。
- 直链淀粉,淀粉的两个组成部分之一,是葡萄糖的多糖链通过(α-1→4)糖苷键。
糖之间的所有构建通过糖苷键的形成——换句话说,两种缩醛形成。
5。水解糖苷键的二糖
与乙D-glucopyranoside一样,上面添加水酸性多糖会回组分水解糖。
D-lactose,例如,可以水解回D-Galactose和葡萄糖水溶液酸:
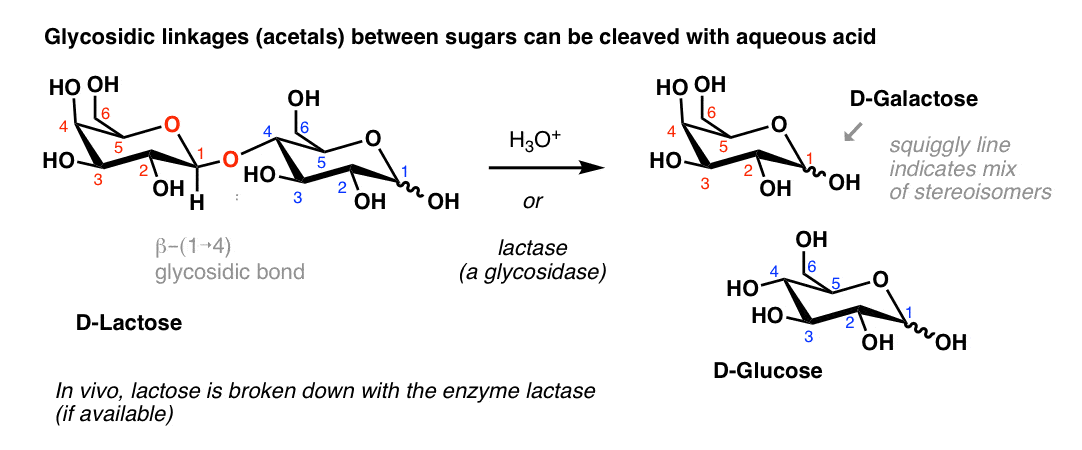
在生物体中,执行苷的水解酶,这些被称为糖苷酶。熟悉的条件”乳糖不耐受”是一个身体的结果缺乏必要的酶(乳糖酶)分解乳糖的糖苷键。
酶可以敏感立体化学。淀粉、葡萄糖的聚合物(α-1→4)糖苷键,很容易分解体内葡萄糖的单位,但纤维素(与(β-1→4)葡萄糖联系)。(有趣的事实:食草哺乳动物如牛依靠微生物在其肠道将纤维素转化成葡萄糖)。
6。酒精组糖的反应:选择性的问题
什么样的反应糖的羟基组接受吗?他们基本上只是醇,对吧?
我们探索了许多重要的醇的反应以前。假设我们想做一个坦诚的醇的反应威廉姆森醚合成在C -3葡萄糖-哦。
你可能记得,执行威廉姆森,所有我们需要做的就是添加基地和一个烷基卤,瞧,一个醚形式。
什么可能出错?
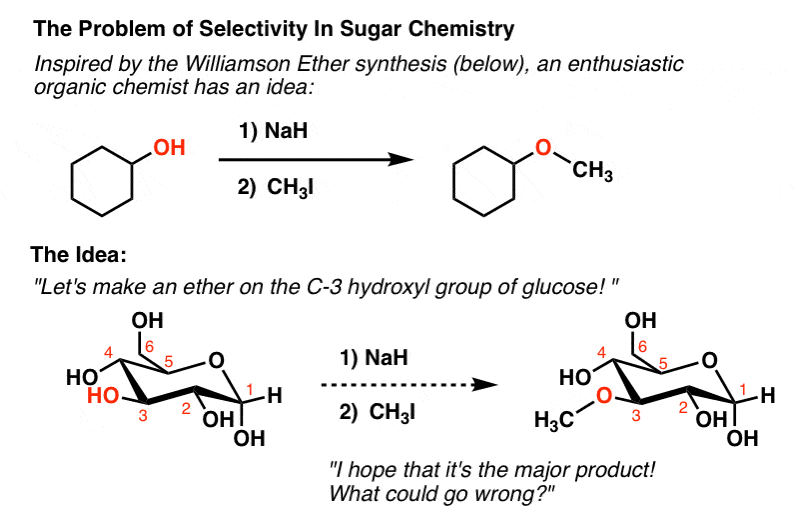
好吧,至少有四件事可能出错。颈- 3哦不是对CH明显更有选择性3我比任何其他四羟基。
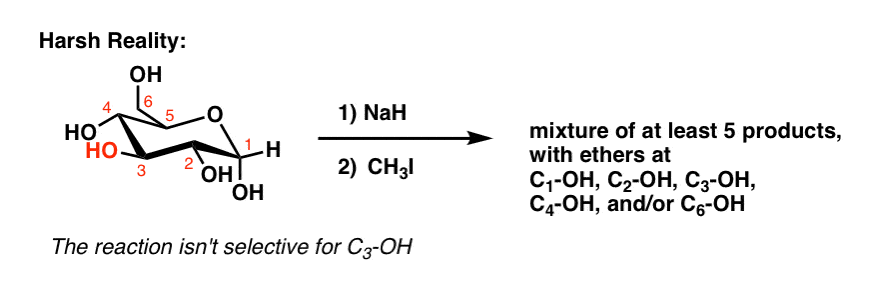
结果是一个混合的产品需要一个冗长的分离。
尽管现代有机化学的进步,没有办法威廉姆森而闻名醚合成发生有选择性地说,C3葡萄糖-哦好的收益率也没有形成其他羟基醚。
这似乎很难相信,但这是真的。我们越学习有机化学,我们学会欣赏是多么不可思议的自然是在设计非常有选择性的催化剂反应糖在特定网站不使用保护组。
仍然有许多发现在有机化学!
(有一个可靠的方法把一个醚糖和葡萄糖组。C6-哦是伯醇,因此不如另一位阻酒精组。可以使用一个非常笨重烷基卤化物等三苯甲基氯并让它反应选择性。看到注1]
无论你什么反应,氧化乙酰化、卤化、或甲硅烷基化,你几乎总是遇到这个问题不受保护的糖。一个解决方案。(注2]
7所示。蛮力方法选择性:使用过量的试剂
如果我们放弃所有希望的选择性,可以获得良好的收益率仅仅用一个巨大的治疗糖超过给定的试剂。例如,如果我们把过剩的葡萄糖甲基碘的存在基础,表示“五”醚在高收益。(我们有时称之为“彻底甲基化”)。(注3]
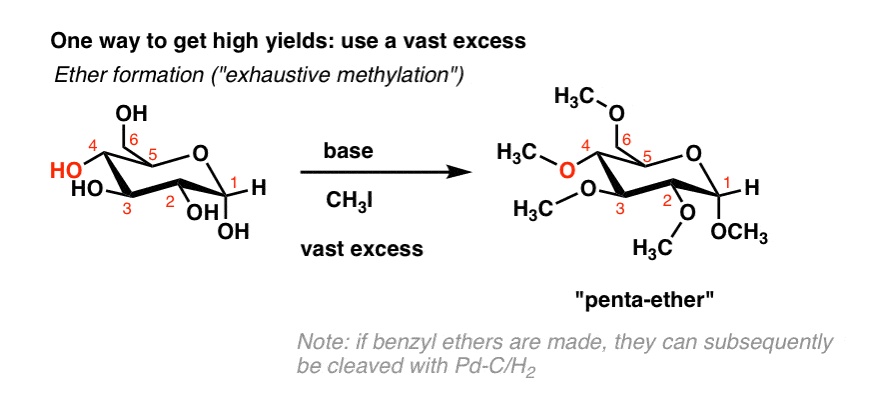
使用过量的乙酸酐,也可以形成一个“penta-acetate”:
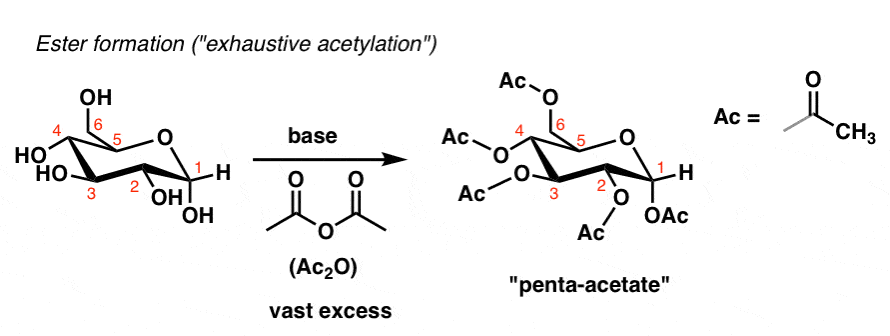
一些非常熟悉的塑料从现代生活的结果将多糖“详尽”条件下纤维素与各种试剂:
8。醚在颈- 1(异头碳)可以选择性地分开
一个音符。可以自由的颈- 1羟基表示“五”醚通过酸性水解,因为异头碳(颈- 1)的一部分缩醛。
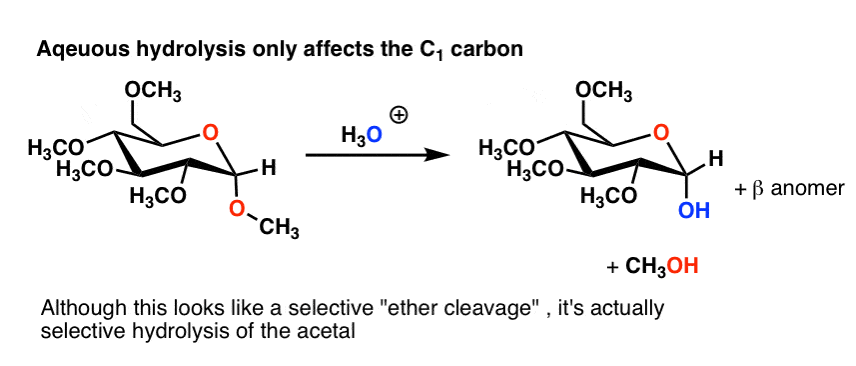
这可能看像一个醚劈理(通常需要一个非常严厉的酸如设定h)但实际上是水解的缩醛。(一个好的“诡计”考试问题!)。
9。在选择性问题怎么走吗?
直到我们开发催化剂,对手酶的能力有选择地与糖的羟基反应,剩下保护组策略。
在这一章我们简要介绍保护组织醇。(参见:“保护组醇”)与糖,保护组策略带到一个全新的水平。这是一个很大的话题,我们今天没有时间在这篇文章中。(不过,这是一个开始。]
一窥以外的土地(Org 3)
我认为保护组糖的策略是一个话题你可能称之为“Org 3”。
这是什么意思?
Org 1和Org 2课程,介绍各种官能团的性质及其主要反应。官能团主要隔离治疗。
这有点像国际象棋。Org 1和Org 2就像学习规则的游戏,以及部分(官能团)移动。
在组织3中,生活变得更加复杂。我们学习如何设计策略来处理许多现实生活中,一个分子具有多个活性官能团(如葡萄糖),我们需要选择性地形成一个债券只是其中之一。
或者在象棋术语中,你开始学习如何协调所有你的作品在一个总体战略。
与此同时,我希望这篇文章已经多少牛肉和面包。
笔记
三苯甲基组(三苯甲基)是如此该死的庞大,它往往只适合初级醇,因此反应选择性与其他羟基:
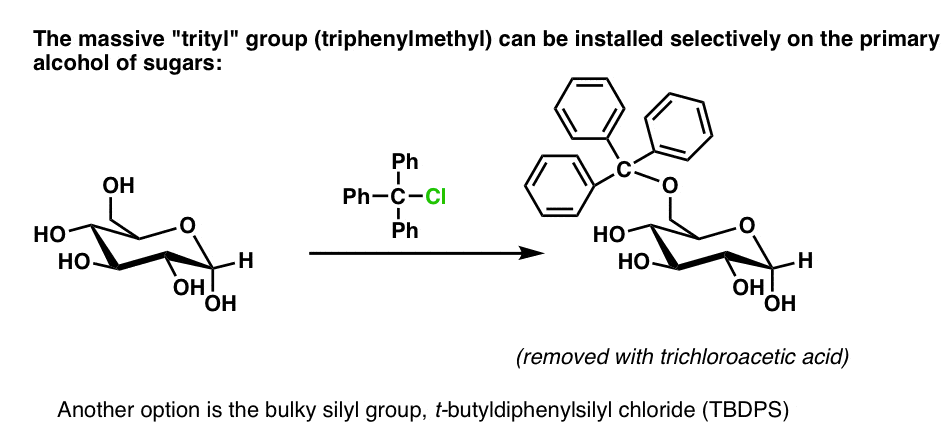
我可以从经验中说,它也感觉很好的把它放在后,因为你的产品的质量就会突飞猛进(“始于400毫克,现在我几乎有一克。——啊!”)。这种感觉消失了,然而,当它与三氯乙酸的删除。另一个选择是笨重的甲硅烷基组t-butyldiphenylsilyl氯(TBDPS)。
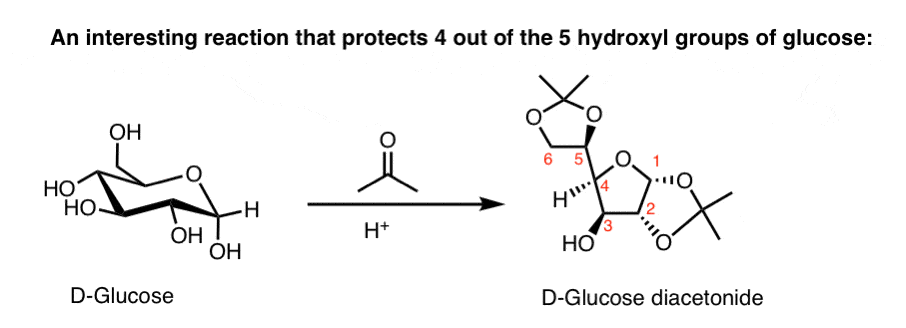
注2。这是远高于Org 2,但这是一个非常有用的保护序列,允许选择性功能化的葡萄糖供给。治疗丙酮和酸(也可以使用路易斯酸,如CuSO4)关系的4 5羟基醋酸酯(缩醛树脂的丙酮)。这使得颈哦,然后可以选择性甲基化(如果需要的话)。(这是用于Leucomycin Nicolaou合成的甲基醚颈的葡萄糖。看到“冒险在碳水化合物化学“更多精彩的例子。]
注3。这个反应的可逆的变体形式苄醚代替甲基醚(可出了名的难以打通)。的苄醚可以被治疗Pd / C和氢气。
(高级)引用和进一步阅读
- 酯化的主要酒精组碳水化合物与醋酸:一般的反应
r·b·达夫
j .化学。Soc。1957年,4730 - 4734
DOI:10.1039 / JR9570004730
早期的论文显示,选择性monoacetylation在主羟基是可能的,因为这是更活泼。 - 彻底甲基化的氨基葡萄糖
诺伯特•j . Wojciechowski拉尔夫•丹尼尔斯和伯纳德Ecanow
制药。科学。1961年,50(10)888 - 889
DOI:10.1002 / jps.2600501024
抽象状态:“葡萄糖胺的合成报道第四纪导数由化学和红外光谱方法研究。条件下报道了葡萄糖胺被发现成为退化和碘化tetramethylammonium成立” - 碳水化合物化学的应用Tin-Containing中间体
布鲁斯·葛第礼
放置碳水化合物化学。和生物化学。1998年,5317 - 142
DOI:10.1016 / s0065 - 2318 (08) 60043 - 8
的特定选择的酰化和烷基化锡缩醛树脂非常有用的选择性保护的多元醇含有系统,包括保护赤道在轴向羟基和区分两种赤道羟基与不同的空间环境。 - 冒险在碳水化合物化学:新的合成技术、化学合成、分子设计和化学生物学
海伦·j·米切尔博士博士k.c. Nicolaou教授。
Angew。化学。Int。。2001年,40(9),1576 - 1624
DOI:10.1002 / 1521 - 3773 (20010504)40:9
一个绝技审查k.c. Nicolaou教授(目前大米美国)详尽涵盖了碳水化合物化学及其在天然产物全合成中的应用。
当葡萄糖与硝酸反应,菲舍尔(考虑到结构的葡萄糖)只有醛基和最低酒精组结构被氧化生产砂糖酸。所以我的问题是,为什么不会其他酒精组结构的葡萄糖氧化
你好詹姆斯,很棒的主题! !我的问题是关于使用Tf2O Mesylation /甲苯磺酰化甚至。他们仍然选择OH-6喜欢三苯甲基集团吗?
不,你真的需要一个很庞大的保护组三苯甲基甚至tri-isopropylsilyl (TIPS)也将做这项工作。甲苯磺酰基和mesyl triflyl不够选择性;他们会打击一切。我不建议使用Tf,传递一个*大*离去基团,你可能会得到一片混乱。
笨重的取代基的攻击如何u伯醇的C6 C1碳也有主要哦组作为附加到C1进一步jst附加到C2。烷基的主要na吗? ? ? ?
C1碳不是主;这是半缩醛(一个蒙面醛)
哦在其他明显远离其他的分子比任何其他哦组,包括半缩醛在C1,使其更多的活性对笨重的保护组三苯甲基阴离子
如果你一个缩醛糖以外的实际缩醛参与糖苷键,然后你能缩醛水解?
亲爱的詹姆斯,谢谢你的努力。我想问你,如果我们用D葡萄糖反应香兰素。会发生什么?
无酸或其他试剂,最令人兴奋的事情是你的葡萄糖之间形成半缩醛羟基的醛香兰素。不是很令人兴奋。
嘿,詹姆斯
爱你的网站
会发生什么如果你反应与R-SH葡萄糖,硫醇,酸吗?葡萄糖与两个因此羰基氧在哪里?
詹姆斯,你化学人的神!
我肯定不会,但如果你发现了这篇文章有用,我很高兴。