二烯烃和MO理论
二烯烃的反应:1、2和1、4
最后更新:2023年1月8日|
动力学和热力学控制另外二烯烃的哈佛商业评论:1,2 - 1,4 -加法
在今天的文章中我们将讨论1、2、1,4 -二烯烃之外——具体来说,加入强酸如哈佛商业评论。
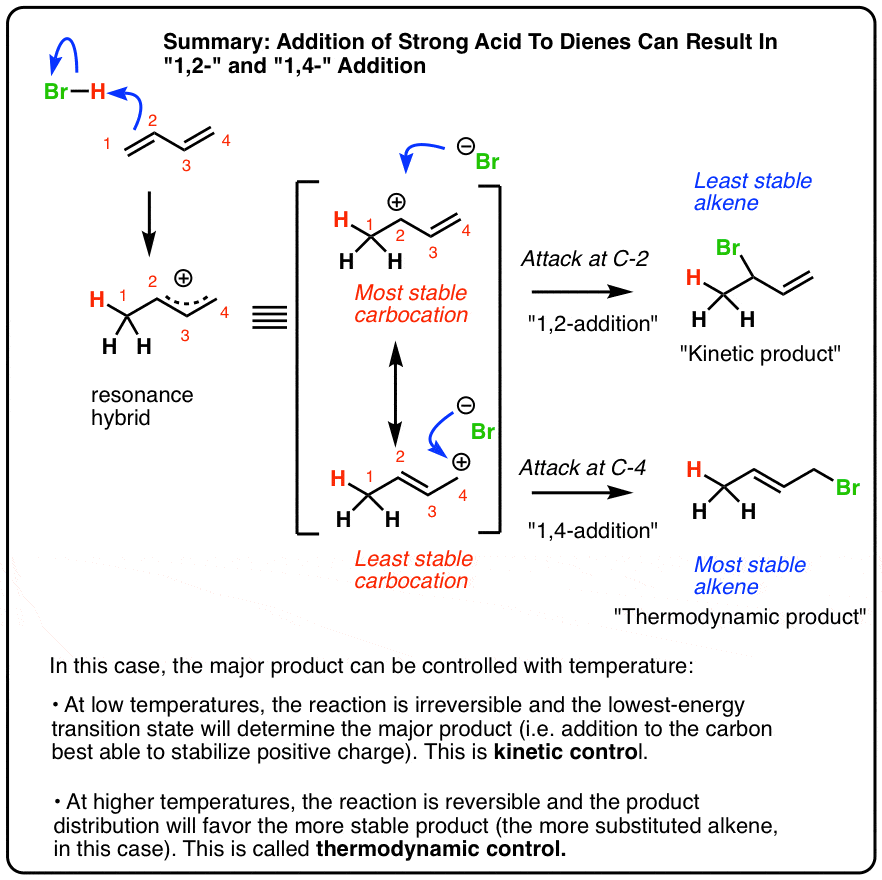
- 当一个二烯经历与强酸反应像哈佛商业评论,质子化作用的结果共轭系统碳正离子
- 共轭碳正离子上可以进行攻击两个可能的位置。
- 当反应进行低温度、反应不可逆转的和主要产品将最低的过渡态,即碳最能稳定正电荷。
- 这被称为运行下的反应动力学控制。
- 在更高的温度下进行反应时,反应可逆的主要产品是一个大部分热动力学稳定,这是一般的most-substituted烯烃。
- 这被称为运行下的反应热力学控制。
表的内容
- 烯烃,再现
- 丁二烯与酸的反应“加法”和“1,4-Addition”产品
- 酸的“1,4之外”的产品增加丁二烯
- 丁二烯的质子化作用使共轭碳正离子上
- 温度的影响:低温给“1、2”除了丁二烯
- 更高的温度给更多的“1 4”的产品
- 丁二烯,“1 4”的产品是更稳定的,因为它有更多的双键代替
- “运动控制”与“热力学控制”:在低温下反应是不可逆的,产品是由相对利率决定的
- 热力学控制:温度升高时的反应是可逆的,产品销售是由稳定
- 使用一个能量图理解热力学与动力学控制
- 分词的警告:“1,产品”并非总是“热力学”的产品
- 其他反应可以给1、2 - 1、4 -添加
- 笔记
- (高级)引用和进一步阅读
1。烯烃,再现
那样的一天我们讨论了烯烃的加成反应。还记得马氏规则的像在烯烃的亲电试剂的吗?
例如,像1-butene烯烃,并添加哈佛商业评论。会发生什么呢?
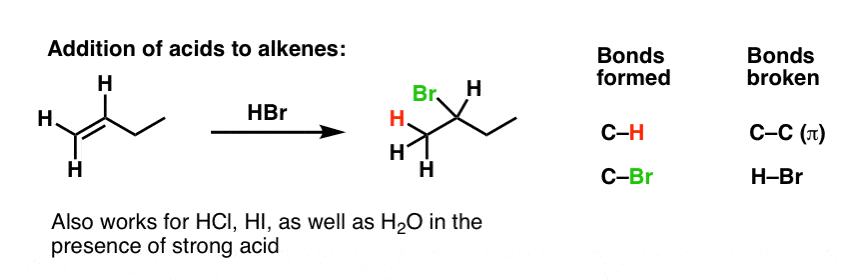
发生加成反应!(碳碳π,并形成邻碳氢键和C-Br债券)。
溴增加最取代碳烯烃的氢和增加了至少取代碳。这是因为碳正离子稳定性:反应所得最稳定的碳正离子,这恰好是最代替。
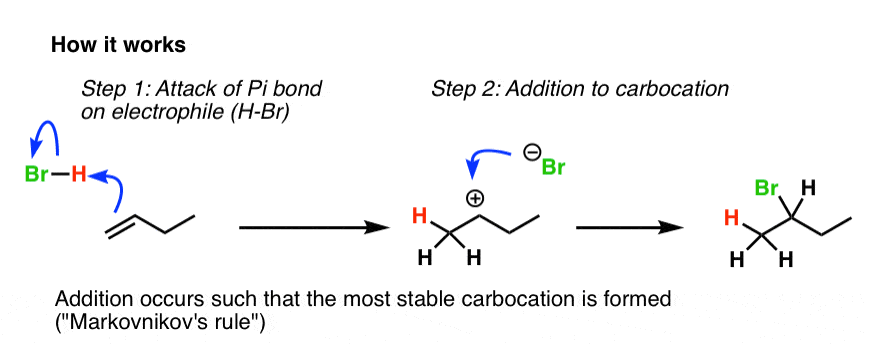
2。丁二烯与酸的反应“加法”和“1,4-Addition”产品
都很好。但是因为我们已经讨论结合共振,让我们加入一个额外的皱纹。
当我们尝试同样的反应二烯?例如,丁二烯。
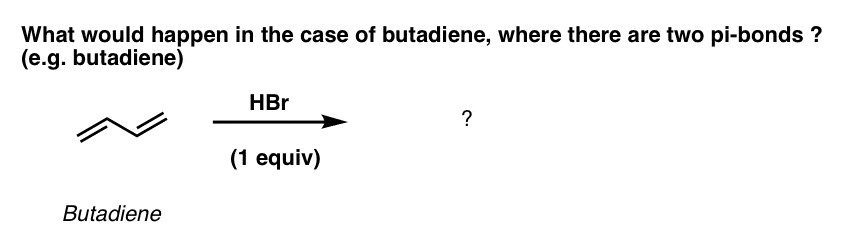
我将告诉你。你把两个产品!(但第二个可能不是你认为它是什么)。
他们是什么样子:
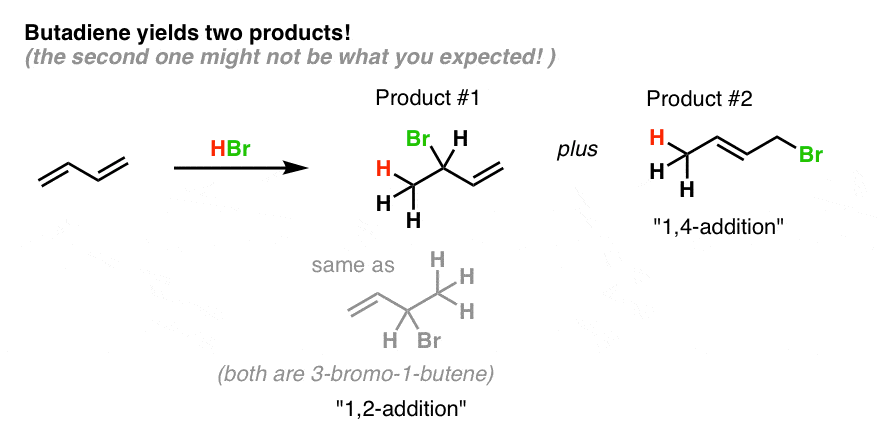
产品# 1基本上是同样的产品,我们看到1-butene例子:H和Br添加连续跨越两个碳双键。注意,由于丁二烯是对称的,同样的产品就形成了不管双键的参与!(我们两边都可以3-bromo-1-butene)。
因为除了发生在连续两个碳,我们常常称之为“1、2之外”。
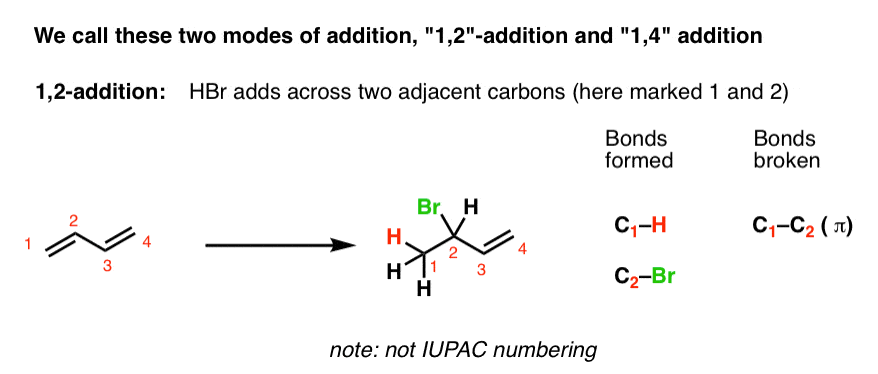
3所示。酸的“1,4之外”的产品增加丁二烯
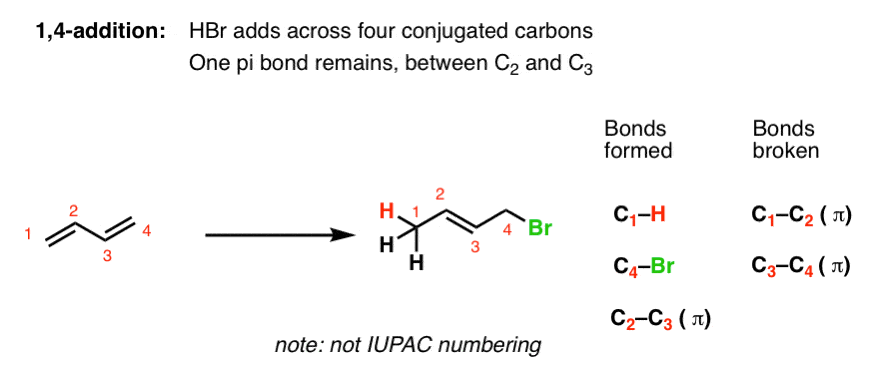
相比之下,产品添加H和Br的# 2显示了结果四个共轭碳。所有四个碳参与反应。一个新的碳氢键单键形成了一端的二烯(颈- 1),和C-Br形成在另一端(c - 4)。注意,C1- c2和C3- c4π键断裂,我们成立了一个新的C之间的π键2和C3。
我们称之为“1,4之外”。
【注:为了简化讨论,我选择忽略双键同分异构体(例如E和Z)在这个分析。在实验室里,1,4 -上面的例子将存在的混合物(大部分)E的z)和少量的产品
那么为什么这个“1 4加法”发生在第一个地方吗?丁二烯有什么不同呢,而不是1-butene只有“加法”是可能吗?
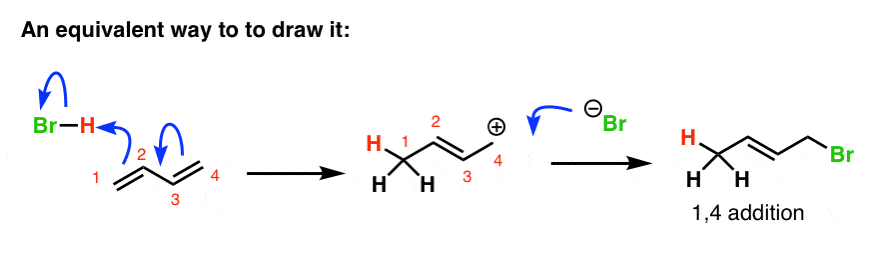
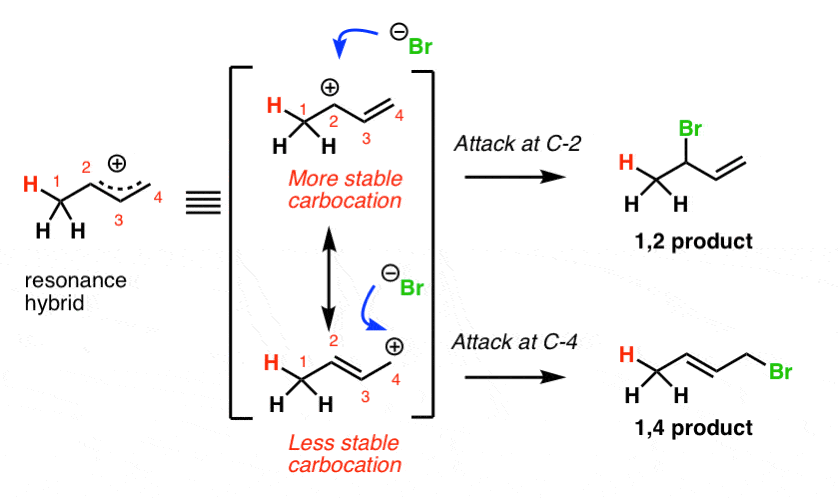
4所示。丁二烯的质子化作用使共轭碳正离子上
首先要注意的是,最初的丁二烯的质子化作用给出了共轭碳正离子上。看到颈- 1的质子化作用给出了共振形成碳正离子,有两个重要?
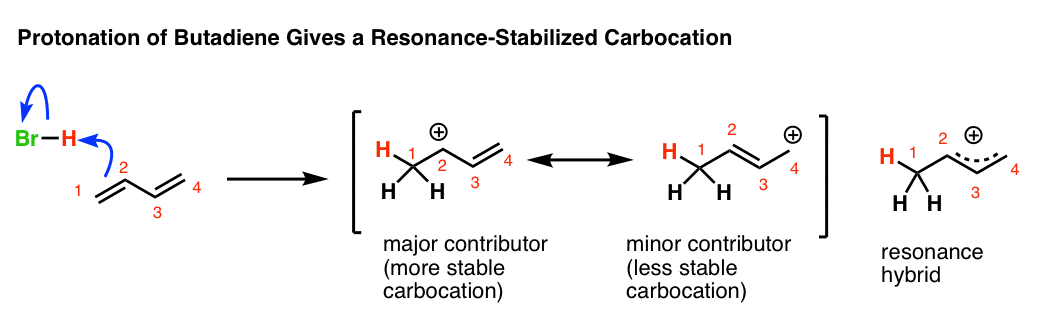
在丁二烯的情况下,
- 的主要因素共振混合动力将是碳正离子的共振形式取代碳正离子(C2)
- 的次要的因素将共振形成碳正离子在哪里少取代碳正离子(C4)。
亲核试剂的进攻(Br- - - - - -在C)2位置的混合将导致1,2-product。
Br的攻击- - - - - -在C4共振杂化将导致1的位置,产品。
(注意:永远不要忘记这一点共振形式是不在平衡彼此。是可以理解随便说“Br(-)将攻击顶部共振形成更稳定的碳正离子”只要你记住,真正的分子的结构混合动力两个共振形式。)在脚注等,我也许一个更正确的方法来显示底部共振形成的形成。
5。温度的影响:低温给“1、2”除了丁二烯
这是最大的问题:两个产品将主要的哪一个?1、加法产品或1 4-addition产品?
我们习惯看到“马氏加成”烯烃(除了发生最稳定的碳正离子),直观看来,1,加法产品将占据主导地位。
事实上,在较低的温度下,1、2除了丁二烯是青睐。这是一个文学的例子。
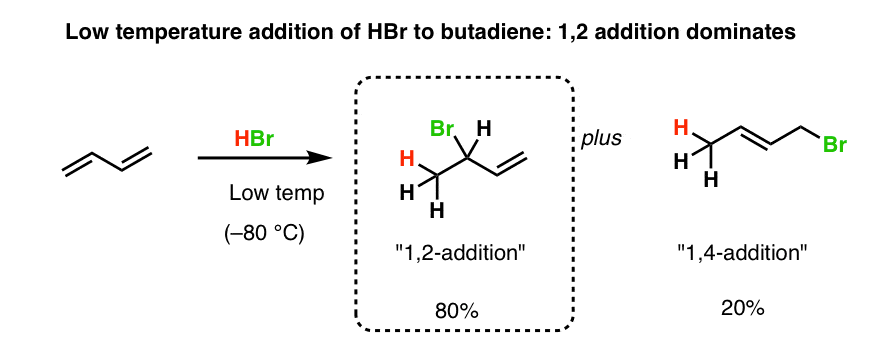
6。更高的温度给更多的“1 4”的产品
然而,有趣的是,随着温度的增加,1、4产品增加。
在室温下,1比2 - 1,4 -除了45:55。
在40摄氏度,4 -产品主导(大约80%)。
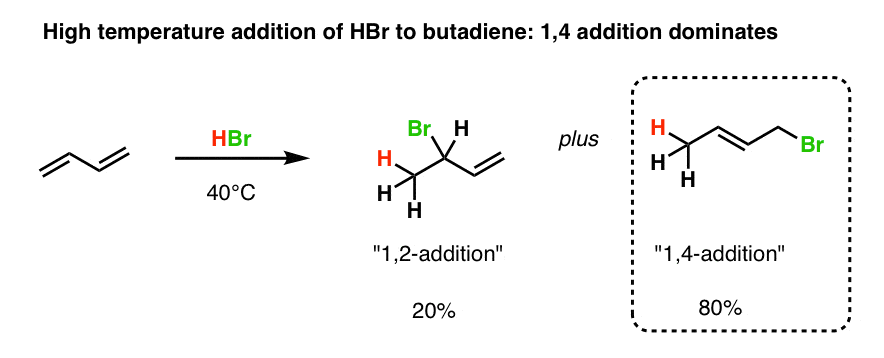
7所示。丁二烯,“1 4”的产品是更稳定的,因为它有更多的双键代替
这是怎么回事?什么结构特点的存在可能使形成1,4比1,产品更有利的2个产品,即使它经过一个“不稳定”碳正离子?
答案就在于双键的替代模式。
还记得扎伊采夫规则吗?同样的协议。1、4产品更加稳定,因为它是一个更代替双键。
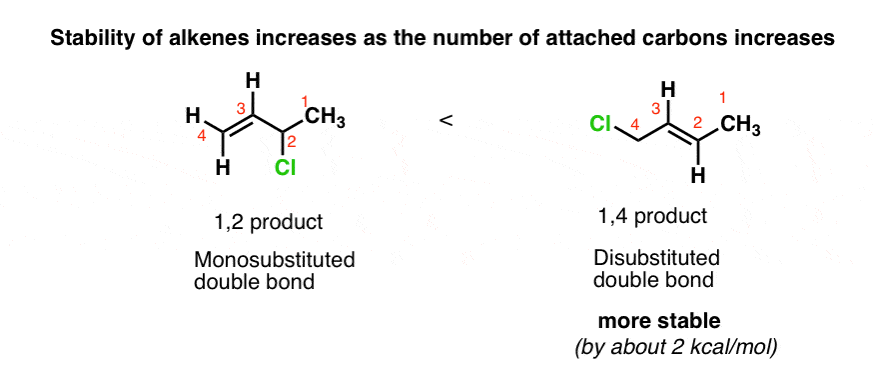
1、4产品di -代替双键,而1,2-product有mono -代替双键。一般来说,双键稳定性随着碳原子数量的增加直接附着在双键增加。(见文章:烯烃的稳定性)
所以为什么1 4更青睐温度较高的条件下,1,2是支持较低的温度条件下?
8。“运动控制”与“热力学控制”:在低温下反应是不可逆的,产品是由相对利率决定的
在低温下,微分系数的相对能量过渡状态导致的产品。1、2产品有一个较长的过渡态,由于电荷是更稳定的碳代替。这些转变的能量状态之间的区别将决定产品的比例。
一个简单的类比。想象你饿了,你只有5美元在你的口袋里。选择麦当劳而阿普尔比连锁餐厅,麦当劳——即使只访问选项,出于某种原因,你喜欢阿普尔比连锁餐厅的更多。
让我们画出来。碳正离子中间体可以通过两种不同的过渡状态,导致1,2 - 1,4 -产品,分别。如果我们选择温度足够低,那么产品销售将反映两者之间的能量差异激活能量E一个(1、2)和E一个(1、4)。只要反应是不可逆的与较低的能量过渡态,产品将占据主导地位。这就是所谓的“运动控制器l”。
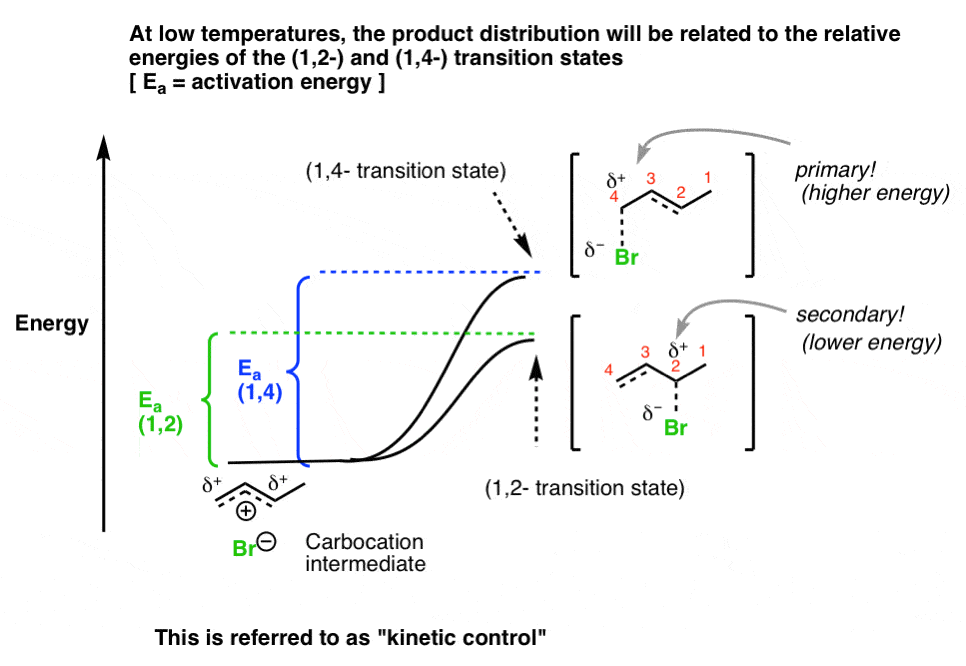
9。热力学控制:温度升高时的反应是可逆的,产品销售是由稳定
在更高的温度,反应有潜力可逆的。(注2]在这种情况下,这意味着两个1,2 - 1,4 -产品电离(想到的第一步N1反应),改革碳正离子中间体。
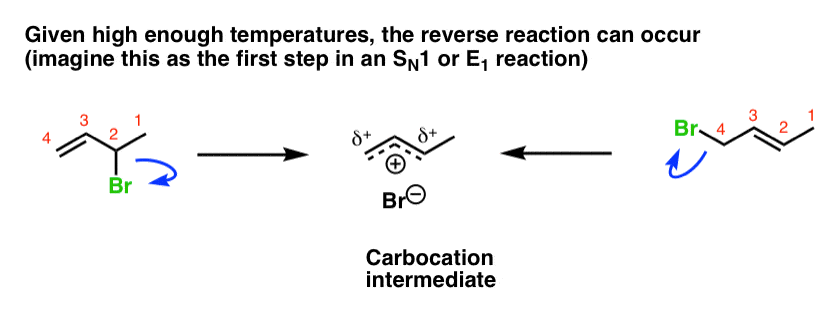
这设置了一个平衡。产品比现在反映的相对稳定性1,2 - 1,4 -产品,导致他们形成不过渡状态。丁二烯的情况,因为1,4 -产品更稳定(它有一个双取代的双键),它将主导产品在更高的温度。
这是被称为“热力学控制”。
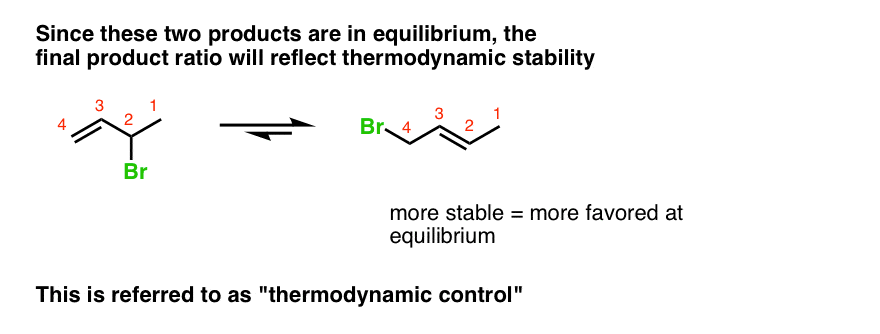
数学插曲:记得ΔG = rt lnK
1千卡每摩尔的差异稳定听起来并不多,但它转化为83:17在室温下产品的比例平衡。
继续我们的类比:有足够的钱在你的口袋里,决定去哪里吃午餐更多少你喜欢的函数整体麦当劳与阿普尔比连锁餐厅的经验,不是他们多少钱。
10。使用一个能量图理解热力学与动力学控制
拟定的反应能量图可以帮助理解动力学和热力学控制。这篇文章在这里进入更详细的,但我们会在这里重复基础。
哈佛商业评论的反应能量图添加丁二烯看起来像这样:
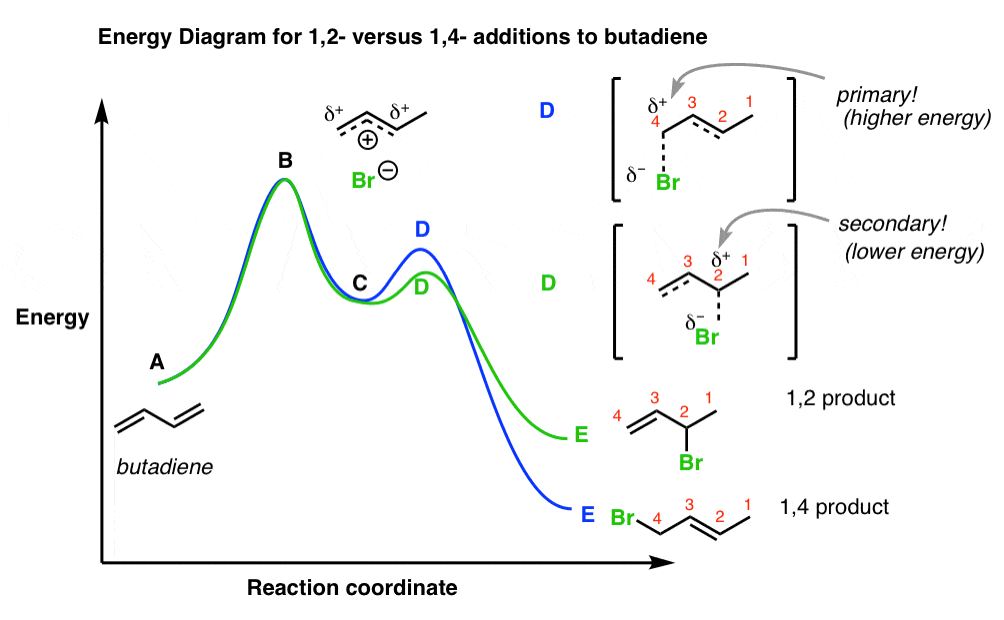
点一个是开始丁二烯,点B是增加H丁二烯的过渡态。
关注最重要的部分是“局部最小值”C共轭碳正离子上。
正如我们前面提到的,从中间C过渡状态D和D代表了能源通道1,2 - 1,4 -而且,分别。
因此正向反应的激活能量等于能源之间的差异D和C(1、加法)D和C(1、4-addition)。我们发现1,加法活化能较低。
现在让我们来看看相反的反应。
点E和E代表的能量1,2 - 1,4 -产品。
的活化能反向反应是能源之间的区别E和过渡态D,E和过渡态D,分别。
从这个图应该清楚,正向反应的活化能(从C通过过渡状态D和D给E和E分别)远远低于激活能量的逆反应(即E和E通过过渡状态D和D回到碳正离子C)。
- 如果我们保持较低的温度,我们支持正向反应,阻碍相反,和获得动力产品。
- 如果温度提高,逆反应变得积极,和建立平衡。我们将获得热力学的产品。
11。一个Parting Word Of Warning: The “1,4-Product” Is Not Always The “Thermodynamic” Product
让我们总结一下。理解下列两个因素是正确回答考试问题的关键。
碳正离子共振形成的相对重要性- 的相对稳定性双键产品。
丁二烯的情况下,它是真实的1、2产品形成了一个更稳定的碳正离子(动力产品),和1、4产品有一个更稳定的双键(热力学产品)。
但它并不总是适用于所有二烯烃! !
这里有三个例子,这将有助于你思考的主要问题(答案在接下来的帖子)。
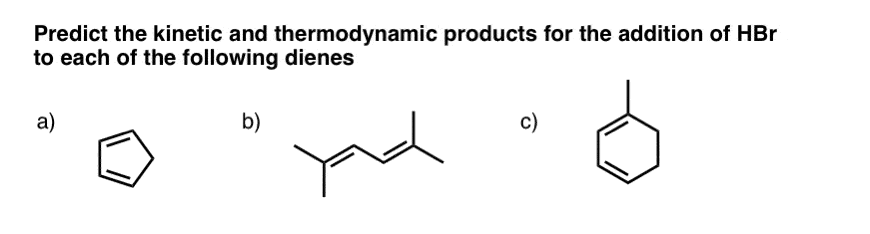
12。其他反应可以给1、2 - 1、4 -添加
这篇文章是足够长的时间,但如果如果我未能注意,就是我的失职了1,2和1、4增加双烯也可能一些其他类的反应。
- 哈佛商业评论与二烯烃自由基条件下(例如:哈佛商业评论+过氧化物)
- 添加溴2(和Cl2二烯烃。
注意,类似的问题将会出现(即稳定的活性中间体和最终产品的稳定性)。我们会详细的时候。
非常感谢汤姆Struble帮忙准备这篇文章。
笔记
注1。我咨询的所有教科书显示图表类似于上面我画,与Br(-)攻击不同的共振形式。也许一个更正确的方法画形成碳正离子的四工位是这样显示。
(高级)引用和进一步阅读
- 添加氢氯丁二烯
j . m . s . KHARASCH KRITCHEVSKY, f·r·梅奥
《有机化学》杂志上1937年,02(5),489 - 496
DOI:10.1021 / jo01228a010
早期论文的受人尊敬的化学家m . s . Kharasch添加盐酸丁二烯,看到的比率是否1,2,4加成反应条件不同而不同。 - 在添加试剂过氧化效应不饱和化合物。十三。丁二烯的溴化氢
m . s . KHARASCH艾莉·t·马戈利斯,弗兰克·r·梅奥
《有机化学》杂志上1936年,01(4),393 - 404
DOI:10.1021 / jo01233a008
另一个早期研究m . s . Kharasch他研究的哈佛商业评论丁二烯,他试图严格分开的两种模式——亲电与激进。 - -Mobile-anion互变现象。第一部分的激活条件的初步研究3个碳系统,并讨论结果与除了共轭系统的模式
哈罗德•波顿和克里斯托弗Kelk英格尔德
j .化学。Soc。1928年,904 - 921
DOI:10.1039 / JR9280000904
经典论文从物理有机化学的先驱者,c·k·英格尔德教授。他建议一般认为1、2和1、4添加产品处于平衡状态,1,2-product能扭转反应并形成1,4个产品。这是我们现在所称的“动能”的基础,“热力学”控制。 - 除了共轭不饱和系统的模式。第九部分。的讨论机制和平衡,3个碳上有一张纸条prototropy
p . b . d . de la母马·e·d·休斯和c·k·英格尔德
j .化学。Soc。1948年,17
DOI:10.1039 / JR9480000017
这里,c·k·英格尔德了所有工作(包括Kharasch)做对的事情在亲电增加共轭系统的研究。 - 共轭化合物的性质。习的一部分。溴化氢与βγαδ-dimethylbutadiene
欧内斯特·哈罗德农民和弗雷德里克·g·b·马歇尔
j .化学。Soc。1931年,129年
DOI:10.1039 / JR9310000129
当甲基添加到丁二烯、1、2和1、4添加比例能显著改变!这是因为碳正离子中间体的稳定性将会改变。
我只是想谢谢你,谢谢!
欢迎你潘文凯,高兴你有帮助。
为什么更稳定的中间有一个门槛降低它的过渡态?不应该相反的是真的吗?
你好,
我们在哪里可以找到解决方案三个例子向结束?
谢谢!
J
在下一篇文章://m.dermacare3d.com/2017/04/11/more-on-12-and-14-additions-to-dienes/
复杂的概念很容易
你们有提供课程从头到熟练水平吗
回到我的邮件id吗
我感兴趣的一个常规课程,迫使你去学习
是一个导师
时间应该是6到9个月左右
有情况是1、2和1、4个产品是相同的,不管温度?
确定。环戊二烯,1 2哈佛商业评论和1、4的哈佛商业评论给你相同的产品:3-bromocyclopentene