芳香性
芳香性规则
最后更新:2022年10月27日|
芳香性的规则:四个关键因素
在最后一篇文章里,我们介绍的概念芳香性房地产的一些异常稳定的苯等有机分子。尽管一些芳香分子确实是香(你好,香兰素!)“芳香性”这一术语实际上无关的气味。我们看到芳香分子:
- 有一个非常高的共振能量(苯36千卡每摩尔)
- 接受替换而不是除了反应
- 有离域π电子
我们也给出了一些例子以外的其他分子苯的芳香,和一些类似于苯(如环辛四烯)。
规则是什么呢?我们如何判断一个分子芳香吗?
表的内容
- 四个关键芳香性规则
- 条件为芳香性# 1:分子必须循环
- 条件# 2:必须共轭环中的每个原子
- 条件# 3:分子必须4 n + 2π电子
- 电子数为“π电子”?
- 吡啶和苯离子
- 一些例子5环
- 条件# 4:分子必须是平的
- 摘要:为芳香性规则
- 笔记
- (高级)引用和进一步阅读
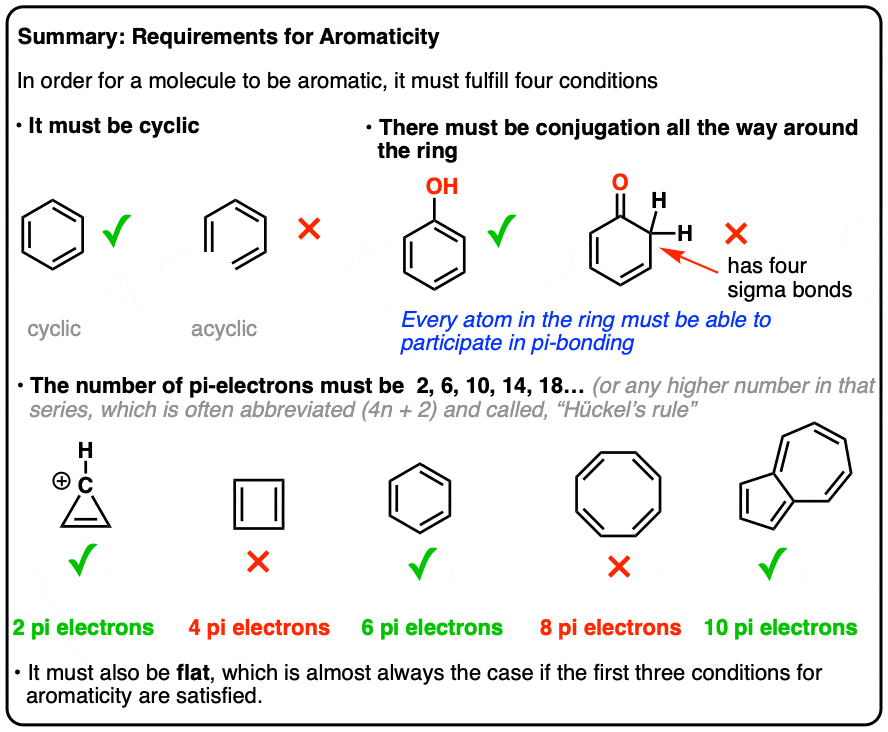
1。四个关键芳香性规则
是4条件有一个分子必须满足为了芳香。
全有或全无。如果这些条件的任何违反,没有芳香性是可能的。
- 第一个,它必须循环。
- 第二个,每个原子环必须共轭。
- 第三,分子必须4 n + 2π电子(我们将深度解释这是什么意思,下面)
- 第四,分子必须平(通常如果满足条件1 - 3,但有罕见的例外)
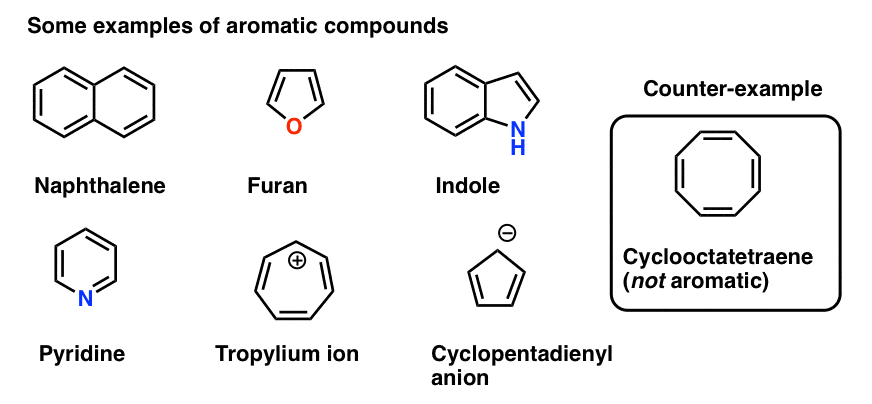
让我们详细。
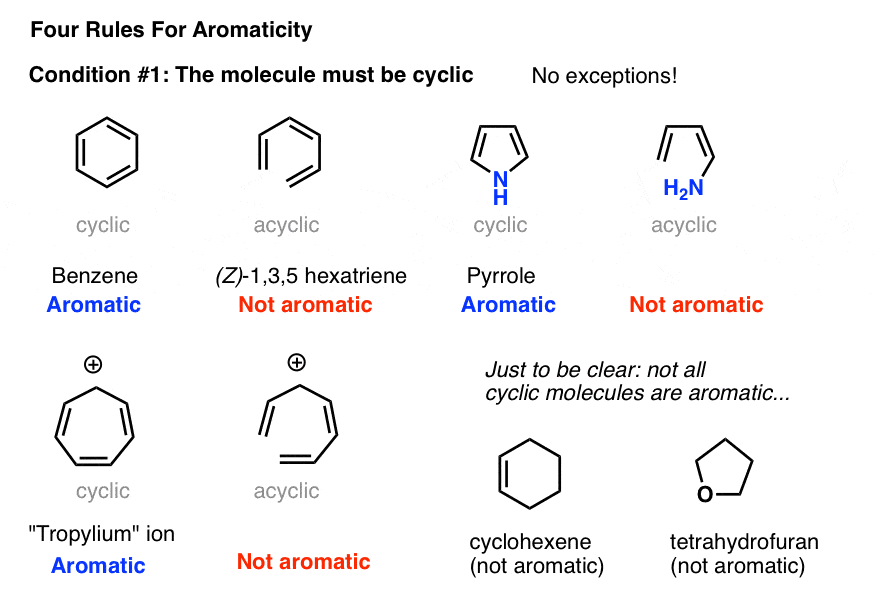
2。条件为芳香性# 1:分子必须循环
确定一个分子是循环很简单。有戒指吗?如果是的,搬到条件# 2。如果没有戒指,算了吧。
例子:Z)1、3、5 hexatriene有相同数量的π键和π电子苯,但不是芳香。没有戒指,没有芳香性。
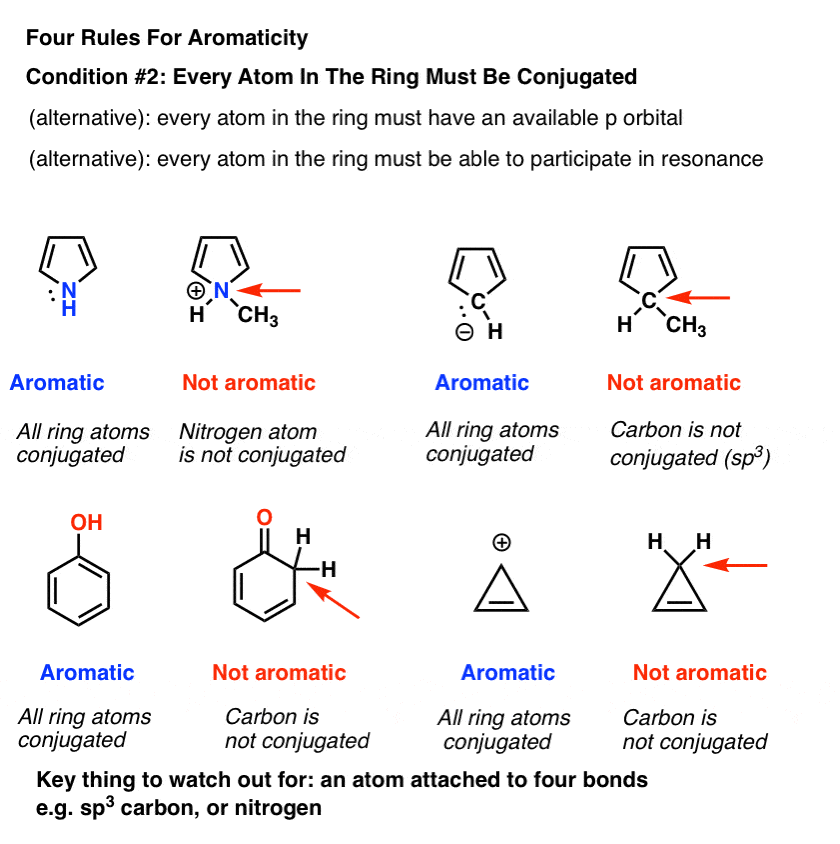
3所示。条件为芳香性# 2:必须共轭环中的每个原子
很明显,被循环不是芳香性的一个充分条件。看看环己烯,上面。没有芳香。
aromaticty为了存在,也必须有一个p轨道的一个连续的环圈,建立成一个更大的循环“π体系”。
说的一个方法是每个原子周围的环必须的能力动词的词形变化彼此。
有一些替代方法说同样的事情。
我们也可以说:
- “每个原子环必须有一个p轨道”,或
- “每个原子环必须能够参与共振”。
记住“可用p轨道”条件不仅适用于原子π键的一部分,而且原子轴承孤对,激进的或空的p轨道(如碳正离子)。(参见这篇文章结合和共振如果你不确定)。
“杀死”结合的关键sp3原子杂化原子和四个键。这样一个原子不能参与共振。
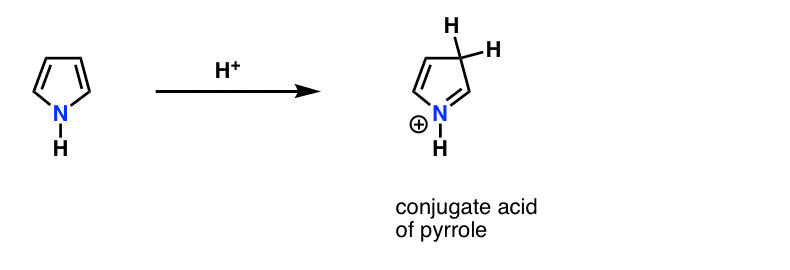
这就是为什么上孤对吡咯(下图)并不像你所期望的基本氮。质子化作用的氮会破坏周围的共轭环,破坏过程中芳香性。(注1]
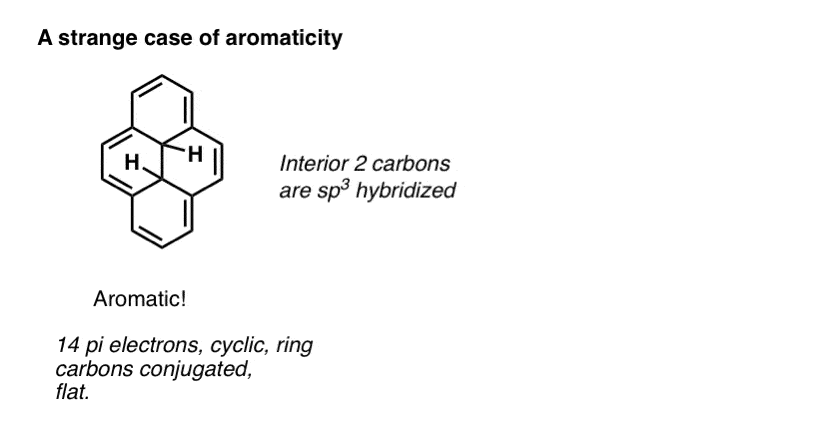
先进的注意。有几个分子共轭的四周环,但内部碳sp3杂化。仍然是芳香。(注2]
4所示。条件为芳香性# 3:分子必须4 n + 2π电子
第三个条件是,循环,共轭分子必须具有正确的π电子的数量。苯和环辛四烯都是循环和共轭,但苯是芳香环辛四烯并不是。所不同的是,苯已6π电子,和环辛四烯8。(我们将解释为什么这一个区别在随后的帖子)。
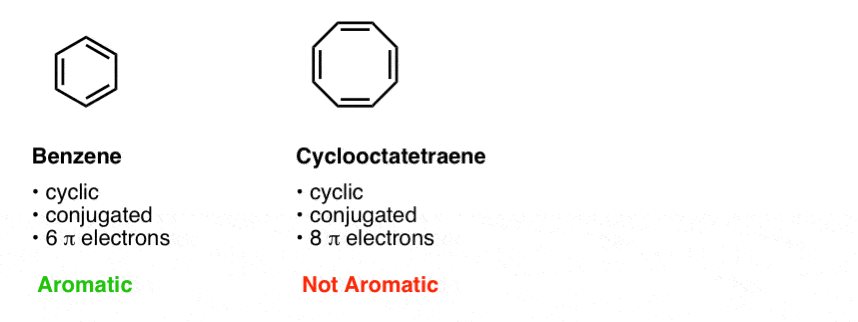
我们经常使用我们快速速记是说苯4 n + 2π电子和环辛四烯没有。
然而,这个术语(4 n + 2)在有机化学造成很多混乱。我认识的学生谁会盯着一个分子,试图找出什么是“n”。
“n”不是一个分子的财产!
评论者克莱尔有一个伟大的方式把它:
“4 n + 2不是一个公式适用于看看你的分子是芳香。这是一个公式,告诉你的数字是什么魔法系列。如果你的π电子值匹配任何数量在本系列芳香性的能力。”
完全正确!“魔法系列”是:2、6、10、14、18、22……(和计数高于4之后)。(注3]
(4 n + 2)是数学系列缩写(2、6、10、14、18、22…]。
我们可以通过插入本系列生成整数(n = 0, 1, 2, 3, 4…) (4 n + 2)公式。这些“n”的值与分子。我们只是用它们来生成系列。
对于n = 0,我们[4 (0)+ 2]=2
对于n = 1,我们[4 (1)+ 2]=6
对于n = 2,我们有[4 (2)+ 2]=10
对于n = 3,我们[4 (3)+ 2]=14
等等。看看它生成系列(2、6、10、14…)?这是[4 n + 2]。
这个“神奇的数字系列”有时也被称为“Huckel数字“Erich Huckel之后,他早在1931年就提出了这一规则。
条件是芳香分子必须[4 n + 2]π电子有时被称为“休克尔规则”。
在下面的图中,分子实现休克尔规则是绿色的;那些不满足休克尔规则是红色的。
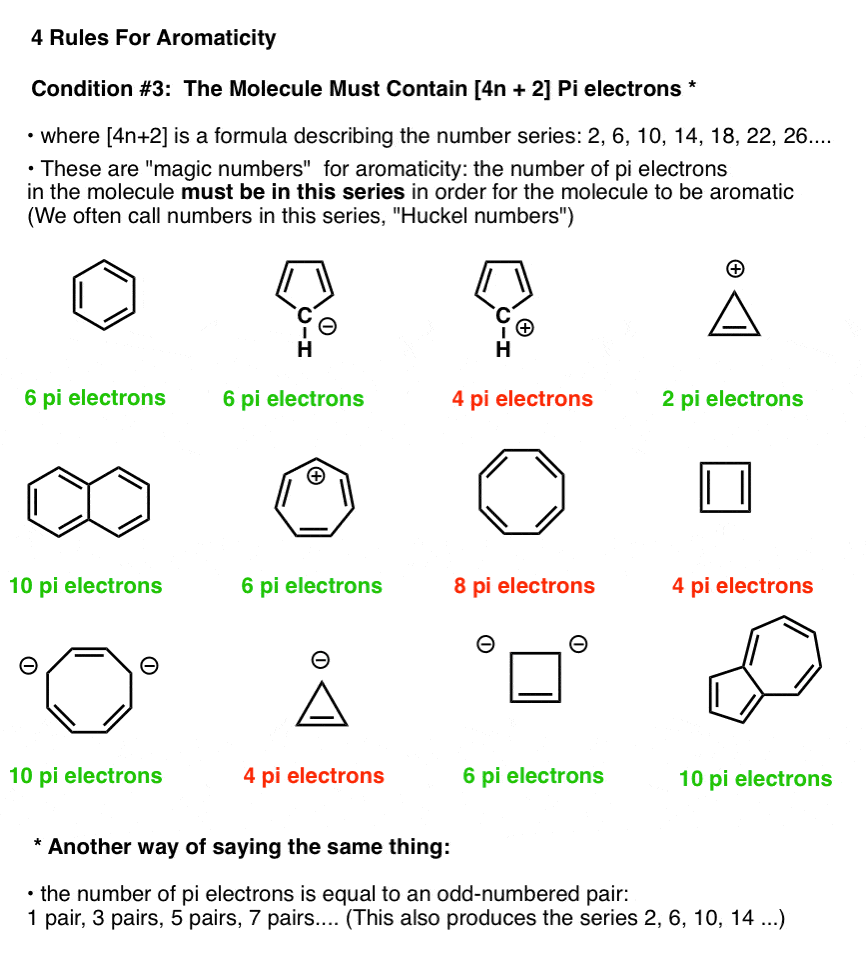
注意,我们可以计算出电子π键以及电子从孤(只要碳不是已经参与一个π键,见下文)。因此,环戊二烯负离子有六个π电子- 4两个双键,和两个孤对碳的。
5。电子数为“π电子”,哪个不?
这似乎非常简单。然而,并发症可能出现当我们有原子参与π键和环也有孤对。例如,
- 我们如何计算苯中电子阴离子(下图左)或吡啶吗?我们计算π电子的孤对电子,给共有8 ?还是我们忽略它们?
- 关于呋喃(中间),有两个孤对氧气吗?
- 吡咯,氮上的孤对,或咪唑,与两个氮吗?
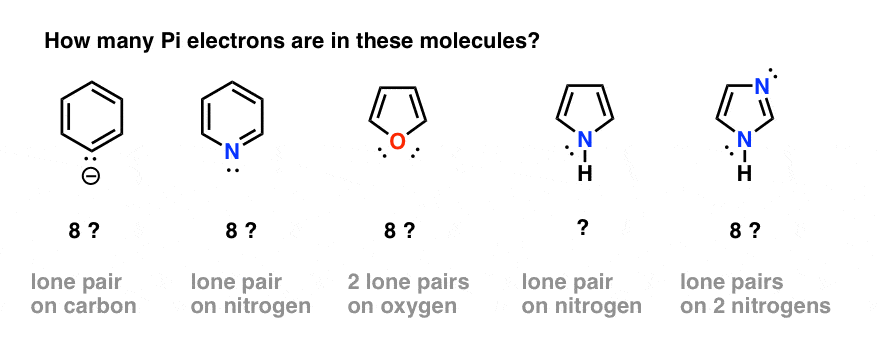
为了回答这些问题,重要的是要提醒自己的p轨道导致苯的芳香性。
在苯中,每一个p轨道有序地排列在平面直角(90°)的戒指。每个p轨道包含一个电子。我们可以验证π电子的总数在苯通过计算π键:3π键*两个电子= 6π电子总数。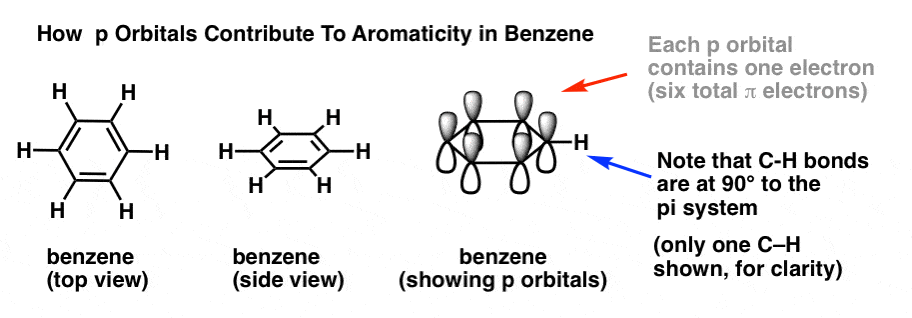
注意,碳氢键在90°的π体系。如果有一个孤对碳氢键在哪里,那么它就不能与π交互系统。这让我们…。
6。有些电子不计数:吡啶和苯离子
苯离子有孤对一个碳原子。这个孤对不可能在一个p轨道,因为p轨道参与π体系。相反,在90度的π体系,在平面上的戒指。
换句话说,孤对碳不算作两个π电子,因为它不能与pi系统重叠。
同样也是如此吡啶,孤对还在直角π体系。
因此,尽管在每种情况下你可能会说他们有8个π电子,正确的答案是6。这是Huckel数量,实际上这两种分子芳香。
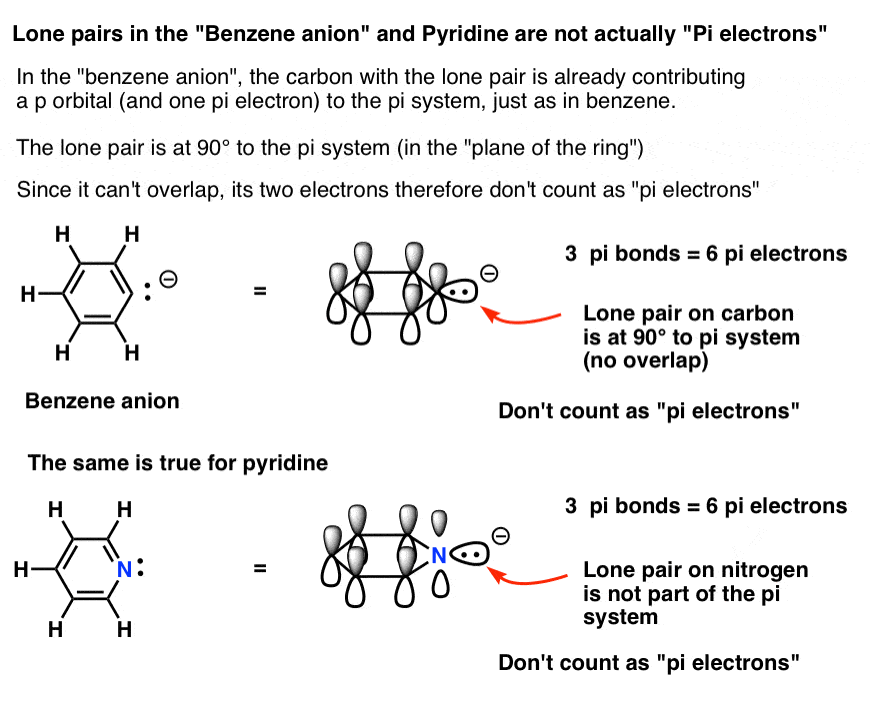
底线是:每个环原子可以贡献最大一个p轨道向π体系。
7所示。芳香5环的一些示例
一些分子五元环也可以出现歧义。
环戊二烯负离子(下图)有孤对的碳原子。这孤对导致π体系吗?
由于碳没有参与任何pi-bonding,答案是是的。
环戊二烯负离子的π电子的总数= 2(从孤对)+ 4电子在两个π键,给我们总共6。这是一个Huckel号码和环戊二烯负离子实际上是芳香。

出现类似的情况吡咯。氮熊孤对,但没有参与一个π键(与吡啶,上图)。因此有助于π体系,这给了我们一共有6π电子一旦我们占了4个电子的两个π键。

一个奇怪的情况呋喃熊,氧气两个孤独的对。这是否意味着呋喃8π电子吗?不!
为什么不呢?因为我们上面所提到的,每个原子都可以贡献最大一个p轨道对π体系。呋喃,孤对p轨道,导致了π体系;另一种是在平面上的戒指。这给了我们一共有6π电子。呋喃是芳香。(所以噻吩、呋喃硫模拟)。

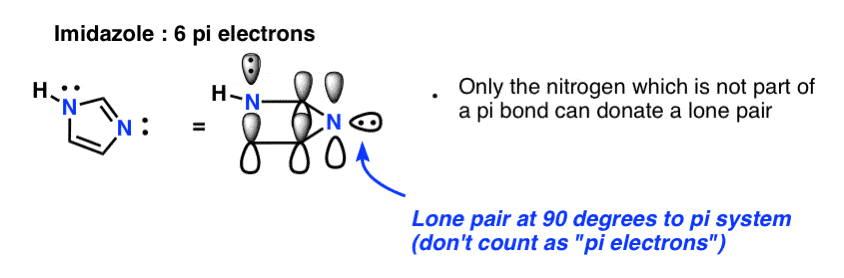
终于有咪唑两个氮,。一个氮(h)不是参与一个π键,因此可以提供一个完整的孤对;另一个是参与一个π键,孤对在平面上的戒指。这也给了我们一个共有6π电子一旦我们占两个π键。
8。条件为芳香性# 4:分子必须是平的
第四个条件为芳香性的分子必须平(平面)。
芳香性是这样一个稳定属性(价值20-36千卡每摩尔),通常这是一个分子
- 循环
- 共轭
- [4 n + 2]π电子吗
也会平的。给一个分子一个足够大的势能,它最终会变成的。
这有点像旧的妙语(原油)开玩笑为什么狗采取一定积极有利的构造:“因为他们可以”。
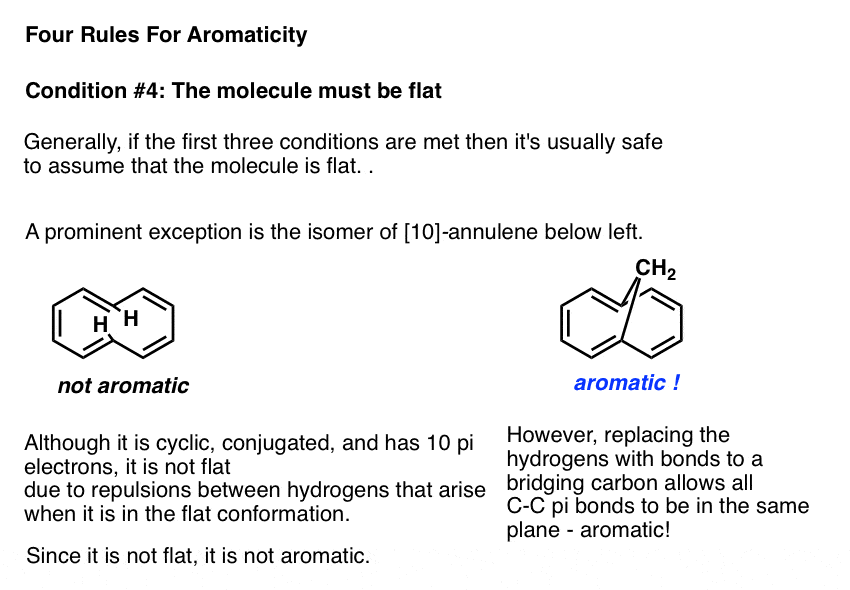
与某些脊椎动物一样,唯一阻止分子满足前三个条件持平,如果平面构象非常紧张。这类的一个例子是分子称为[10]轮烯,一种异构体的下面画了。在反式,独联体,反式、独联体、cis异构体的分子是循环、共轭和10个π电子,但这两个氢原子碰撞时试图采用平面构象。
分子阻止采用平面性是由于这种惩罚性的范德瓦耳斯应变,因此没有芳香。
有趣的是,如果氢被删除,取而代之的是一个桥接CH2组织应变松了一口气,π键可以采用平面构象。下面的分子正确显示预期的芳香分子的性质。
9。摘要:为芳香性规则
这篇文章通过一个分子必须满足的四个条件是芳香。
一般来说,决定如果循环和共轭分子不是什么会绊倒人。
这是该死的πelectron-counting !
在下一篇文章中,我们将玩游戏秀”这是芳香吗?”with a series of different contestants and try to demonstrate a relatively quick n’ easy plan for determining if an unknown molecule is aromatic or not.
这以后,我们将看看分子轨道,试图了解到底是什么如此特别Huckel系列。
感谢马特Knowe援助与这篇文章。
笔记
注3。应该注意的是,休克尔规则开始分解为高数量的π电子(> 20)多环系统。我不会进入这里的细节。维基百科的文章涵盖了它。
(高级)引用和进一步阅读
- Quantentheoretische Beitrage zum Benzolproblem
死Elektronenkonfiguration des粗苯和学会Verbindungen
Erich Huckel
Zeitschrift毛皮物理学1931年,70年,204 - 286
DOI:10.1007 / BF01339530
Erich Huckel实现识别的详细说明,以及彼得·德拜理论强电解质在1923年,后来通过应用一个简化版的量子理论中p电子共轭分子,这被称为Huckel分子轨道(HMO)理论。虽然他从来没有明确制定一个“4 n + 2规则”,这是明显的从他的工作。Huckel表明单环系统连续接合有6、10、14等p电子受益于额外的稳定和芳香。但它是更准确的指“Huckel 4 n + 2 p,电子规则,”而不是“休克尔规则”。 - 今天芳香性:精力充沛和结构标准
米哈伊尔·Glukhovtsev
《化学教育1997年,74年(1),132
DOI:1021 / ed074p132
本文讨论的两个标准建立芳香性——平面化和积极稳定的能源。后者可以通过计算方法验证,如本文所示。 - 在纳米尺度上全球芳香性
Rickhaus, M。,Jirasek, M., Tejerina, L. et al.
化学性质。12236 - 241 (2020年)
DOI:10.1038 / s41557 - 019 - 0398 - 3
这篇论文发表在2020年初正式设置记录最大的芳香体系,与162 p电子!芳香性的证据来自于两个核磁共振测量和实验(nic)计算。 - Nucleus-Independent化学变化:一个简单而有效的芳香性调查
保罗·冯·Rague Schleyer Christoph Maerker, alaska airlines Dransfeld, Haijun娇,尼古拉斯·j·r·范Eikema Hommes
美国化学学会杂志》上1996年,118年(26),6317 - 6318
DOI:10.1021 / ja960582d
本文是一个高级主题但价值包括在这里,因为它是Schleyer教授最高度引用的论文。芳香性是一个很难准确定义的概念,但实际测量的一种方法是使用计算方法。这里,Schleyer教授描述了“网卡效应”的方法测量芳香性,基于磁化率提高。芳香族化合物有一个“环电流”的结合p轨道和电子离域p的存在,因此抗磁性。这个可以测量实验或调查计算。 - Cyclodecapentaene系统
e·沃格尔博士,该化学。h·d·罗斯
Angew。化学。Int。。1964年,3(3),228 - 229
DOI:10.1002 / anie.196402282 - Perspektiven der Cycloheptatrien-Norcaradien-Valenztautomerie
伊曼纽尔沃格尔
纯粹的达成。化学。1969年,20.(3),237 - 262
DOI:10.1351 / pac196920030237
上述两篇论文的合成和表征cyclodeca-1, 3, 5, 7, 9-pentaene。NMR光谱显示出抗磁性环电流的类型将在一个芳香体系。 - 合成1,6-didehydro[10]轮烯。观察它的异常灵巧的重排形成双游离基1,5-dehydronaphthalene
安德鲁·g·迈尔斯和纳撒尼尔·s·芬尼
美国化学学会杂志》上1992年,114年(27),10986 - 10987
DOI:10.1021 / ja00053a059
迈尔斯(现在哈佛大学)开始他的职业生涯作为一个加州理工学院的教授和他的早期论文的宝石在物理有机化学。这个也不例外,简洁的沟通掩盖这个实验工作的极端困难,在合成和表征。复合分子内使环化萘通过低温双自由基中间体,现在这种类型的反应称为“迈尔斯环合”迈尔斯教授。 - HOMO-AROMATIC结构
美国Winstein
美国化学学会杂志》上1959年,81年(24),6524 - 6525
DOI:10.1021 / ja01533a052
“homoaromaticity”这个词在本文首次引入化学,有机化学家扫罗教授Winstein(加州大学洛杉矶分校)。今天,前缀的homo -化学常用来表示扩展1亚甲基(ch2-)组。 - 不饱和的大环化合物。XV.1 CYCLOTETRADECAHEPTAENE
弗朗茨·桑德海姆和Yehiel Gaoni
美国化学学会杂志》上1960年,82年(21),5765 - 5766
DOI:10.1021 / ja01506a061
[14]轮烯合成但发现不稳定,尽管它有14个p电子按照Huckel 4 n + 2 p电子规则。这是因为它不能实现平面性,从而证明平面性是一个重要的标准实现芳香稳定! - 的结构和热化学[18]轮烯
杰罗姆·m·舒尔曼和雷蒙德- Disch
《分子结构:THEOCHEM1991年,234年,213 - 225
DOI:10.1016 / 0166 - 1280 (91)89014 - r
[18]轮烯足够大以减少空间之间的相互作用的内部氢的几何角应变。的性质[18]轮烯符合它的芳香。 - 从头开始密度Funtional vs哈特里福克预测[18]轮烯的结构:证据债券本地化和减少环电流Bicycloannelated[18]轮烯
金正日k Baldridge教授杰伊·s·西格尔
Angew。化学。Int。。1997年,36(7),745 - 748
DOI:10.1002 / anie.199707451
稳定能源18千卡每摩尔已经计算了[18]轮烯。
谢谢你的澄清詹姆斯reg。在吡咯C2更亲核。
想这需要一个小校正你的一个回答,也许早些时候对整个文本部分太. .:)
吡咯发生亲电取代C2(或C5)而不是C3 (C4)。这并不意味着C2 (C5)亲核比C3 (C4) ?替换在C3往往只发生如果C2 (C5)已经取代。
是的。碳原子相邻的氮吡咯更亲核。
文章几乎一切完全交付。
拥有一切;-)
请告诉为什么cyclo-pentadiene阴离子芳香吗? ? ? ?
想想芳香性的规则和工作。它是循环吗?共轭以外的戒指吗?它有多少个π电子?
谢谢你詹姆斯尽管有点奇怪整个分子不遵循huckel规则,每个原子都是共轭
一个环芳香族和其他显然不是。把它看作一个取代苯衍生物。
是1,4 dihydronapthalene芳香?
是的,苯环部分芳香!
如果有一个系统的2稠环完全共轭但另一个sp3碳,所以将结构被认为是芳香的,因为一个芳香环?
是的。你给1的具体例子,4-dihydronaphthalene是有用的!
非常感谢詹姆斯
我们应该为个人环每次计算它的孤立系统? ?
是的,每个孤立系统计算它。
bi苯呢,我们怎么能说它芳香吗? ? ? ?
看看每个单独的两个戒指。戒指都是芳香。
你好,詹姆斯,
请你告诉我,“- 1,3二烯芳吗? ? ?
不,绝对不是。
你好,
如果这样呋喃孤对电子的吗?
芳香性会有任何改变吗?
https://hizliresim.com/6CuBRw
谢谢你!
虽然显示了呋喃孤对每一方,这是更多的交流这一事实呋喃有两个孤对,而不是传达的准确描述其孤在空间。呋喃氧气将sp2。在p轨道的孤对电子,与另一个p轨道的π体系。另一个孤对将在同一个平面上的分子碳氢键。
你好,
为环戊二烯基负碳离子,评论rehybridization sp3(典型的负碳离子物种)sp2从共振稳定得到一些好处,因为它与其他sp2杂化碳原子应该给。
伟大的工作!
好建议。谢谢鲁本!
很好的帖子,很容易理解,清晰和简单。我不能赞美只是一个词
很高兴你有帮助Sendhan !
那么,富烯anti-aromatic还是non-aromatic ?我orgo教授说这是non-aromatic,但我看不出为什么。是因为ch2外环上的p轨道没有好的重叠与内部的碳环吗?
非芳香。这是稳定和可隔离的。如果是antiaromatic不会可隔离的。p轨道的ch2外环不是循环的p轨道的一部分。将会有一个非常重要的共振形成的富烯,“精彩”π键极化,环的p轨道有两个电子和p轨道外环为零(换句话说,CH2外环的碳正离子和碳它连着负碳离子)。但是这并不足以使它真正的芳香。
为什么室内sp3杂化碳原子的分子列为10π电子而不是14 ?
你是对的。固定!
你好詹姆斯,好的文章!然而,我认为奇怪的芳香性的分子有14个π电子(如有7个π键),不仅10 ?
谢谢你戴夫!固定
如果你有一个三角形的碳结构,一个孤对,没有双键;这还算是芳香由于共振吗?或nonaromatic因为你以前sp3共振?明天我有一个考试,我感到很困惑
你听起来就像你描述环丙烷的共轭碱。这不是芳因为有sp3杂化碳原子。
为[10]轮烯的例子:它的异构体,CH2,你说它允许它是芳香的,因为它允许平面。然而,不是CH2 sp3杂化?不会违反接合和空的p轨道规则吗?谢谢你!
这是一个特例,因为分子的几何- ch2高于飞机π键在哪里;π键是平面
嘿,詹姆斯,我不明白。苯离子:LP的碳在p轨道1个电子之前得到一个负电荷,然后,你认为这是p,电子仍然完好无损,但*有孤对*在新占领的轨道?这是不对的,是吗?它可以被一个单一的电子在新占领的轨道或其p轨道电子吸引到新的。
孤对来自碳氢键,在p轨道直角
自从4 n + 2 UG学生造成很大痛苦,我倾向于使用奇数的π电子对…。
苯碳正离子是芳香族或非芳香和为什么
里面是空的p轨道pi-system苯基碳正离子的关系?这才是你的答案。
冠醚十氢化萘没有提到
它与芳香性无关!
从巴西的问候!
本文就足以清楚我的怀疑。非常感谢。:-)
一个药房的学生。
太好了,很高兴听到它Matheus !
你也能解释anti-aromatic化合物呢?
在这里://m.dermacare3d.com/2017/03/27/antiaromaticity/
哇!希望我有看到这篇文章前6个月_ -迟到总比不到好:)也在吡咯的情况下,我有一个查询(可能是无关紧要的虽然在这里发布)。在吡咯的远端和近端碳(关于N)更多的电子密集的吗?也有文章,你在“反aromacity”?找不到这里。再次感谢,你是我的O-chem last-minute-saviour。
文章anti-aromaticity://m.dermacare3d.com/2017/03/27/antiaromaticity/
吡咯、颈- 3更亲核。好考试问题的方式,看你能不能找出原因比c - 2亲核的供给。
我很高兴,但有些惊讶,你没有提到homoaromaticity。大能的蠕虫。你故意标记为“愤怒”的规则吗?
Homoaromaticity是值得一个脚注的事情,因为它很有趣,但可能不是普通读者所必需的。谢谢你的建议关于“愤怒规则”:-)