胺
还原胺化反应
最后更新:2022年9月21日|
做替换胺通过还原胺化作用
- 直接烷基化胺与烷基卤化物是一个难以控制的反应。
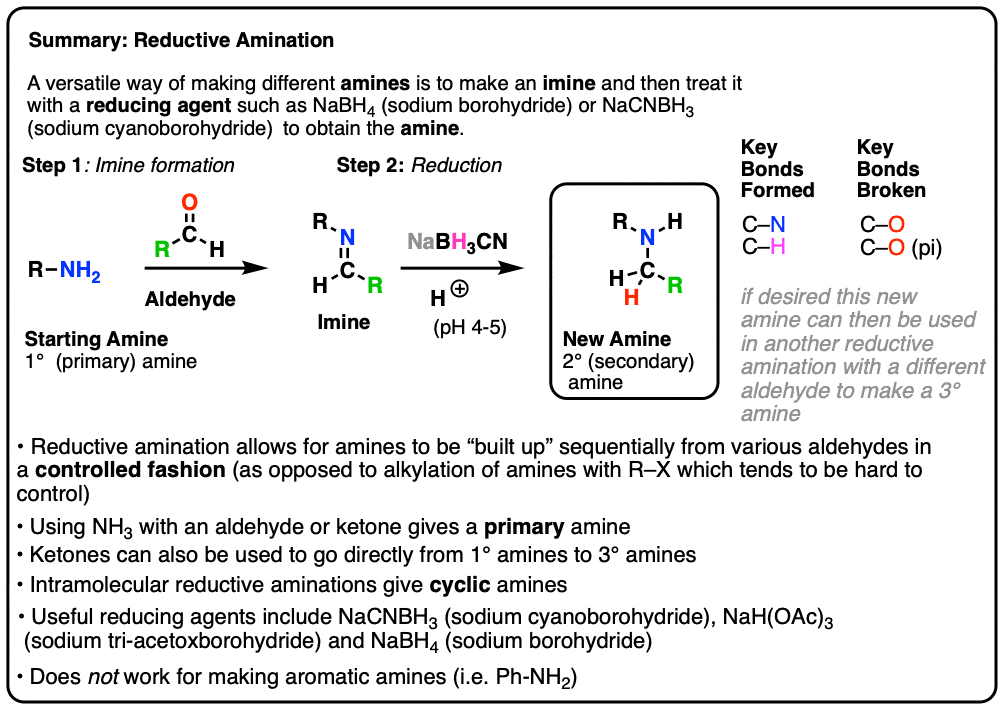
- 另一个选择是形式非常好亚胺一个胺用一个合适的醛或酮,然后减少的亚胺胺。这就是所谓的还原胺化反应并避免多个烷基化的问题。
- 一个常见的还原剂这个目的是cyanoborohydride钠(NaBH3CN),可以选择性地降低亚胺醛的存在。许多其他的减少代理(NaBH4,NaBH(OAc)3可以使用等)。
- 可以从小学开始胺连续做两还原胺化作用,获得第三胺。
- 不工作形成债券从氮还原胺化芳香环。
表的内容
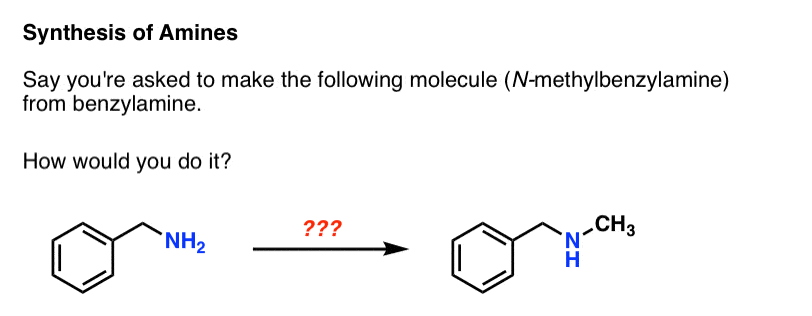
1。我们如何使这胺,如果直接烷基化不工作吗?
说你有一个主胺如苄胺和愿N-methylbenzylamine。你怎么做?
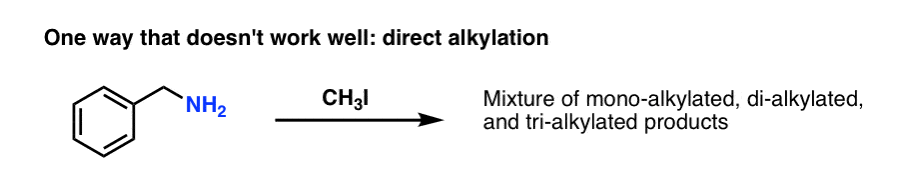
苄胺的直接治疗与烷化剂(如碘甲烷、CH3我)将导致不良的重要形成三级胺(即。迪烷基化)。
是的,你可以试试,把次要的胺这是由三级胺,但我们不会满足于10 - 30%的收益率。分离混合物在纸上是好的,但是(相信我)它可以在实践中真正的痛。有另一种方式去做吗?
2。还原胺化作用的救援
进入还原胺化作用!
虽然多次在一个会发生烷基化胺,亚胺只在一个给定的形式一次胺。一旦形成亚胺,C = N键可以减少,给我们一个新的烷基集团在氮。
这是一个更形成氮碳键的控制方式。
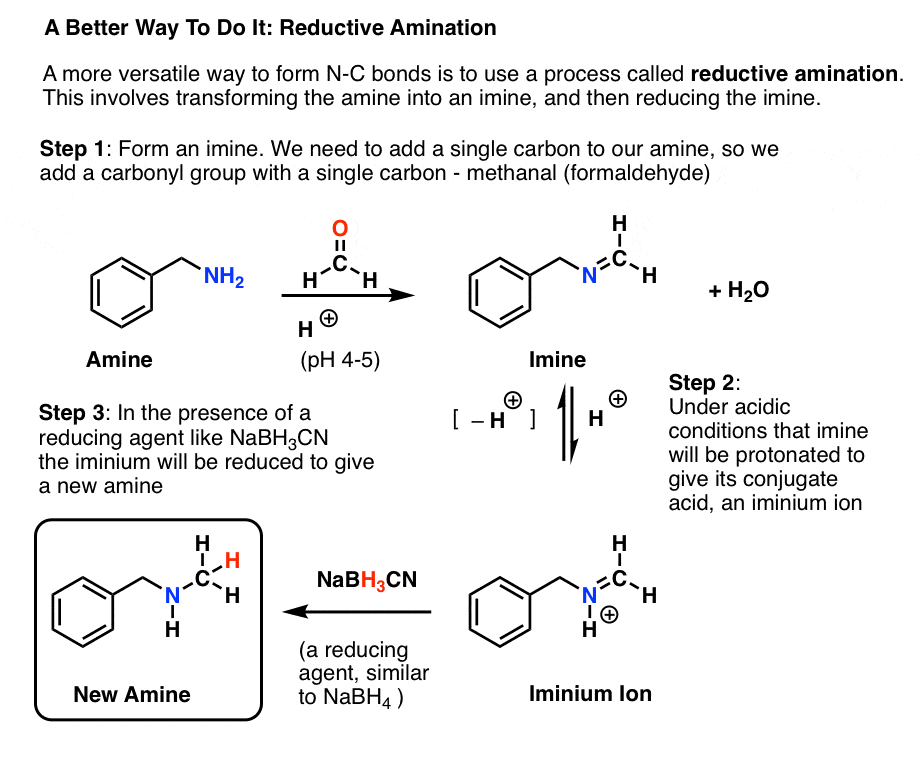
我们覆盖了亚胺形成之前(见文章:亚胺-属性、反应机制)。刷新自己的机制,徘徊在这里和一个图像会弹出(链接)。
亚胺形成之后,它必须减少胺。可以使用熟悉的还原剂硼氢化钠(NaBH4)这个过程。您可能还记得,NaBH4用于醛和酮的还原。
还有两个常用的还原剂还原胺:钠cyanoborohydride (NaBH3CN)和钠tri-acetoxyborohydride (NaBH(OAc)3)。就我们的目的而言,他们可以被认为是相同的。在实践中,NaBH3CN有点比NaBH4。
(讨论的原因NaBH3CN是一个更好的选择比NaBH4,请参阅注2。在下面的方案中,我们将使用NaBH3CN,但NaBH4和NaBH(OAc)3可以考虑工作。]
3所示。应用还原胺化作用
还原胺化作用是极其多才多艺的,可以用来安装各种各样的不同烷基组一个胺。最妙的是组只进行一次。
下面的表显示了甲基的例子,乙,丙,丁,苄可以安装在一个组胺,通过使用一个适当的醛。(注意,不还原胺为安装工作苯基组。为什么不呢?注1。]
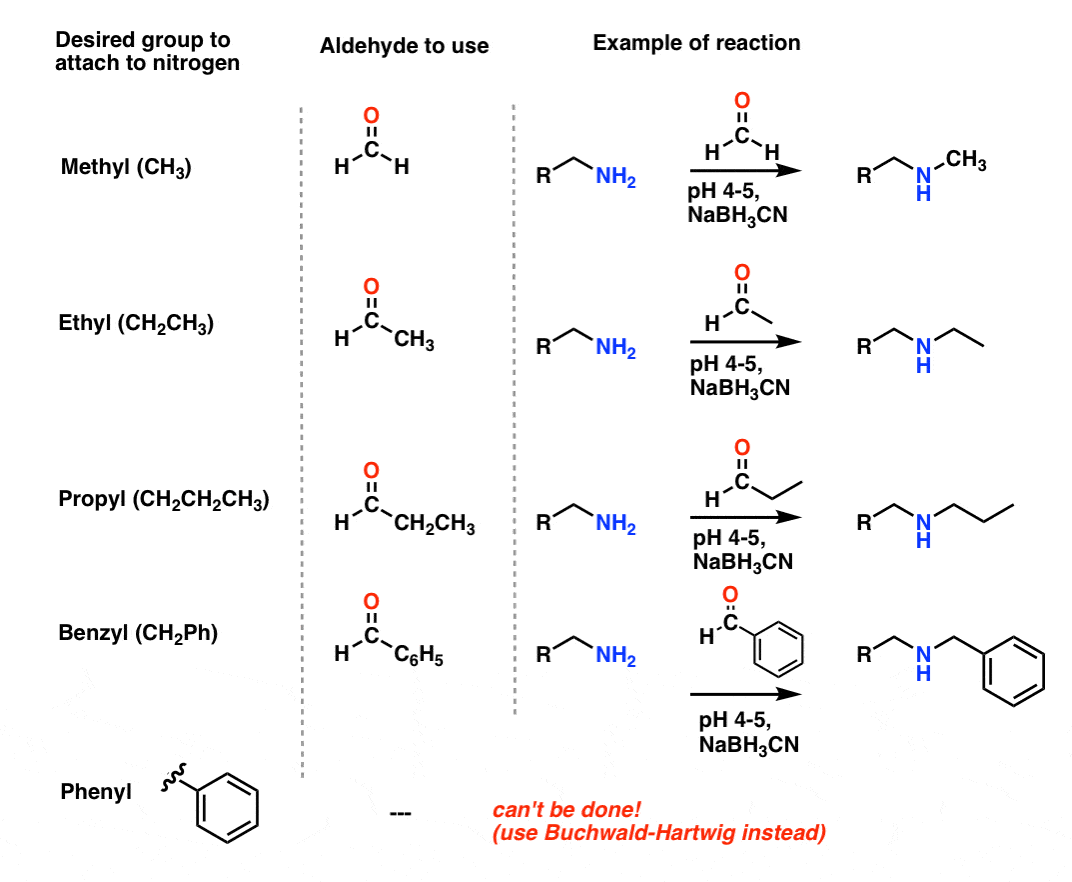
4所示。酮也工作
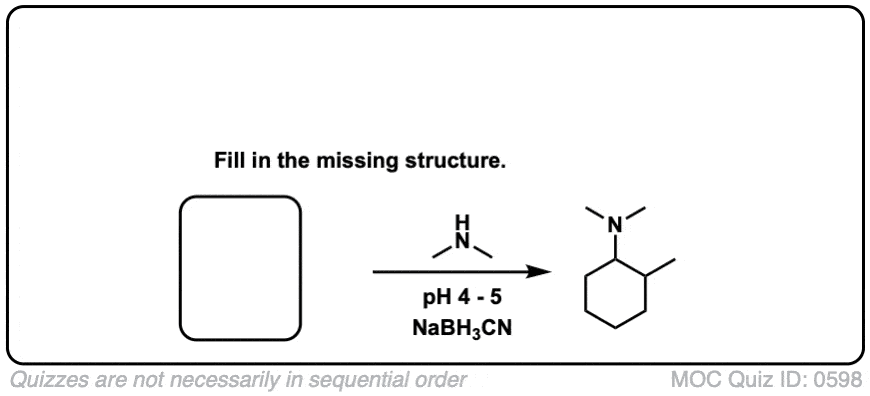
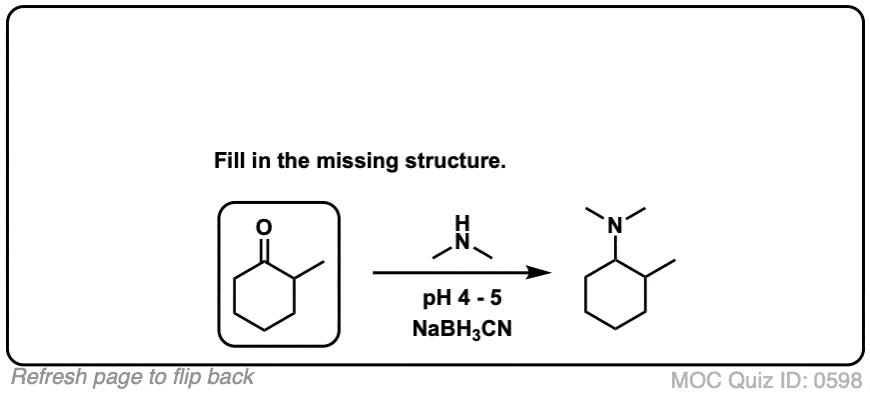
酮呢?他们的工作!雇佣一个酮会导致支吗烷基取代基的胺。例如,使用丙酮下面给出一个还原胺化异丙基组。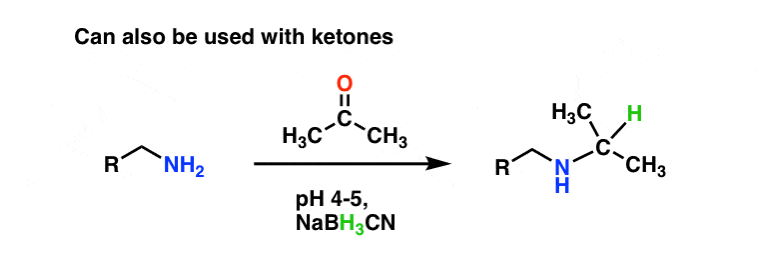
5。顺序还原胺化作用
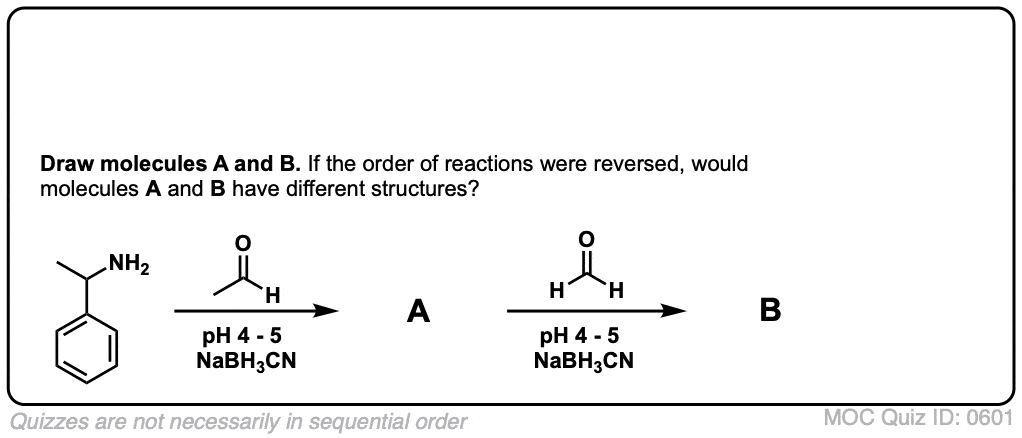
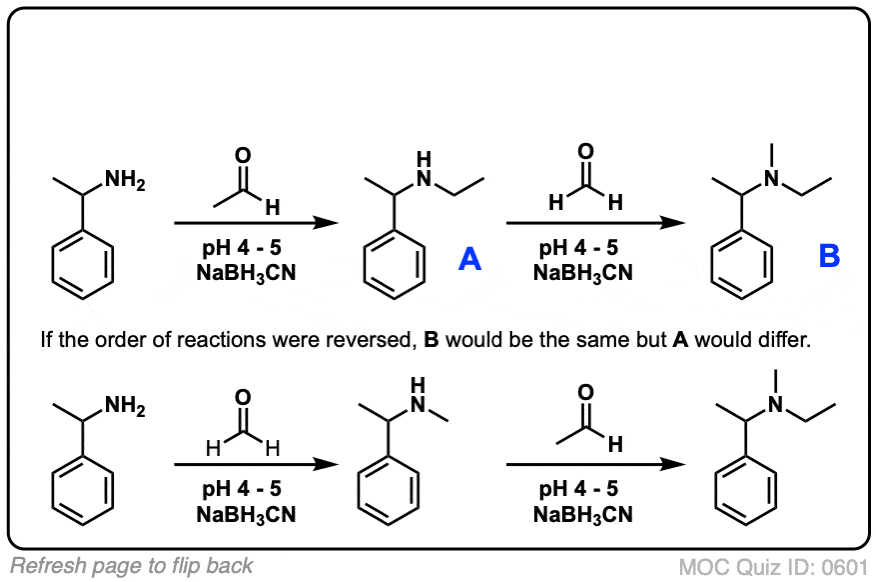
还原胺化反应的另一个有用的功能是两个(或三个如果一开始氨)还原胺化作用可以使用序列。例如,看叔的合成胺在下面。
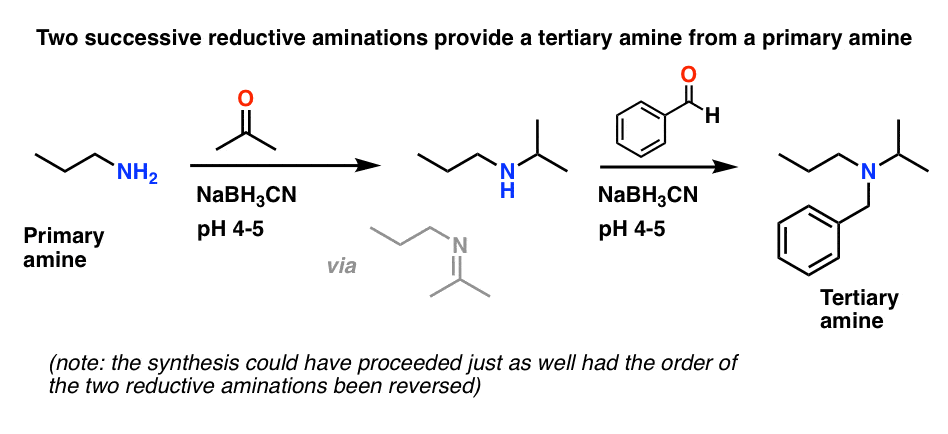
重要的是,反应的顺序并不重要。我们可以做第一个先用苯甲醛还原胺化,和丙酮其次,仍然得到相同的产品。
6。分子内还原胺化作用
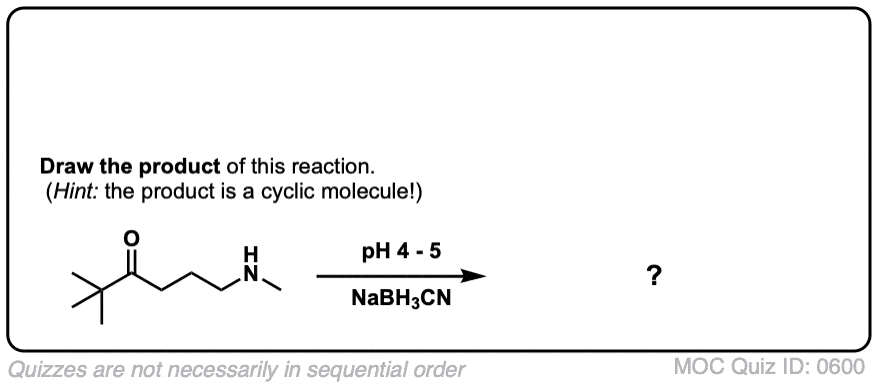
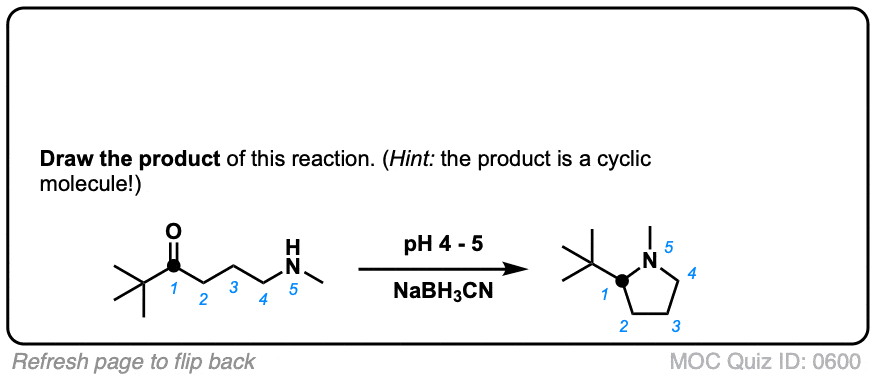
最后,有分子内的情况下,它似乎总是给学生一个头痛。如果一个分子包含一个胺和一个羰基,那么它可以使环化循环胺。
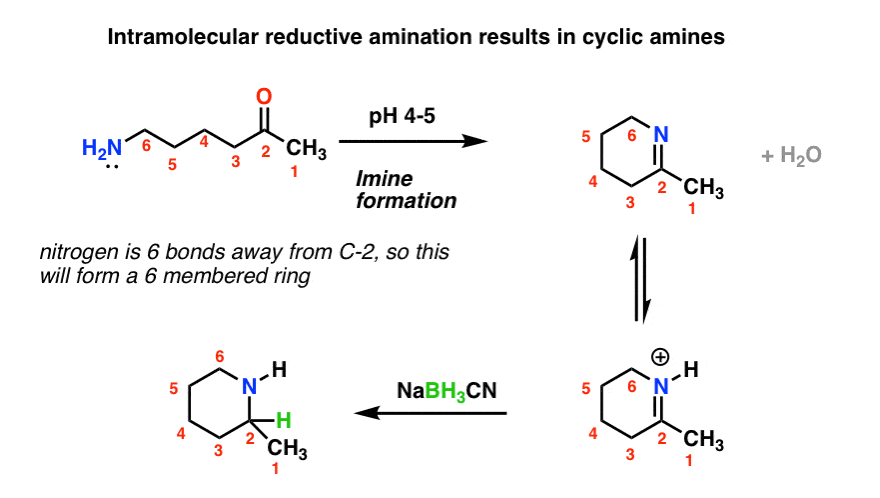
当画成环的产物,我强烈建议你碳数和编号。我看过那么多学生犯错误当重新划定值得仔细检查的时候,你没有留下任何东西。
7所示。向后的工作:规划一个还原胺化作用
它可能需要一些时间来欣赏,但是是一个极其强大的还原胺化的方法胺。
这是非常有用的能够认为从一个胺产品的起始原料是什么样子的。
看看以下三级胺。它连接到三个碳,我们可以标签,b和c。每一个c债券可能通过还原胺化作用形成的,因为他们有碳氢键。
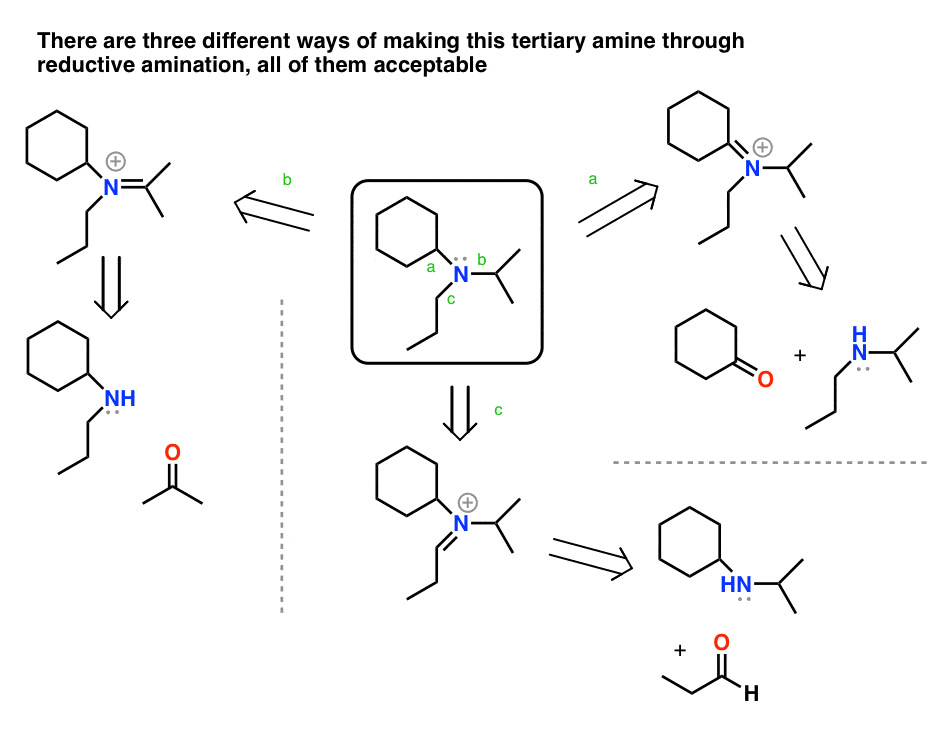
这意味着有三种可能的方法的胺通过还原胺化作用,都可以接受!
简而言之,是一个非常强大的和有用的协议还原胺化的形成胺。
笔记
注1。安装一个呢苯基组(见上图)?氮与sp之间形成的债券2杂化碳原子(如。烯烃或苯基组)之间或氮和sp-hybridized碳(如。炔烃),不会还原胺化工作。
想想。注意,碳与氮没有碳氢键。因此我们不能工作向后氢化还原C = N键的来源。

一个人必须诉诸替代技术。Buchwald-Hartwig交叉耦合就是其中之一。
这种试剂,有一个轻微的问题。如果NaBH4最终减少了醛或酮才有机会与亚胺反应吗?这将导致更低的收益率。(实际上,这可以减少给亚胺足够的时间形成,然后加入NaBH4。]
一个更好的方法是使用略弱还原剂钠cyanoborohydride (NaBH3CN)。
为什么要使用较弱的还原剂吗?
回想一下,形成亚胺的最好在温和的酸性条件下完成(pH值4或5)。在温和的酸性pH值,羰基氧气是质子化了的,加速的羰基碳;如果解决方案太然而,酸性胺亲核试剂将被转换成(non-nucleophilic)共轭酸,一个铵盐,没有反应就会发生。)
一旦亚胺形式在pH值4 - 5,它将被转换成它共轭酸,一个iminium盐。
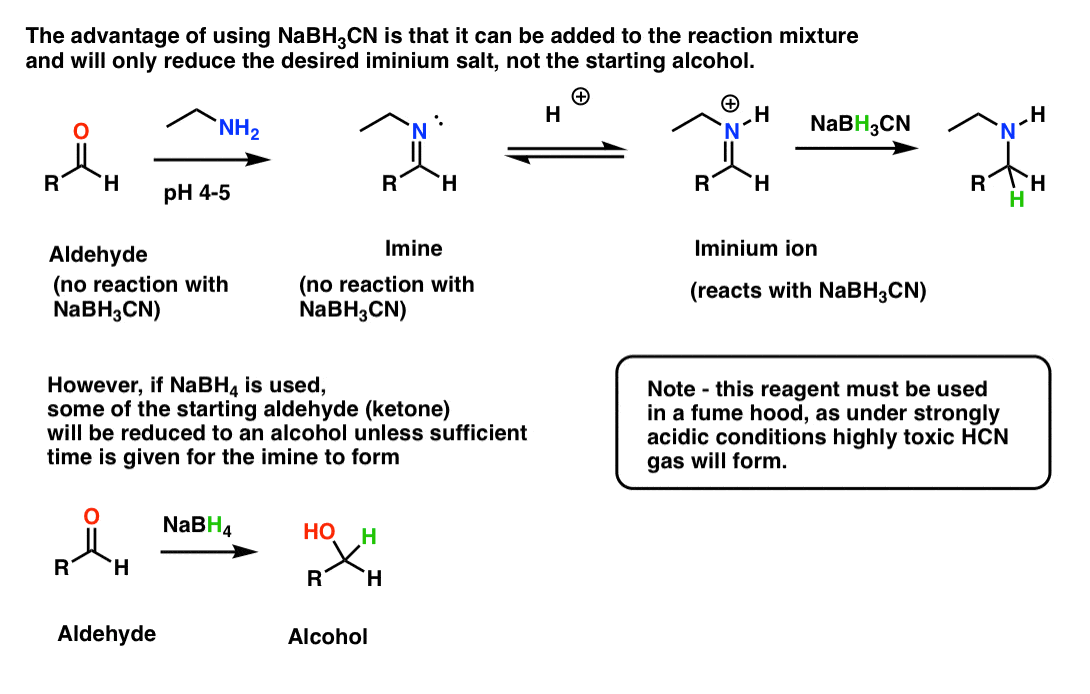
使用的优势NaBH3CN是它不够强大还原剂减少醛或酮,但它是一个足够强大亲核试剂减少iminium离子。因此更多的开始醛/酮将转换成吗胺。(这是特别重要的在处理非常珍贵的样本醛]。
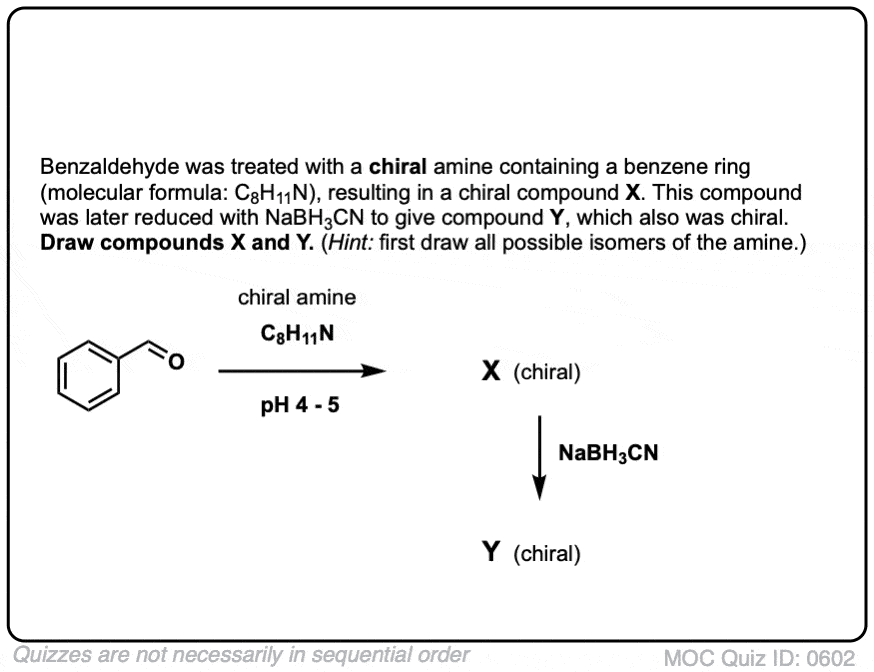
测试你自己!
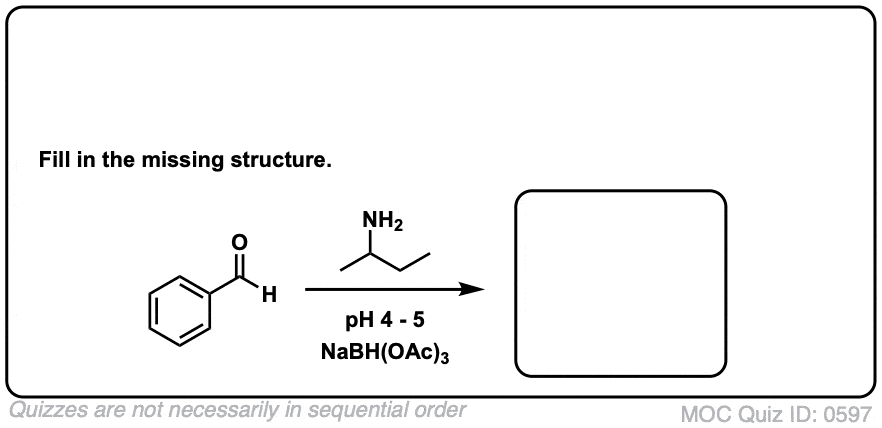 点击翻转
点击翻转
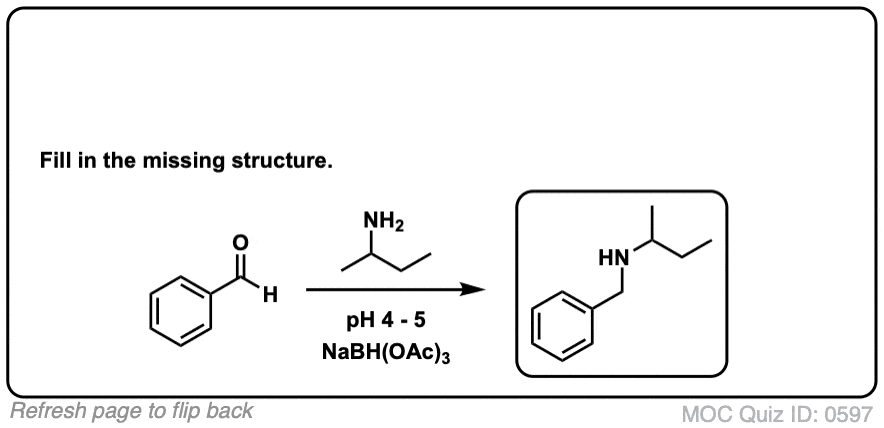
 点击翻转
点击翻转
 点击翻转
点击翻转
 点击翻转
点击翻转
 点击翻转
点击翻转
 点击翻转
点击翻转
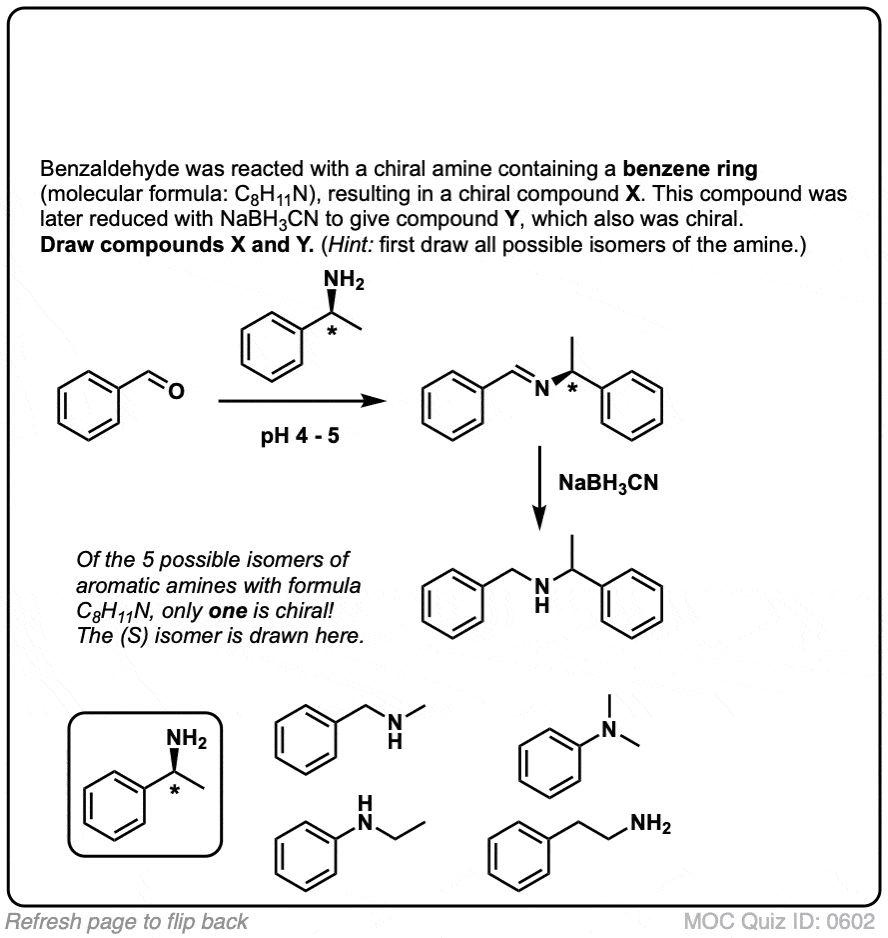
(高级)引用和进一步阅读
- Cyanohydridoborate阴离子选择性还原剂
理查德·f·Borch马克·d·伯恩斯坦,h·杜邦杜斯特
美国化学学会杂志》上1971年,93年(12),2897 - 2904
DOI:1021 / ja00741a013
第一个报告的使用NaBH3CN是一个还原剂还原胺化作用。 - 还原烷基化的一种改进方法胺使用钛(四)异丙醇盐和钠cyanoborohydride
罗纳德•j•马特森Kahnie m·范教授David j . Leuck和肯尼斯·a·考恩
《有机化学》杂志上1990年,55(8),2552 - 2554
DOI:1021 / jo00295a060
Ti (OiPr)4可以用来作为路易斯酸激活吗酮/醛对添加的胺以及由此产生的亚胺可以减少原位通过NaBH3CN,还原胺化作用。 - 醛和酮的还原胺化钠Triacetoxyborohydride。研究直接和间接还原胺化作用过程
艾哈迈德·f·Abdel-Magid肯尼斯·g·卡森,辛西娅·a·Maryanoff布鲁斯·d·哈里斯和瑞卡·d·沙阿
《有机化学》杂志上1996年,61年(11),3849 - 3862
DOI:1021 / jo960057x
NaBH(OAc)3也可以用作吗还原剂在还原胺替代程序NaBH3CN,如果担心氰根离子浓度的产品或废物流。 - 开发生产的可伸缩的路线独联体- n -苄3-methylamino-4-methylpiperidine
大卫·h·布朗是Stefan银白杨weil Cai,托德Blumenkopf,杰弗里·m·Casavant乔纳森•l . Doty马克·弗拉纳根基督教Koecher,克劳斯·w·劳厄基思•麦卡锡悬崖Meltz, Mike Munchhoff Kees Pouwer,巴拉特·沙阿健民太阳、约翰•特谢拉吨弗里斯,大卫·a·惠普尔和格伦·威尔科克斯
研发的有机过程2003年,7(1),115 - 120
DOI:1021 / op025599x
OPRD是一个伟大的来源可靠的程序,因为反应扩大需要健壮的、高收益,不需要外来的溶剂或superstoichiometric大量过于昂贵的试剂,并有简单的净化程序(避免色谱在可能的情况下)。 - 锅共轭醛和酮的还原胺化硅胶和硼氢化锌
Brindaban c . Ranu Adinath Majee, Arunkanti Sarkar
《有机化学》杂志上1998年,63年(2),370 - 373
DOI:1021 / jo971117h
锌(黑洞4)2也可以用作吗还原剂还原胺化作用。 - 单一Stereodifferentiation与碳原子插入在钖Ion-Initiated Dihydrofuranyl频哪醇重排和Dihydropyranyl甲醇
狮子座a . Paquette詹姆斯·c·兰特和杰弗里·n·约翰斯顿
《有机化学》杂志上1997年62年(6),1702 - 1712
DOI:1021 / jo962019j
狮子座Paquette教授表明stereodifferentiation pinacol-type重组是可能的。 - α-PHENYLETHYLAMINE
约翰·c·罗宾逊,jr .)和h·r·斯奈德
Synth。1943年,23,68年
DOI:10.15227 / orgsyn.023.0068
一个使用NH还原胺化作用3随着胺。 - 25周年Buchwald-Hartwig氨基化:开发、应用和前景
Paola a Forero-Cortes和亚历山大•m . Haydl
研发的有机过程2019年,23(8),1478 - 1483
DOI:10.1021 / acs.oprd.9b00161
的简短回顾Buchwald-Hartwig氨基化,发展,应用程序和未来前景。OPRD(连同有机合成)是一个好地方去寻找可靠和健壮的反应,这就是最有价值的化学过程,在开发大规模的反应。
感谢您使有机化学的和可以理解的,你的工作是令人印象深刻。
只是一个问题:在羰基存在alpha-H伙伴,并通过烯胺中间体的反应还是最喜欢的互变异构化iminium离子总是吗?在第一种情况下,仍然是NaBH3CN最好的还原剂或类似的?
它可以形成烯胺,但在酸的存在,会有烯胺和iminium之间的平衡。只要iminium形成减少可能发生的。
我认为这更有意义,酸”能迅速使质子化后的氧气之外. .“提前而不是使质子化羰基。但是,为什么会出现这样的机制在很多文本吗?当然,作者知道羰基氧的激烈的pKa差异和胺(这是一个基地!)。我想知道在某些溶剂羰基实际上是优先质子化了的?我用二氯甲烷作为溶剂的反应和效果的两倍小醋酸。在任何情况下,反应机制往往是好的猜测有很多矛盾如果太仔细的检查。
谢谢你!我在注意这一步的研究和正确的。
嗨,漂亮的帖子。我想评论一个常见的误解你。从上图:
“记得,形成亚胺的最好在温和的酸性条件下完成(pH值4或5)。(在温和的酸性pH值,氧羰基质子化了的,加速的速度除了羰基碳;然而,如果溶液酸性胺亲核试剂将被转换成其(non-nucleophilic)共轭酸、铵盐,没有反应就会发生。”
使质子化的pka胺是9 - 12,而的pka羰基质子化了的是6或在那附近。因此在弱酸性溶液羰基不会明显的胺相比,质子化了的。这种机制的第一步是胺羰基。轻微的酸度可以迅速使质子化后氧胺和促进质子转移的除了水的去除。至少我就是这样理解它。这是一段时间以来phy org。大多数文本得到这个错误的。
我爱你的引用,为教师和学生很棒的资源!
欢呼,
低潮
感谢,我将其添加到我的修正队列!虽然我可能是错误的,我看到pKa的羰基质子化了的在2左右。不过,大约15数量级的遍历,所以在这一点上你是正确的。
伟大的文章。
是来有一些参考。我是NaBH3CN部分特别感兴趣。
谢谢你!
我将查百科全书的有机合成试剂。我看到的是Borch原始的参考。R f等人,江淮,1971,93,2897。https://pubs.acs.org/doi/10.1021/ja00741a013
没有部分的语句顺序还原胺化作用”与“虽然胺烷基化可能发生多次,在给定的胺亚胺只形成一次”吗?
啊。是的,我看到你的问题的来源。也许我应该写,“在同一反应容器”。
烷基化反应过程中,胺烷基化,然后再可以烷基化产品。所以,当你去做一个隔离产品,你会发现多个发生烷基化。
亚胺还原胺化作用,只会形成一次同样的反应容器,一旦他们减少,反应结束。只有一个新的碳氮键将形成。
现在,一旦你孤立和净化产品,如果是一级或二级胺没有什么阻止你做*第二*不同醛还原胺化。
这说得通吗?
我知道,通常情况下,必须使用过量的胺,同时进行还原胺化作用。这是增加产量的亚胺吗?
如果是的,那么将使用过量的醛/酮还工作吗?
嘿布兰妮——你想使用过剩确保胺有机会和所有的醛/酮反应,再氢化物源。一旦氢化物源添加任何醛/酮仍将减少酒精呈现这无用的过程。
可以啦减少胺亚胺?
“应用”还原胺化,下表中所示的苯甲醛有一个额外的CH2醛使用。
谢谢你!将修复。
我有一个问题。
如何解释difffent反应的亚胺(iminium离子)之间与NaBH3CN羰基(质子化了的)?
亲电试剂是碳,对吗?和部分正电荷越多,碳,更好的一个亲电试剂,对吗?现在画的共振形成亚胺,你移动的电子氮氮π键。接下来,画出共轭酸(iminium)和做同样的事情。共振形成两者之间你觉得会更稳定?这才是你的答案。
底线,质子化作用的氮导致共振形成的更大的贡献有一个正电荷的碳,这是更多的亲电。
还原胺化作用凝聚和彻底的解释。谢谢!
很高兴对你有用乔希,干杯!
我们感兴趣的二次还原胺化脂肪胺与甲醛dialkylmethylamines氢分压下,而不是固体还原剂。
也感兴趣的是直接转换的主要脂肪腈dimethylalkylamines DMA。这似乎是很好的描述可用的文学。
在工业规模、转换和收益率高于95%是很重要的。
喜欢你的帖子!
好的文章!错误:还原维护- >还原胺化作用
谢谢你!该死的自动更正。