碳水化合物
为糖D和L符号
最后更新:2022年9月18日|
D, L -符号的绝对构型糖和氨基酸
D -和L -经常发现面前的糖和氨基酸的名字。他们是什么意思?
- D - L -是一种描述方式绝对构型刷新的分子((R, S))CIP系统。
- D, l是一个古老但still-convenient简称说分子对映体。如葡萄糖和L-glucose重叠镜像,而不必编写出一个长国际命名的(R)和(年代)描述符。
- 最自然的糖是D -和最自然的L -氨基酸。
- 判断一个分子的一个方法是D -或L -通过观察分子的费舍尔投影。如果(nh -哦2在最底层的手性氨基酸)的中心右边费舍尔的投影,这种分子是“D”。如果是左边,分子“L”。
表的内容
- D, L -提供了一个快速简称指定对映体
- 我们为什么要把这个古老的命名?
- L - D -系统分配“绝对配置”
- 四碳醛D, L -糖(Aldotetroses)
- 五碳醛D, L -糖(戊醛糖)
- 六元醛D, L -糖(己醛醣)
- 但是等等——还有更多!(氨基酸)
- 摘要:D -和糖类和氨基酸L -符号
- 笔记
- (高级)引用和进一步阅读
1。D, L -提供了一个快速简称指定对映体
D, L -符号提供了一种快速简称指定对映体。
葡萄糖是对映体L-Glucose,例如。丙氨酸是D-Alanine的对映体。
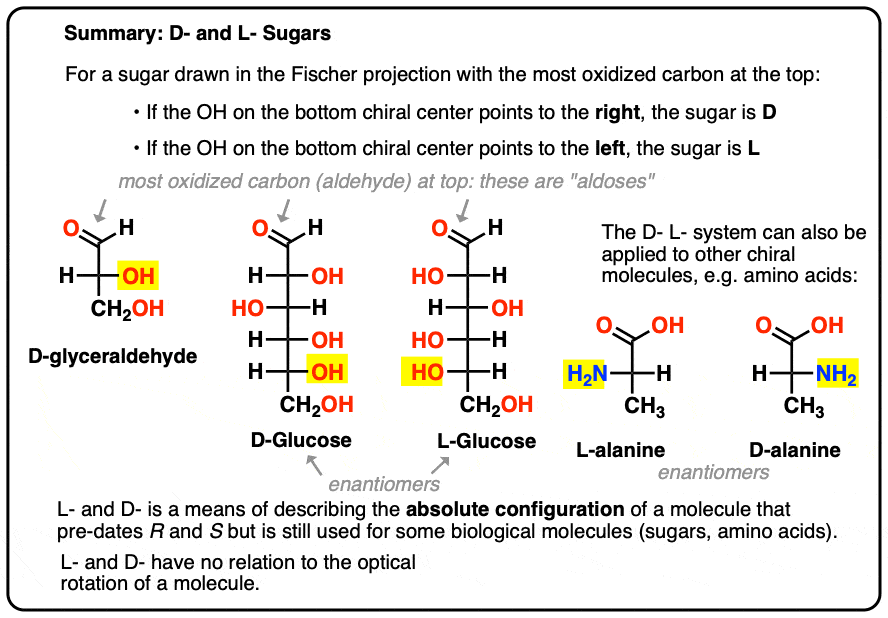
- 如果哦手性中心指向正确的底部,它被称为D -
- 如果哦底部指向左边的手性中心,它被称为L -。
这个术语也适用于氨基酸:见上图中的L -、D -丙氨酸。
2。我们为什么要把这个古老的命名?
你可能理由问:我们不已经有一个系统来分配绝对构型((即命名规则。R和年代)]?为什么我们需要一个新的系统?
D-L系统并不是一个新系统,伙计。这是一个旧系统——它早于命名。
D-L系统实际上是一个马车时代的遗迹,可以追溯到埃米尔费舍尔在碳水化合物的工作在1800年代末,当有机化学家没有办法确定绝对构型立体的,只在1951年成为可能(谢谢,毕吉博)。
那么为什么还习惯吗?不应该被扔进历史的垃圾箱里,连同计算尺,音乐专辑磁带5¼”软盘吗?
有繁荣的社区在美国农村地区马车坚持——如果你知道去哪里看。(也许有一天会有公社,人们只使用1970年代和1980年代计算机技术?)
同样有一个口袋的有机化学D-L系统还发现使用专门的领域糖和氨基酸。
这不是一个反抗阿米什化学家对现代CIP系统的罪恶,。至少有3个理由,糖和氨基酸的具体案例,利用L - D -:
- 简洁。葡萄糖是一种更快的写和说比(2 r, 3 s 4 r 5 r)2、3、4、5、6-pentahydroxyhexanal。L / D -系统允许的配置一个分子与多个手性中心总结了一个字母(当然,加上它普通的名字,谢谢诺埃尔提醒)
- 更简洁。它指的是一个快速的方法对映体。的对映体L-glucose是葡萄糖。色氨酸是D-tryptophan的对映体。虽然我们可以用(+)-(-)-前缀来区分这两个概念对映体葡萄糖等糖类,旋光性的符号可以随溶剂、温度、浓度等因素使它并不理想。另外,L - D -特别提到绝对构型,而(如前面我们提到的)没有简单的旋光性的符号之间的关系和配置。
- 事实证明,大多数天然糖D -,和大多数天然氨基酸L -。有一个巨大的信息压缩在声明中没有竞争系统(R / S + / -)可以取代L - D -和一个字符。注1
值得重复的是:糖和氨基酸、L -和D -名称是非常有用的。对于其他分子,可以很大程度上忘掉它。[(一些可怜的人分配自然发生的吗啡D -。给我R和S名称。)
那么是这D / L -系统,这些条件与结构如何?
和我一起当我们通过时间旅行…
3所示。L - D -系统分配“绝对配置”
埃米尔费舍尔开始研究碳水化合物在1880年代末。是被时间(通过范托夫)碳四面体,也知道分子含有一个碳有四个不同的取代基可以旋转平面偏振的光(如。巴斯德)。什么不是是已知的绝对构型的手性分子——我们称今天为“R”和“年代“配置。
最简单的碳水化合物[Cn(H2O)n甘油醛)含有一个手性中心,C3H6O3。甘油醛3个碳;使它成为“丙糖”。甘油醛是一种最氧化碳醛,这也使其成为“醛糖”。(这些术语往往结合:“奥尔多三大阪证交所”是指一个3碳糖含醛。]
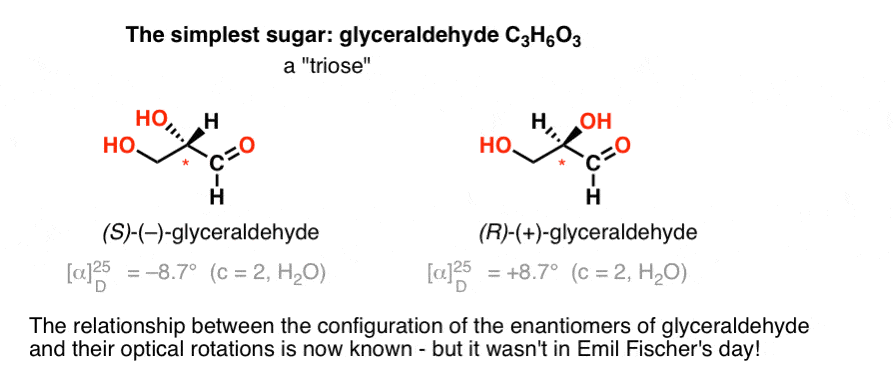
1888年,两个对映体的甘油醛((+)和(-))被孤立和特征。但由于没有之间的简单相关的配置一个手性中心和旋转平面偏振光线的方向,埃米尔费舍尔没有办法系的旋光性(+)和(-)甘油醛绝对手性中心原子周围的配置。
用今天的术语,他没有办法知道是否(-)甘油醛(R)或(年代)。
缺乏这个关键信息,费舍尔选择猜一猜。
猜,这是正确的,是(-)甘油醛配置我们现在所称的年代,(+)甘油醛的配置我们现在所称的R。
当然,卡恩,英格尔德,测前还没有出生,和CIP系统只会开发1951年毕吉博的工作后。所以费舍尔开发自己的命名法。
画甘油醛在后来被称为费舍尔投影,他左边的配置分配给(-)甘油醛,并称之为L -(拉丁语laevo)。然后他右边的配置分配给(+)甘油醛,并称之为D -(拉丁语右旋的)。
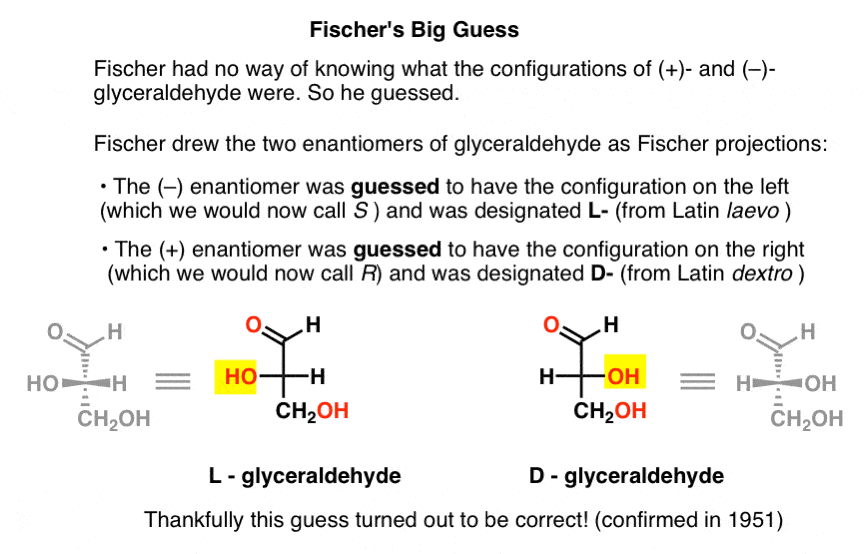
为什么这是如此重要?
分配绝对构型L -、D -甘油醛是有点像分配本初子午线(0°经度)格林威治皇家天文台的,英格兰。就像地球上其他地方的经度可以确定相对于这一点如果他们的相对距离是已知的,绝对构型其他异构中心可以确定,如果它的配置相对于L -或D -甘油醛是已知的。
这可能不是最清晰的类比。让我们看看另一个例子的4碳糖。
4所示。四个碳醛D -和L -糖(Aldotetroses)
曾经的绝对构型提出了L -、D -甘油醛,其他手性化合物的绝对构型可以建立了类比(很多化学繁重工作)。
今天不是至关重要的,但对于这种推理的一个例子,看到这个(注2]。(我们将重新审视它,当我们写费舍尔证明葡萄糖的结构。)
手性中心的概念被引入的时候,你可能发现一个分子与n手性中心将会有2n立体异构体(只要没有内消旋化合物)。
有两个四碳醛糖,苏阿糖和赤藓糖。他们每个人都有两个手性中心。每个存在的一对对映体(L - D)给四个立体异构体。
在这儿呢。下图中值得注意的一件重要事情是,糖的L-family哦组底部左边的手性碳,和d户型有哦组底部右边的手性碳(强调)。
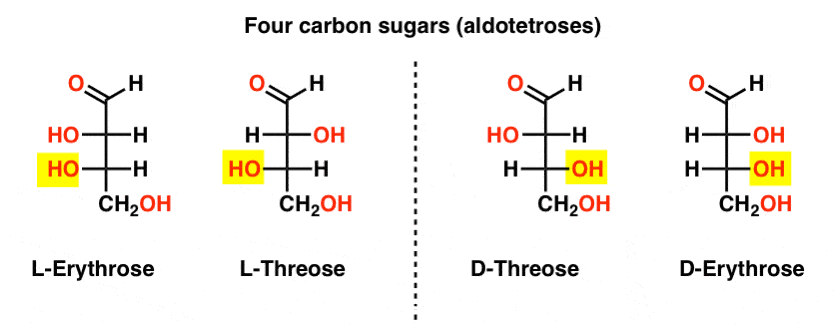
看到L-Erythrose和L-Threose构建异构中心成立于L-glyceraldehyde(强调),和D-Erythrose D-Threose建立异构中心成立于d -甘油醛(强调)。
糖是建立有点像二进制系统;你可以把每个异构中心是一个“点”,可以有两个值之一。的配置L-erythrose和L-threose只在一个异构中心有所不同。如果我们抛H和的位置哦,我们会得到另一个。这种关系有一个名字,你可能会看到有时:两个分子,产生相反的配置在一个异构中心被称为异构体,特别是当一个原子连接到异构中心是一个氢(H)。
5。五碳醛D -和L -糖(戊醛糖)
有一个五碳四方醛糖(戊醛糖):核糖、阿拉伯糖、木糖和来苏糖,每个现有的一对对映体(D, L -)。
应该最熟悉的名字列表核糖糖的骨干,这是核糖核酸(RNA)。
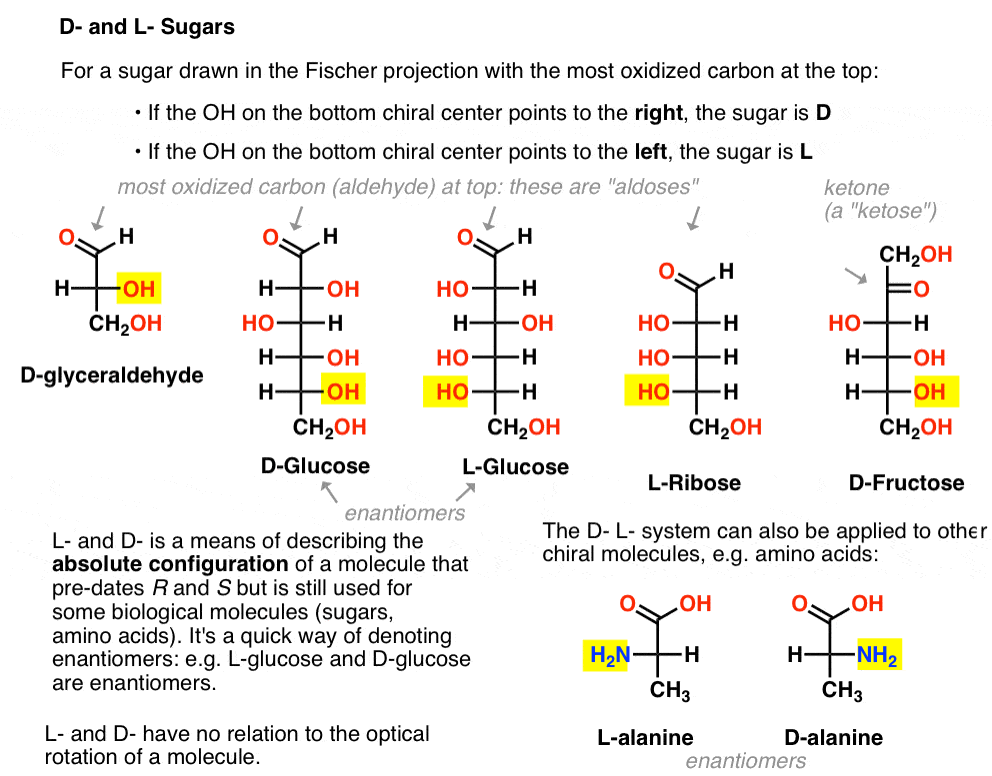
在下图左边,我们有L-aldopentoses,所有共享相同的配置异构中心当底部醛放置在顶部。
他们的对映体D-aldopentoses,右边,底层异构中心的所有共享相同的配置(强调)。
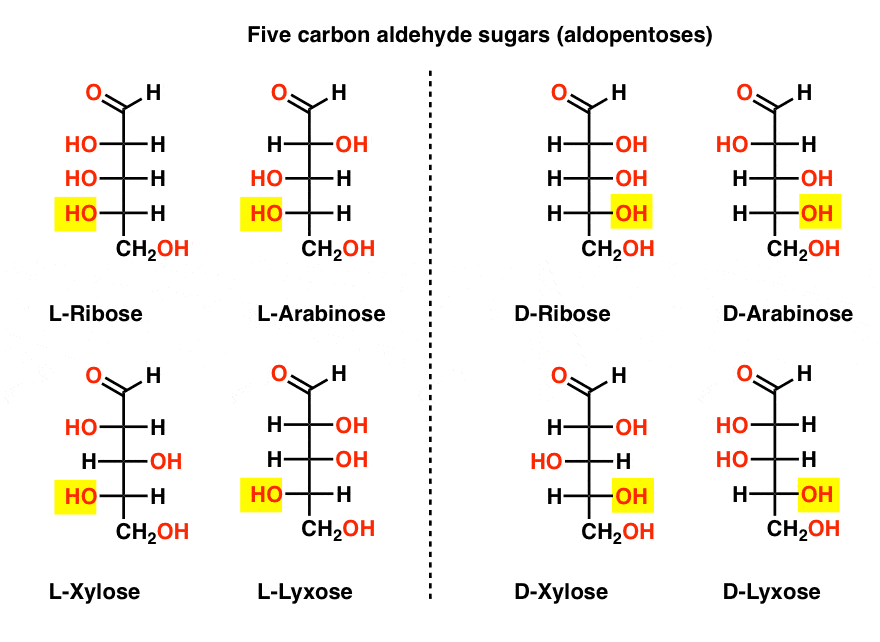
在这一点上我们应该指出,绝大多数的糖在地球上的生命形式是D -糖,包括一小RNA的支柱。为什么和如何在地球上所有生物以e糖结束是一个谜,是一个假定l糖会工作得很好。这提供了谷物等科幻作家阿瑟·c·克拉克,以及有些差强人意《星际迷航》的小说。谢谢@Prof_West,@vancew,@RoseChem2和@PeONor建议!)
6。六个碳醛D -和L -糖(己醛醣)
如果有4戊醛糖,每一双D - L -对映体(8立体异构体总量),那么有多少己醛醣?
有8个D-L -双(16立体异构体总量)。最熟悉的是葡萄糖,但你可能会认识甘露糖和半乳糖。有些人很少,在自然界发现的(艾杜糖,有人知道吗?)。
这是D-aldohexoses。注意,他们都有相同的配置的手性中心,d -甘油醛。我们看到的一样
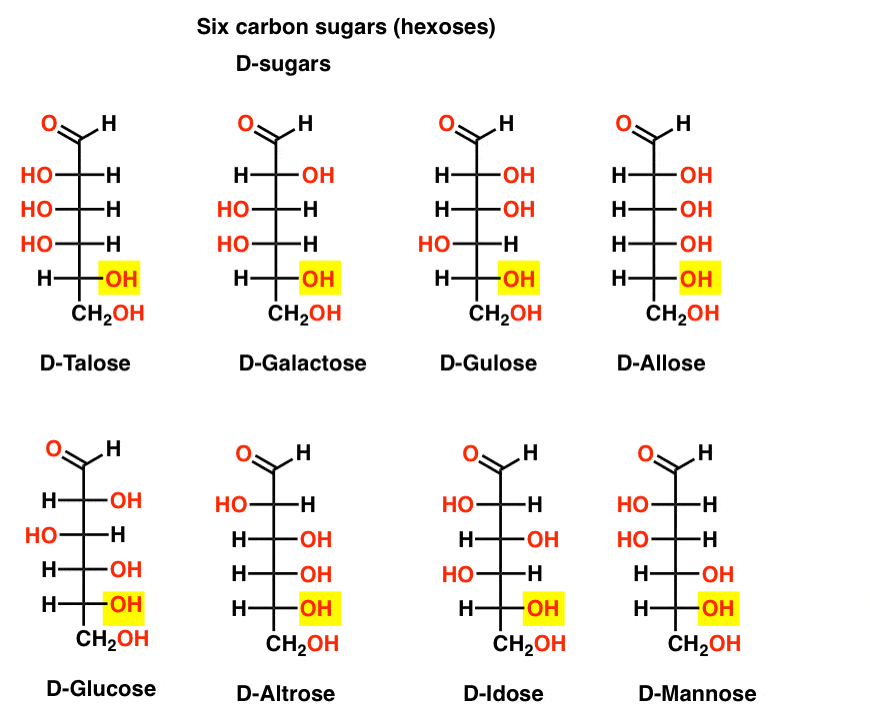
在L - e糖相比,糖在自然界发现的(下图)很少。有趣的是,L-glucose一直探索作为糖的替代品。它的味道是区别天然葡萄糖,但因为它没有提供营养不能被分解由我们(手性)的酶。结果是生产与代糖太昂贵,甜菊糖甙、阿斯巴甜等人。
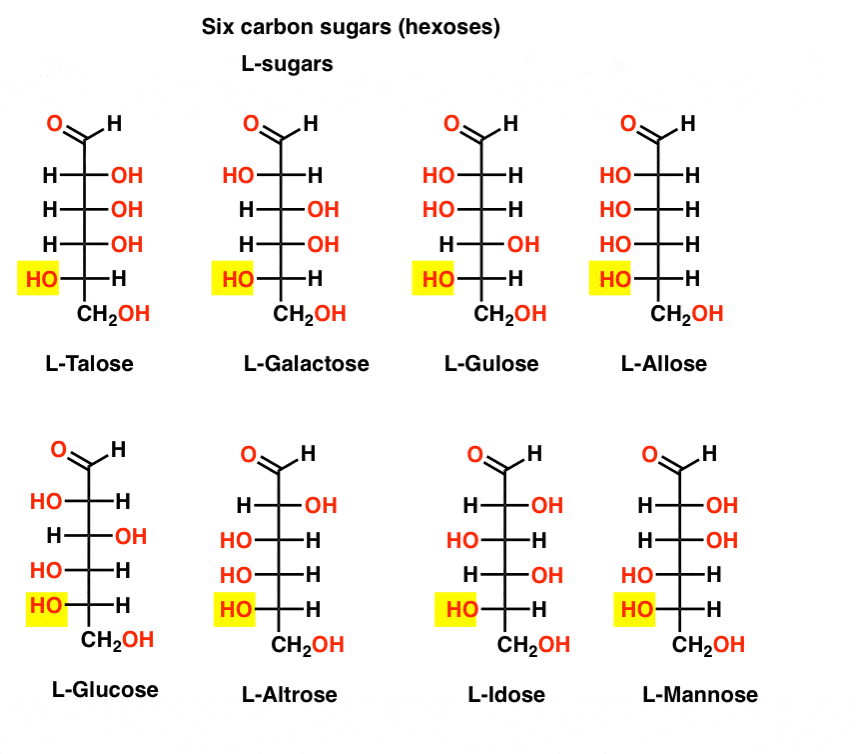
好,这就够了。已经7号碳糖(庚醛糖),但他们不是生物学意义重大。
7所示。但是等等——还有更多!(氨基酸)
如果你画氨基酸在费舍尔投影用最顶部(氧化组羧酸),那么你也可以分配L - D。
纳入19手性氨基酸的蛋白质(proteinogenic是适当的术语)都是L -。(甘氨酸是手性的,所以D, L -不适用)。一些D -氨基酸是自然发生的,但他们很少(主要在细菌,发现的例外鸭嘴兽毒液),不是由信使rna编码。
有趣的是,尽管19个手性氨基酸L -,只有18 19 (S)。有什么异常吗?
(这是好有机化学酒吧琐事)。
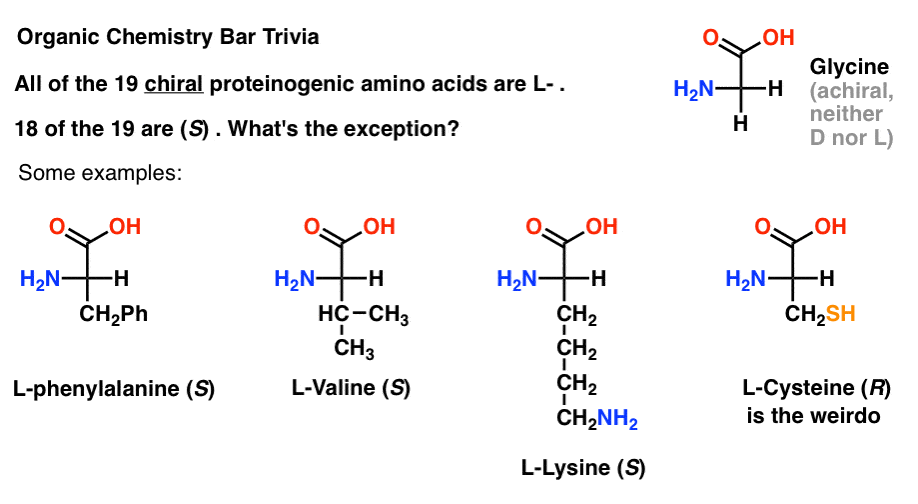
半胱氨酸是怪人。
(如果你还说加分硒代半胱氨酸…书呆子)。
8。摘要:D -和糖类和氨基酸L -符号
这是D - L -系统转让绝对构型。它适用于糖类,因为他们可以建立系统(如二进制系统)。它也是有用的氨基酸。关键是看底部异构中心虽然费舍尔的画投影。对吧?d .离开吗?l
当然,糖在费舍尔并不总是那么有助于吸引预测——他们形成环。我们会写关于确定D, L -在循环糖在以后的帖子中。
我不得不说的是,感谢无论你选择相信神,费舍尔的猜测是正确的。这将是一个巨大的眼中钉筛选70 +年的化学文献知道错误的配置被分配给所有糖类和氨基酸。
感谢托马斯Struble援助与这篇文章。
笔记
相关文章
注1。“倒数第二异构中心在大多数手性糖是R,虽然在大多数氨基酸异构中心S”没有完全相同的戒指,特别是半胱氨酸是R .)
注2。这里有一个思维实验确定的相对配置赤藓糖和苏阿糖。(我说“思想实验”,因为我不想包括特定的试剂,它可以是分散)
如果一个人开始纯(+)赤藓糖和氧化伯醇到一个醛用已知的方法,得到一个化合物缺乏任何旋光性。(-)赤藓糖也是如此,它返回一个完全相同的化合物。从这可以推断,新化合物的结构必须的分子有一个内部镜飞机吗(即内消旋)。(di -氧化化合物进一步羧酸会产生内消旋酒石的酸,其结构是已知的)。
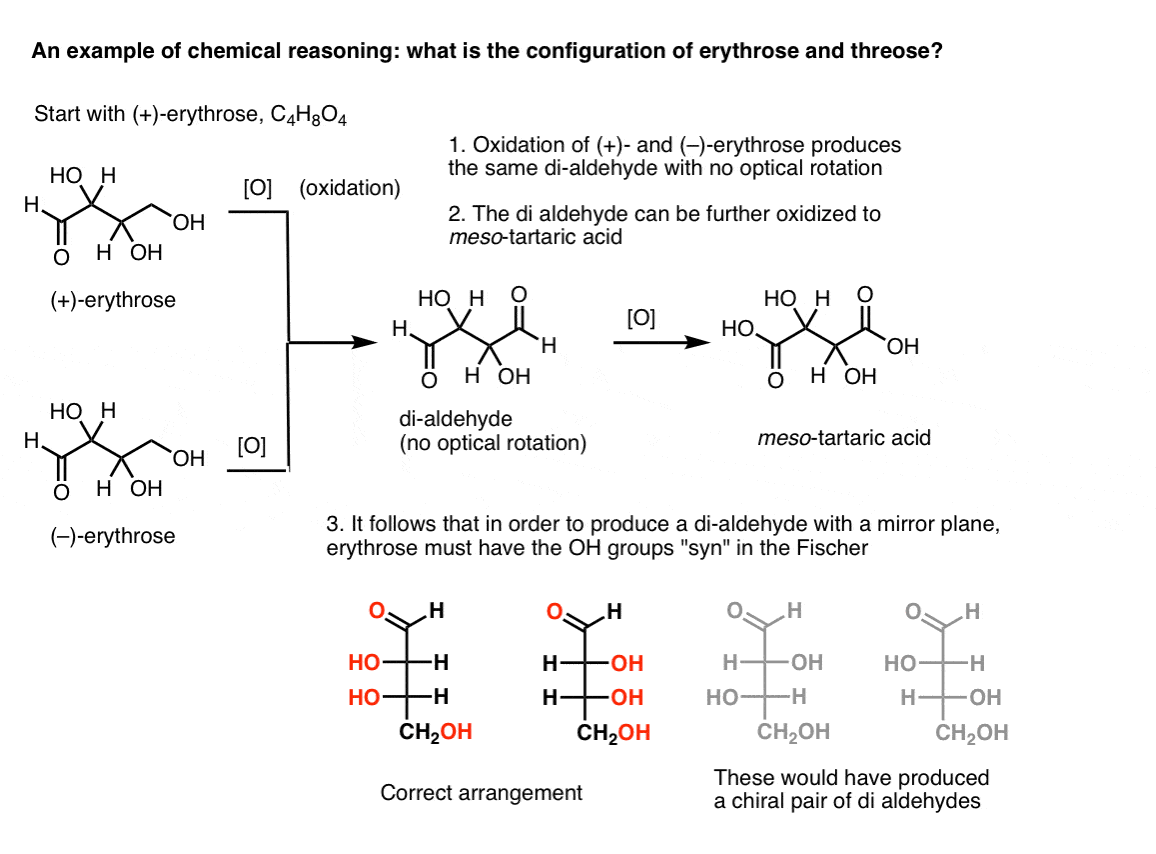
相比之下,执行相同的操作(+)在di -苏阿糖结果醛保持旋光性。与大小相等,方向相反旋光性化合物是由(-)苏阿糖上执行相同的操作。这两个化合物是对映体。为了是真的,苏阿糖的羟基的相对取向必须反。这些化合物可以被进一步氧化,分别为(-)-(+)-酒石酸。
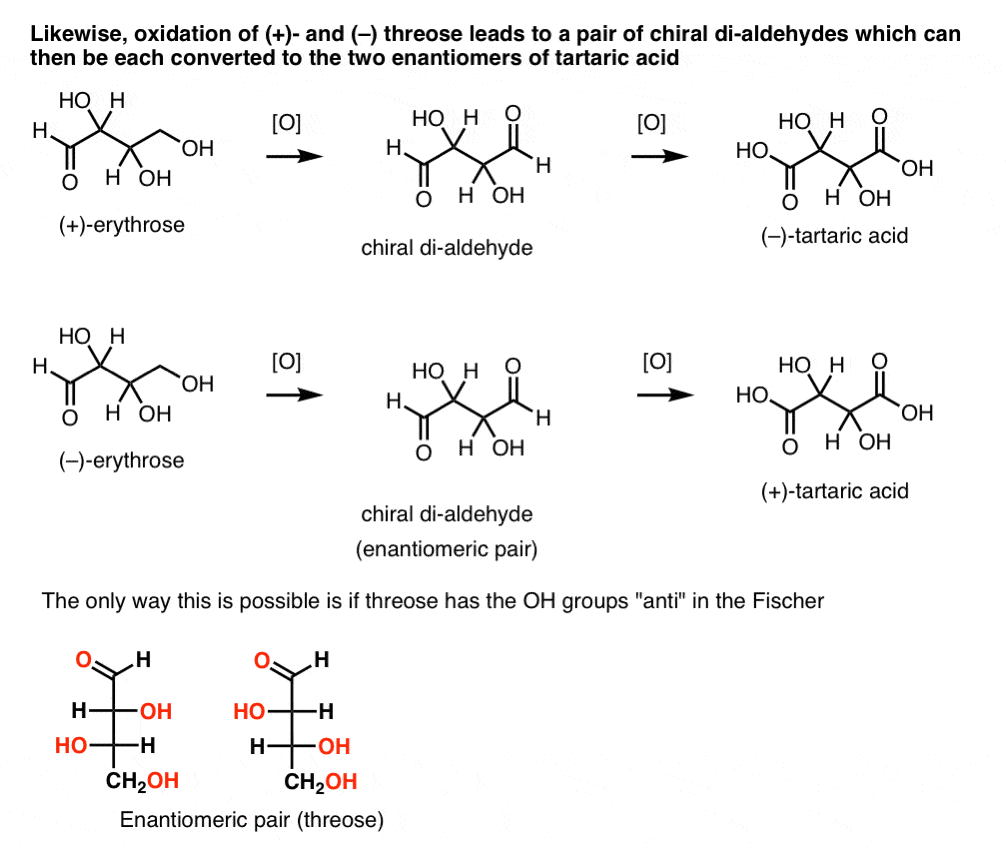
同样的推理可以用相反的方向(减少)。例如(-)或(+)- - - - - - -赤藓糖可以减少tetra-ol赤藓糖醇,这是内消旋。
同样,减少(+)和(-)苏阿糖结果tetra-ols一对旋光异构体,threitol。
从这些事实中我们可以推断出的相对取向哦组。
(注:在旧文学,这些条件erythro -和threo -有时被用来描述对非对映体之间的关系有两个手性中心。现在我们倾向于使用syn和反相反)。
(高级)引用和进一步阅读
- 超级死名称冯optischen Antipoden军队Buchstaben死去d和l
埃米尔费舍尔
的误码率。1907年,40(1),102 - 106
DOI:10.1002 / cber.19070400111
这就是著名的纸,埃米尔费舍尔教授(任意)(-)甘油醛L-stereochemistry分配。 - 合成嘌呤和糖组
埃米尔费舍尔
诺贝尔演讲,1902年
费舍尔的诺贝尔演讲,他谈到他的工作不仅在碳水化合物,而且在嘌呤,其中化合物咖啡因和可可碱等成员。费舍尔教授预测能量饮料的兴起(如红牛),说,“一天一点想象力的锻炼可以预见当bean将不再被要求做出好的咖啡:少量的粉末从化工厂一起水将提供一种美味,清凉饮料便宜得惊人”。 - 的决心绝对构型通过x射线光学活性的化合物
毕吉伯,J。,PEERDEMAN, A. & van BOMMEL, A.
自然1951年,168年,271 - 272
DOI:1038/168271a0
著名的论文证明,使用x射线结构分析,“埃米尔费舍尔的惯例,分配的配置图2的右旋的酸,似乎回答现实”。 - 埃米尔费舍尔的发现葡萄糖的配置。一个五十周年回顾
c . s .哈德逊
《化学教育1941年,18(8),353年
DOI:10.1021 / ed018p353
早期检查覆盖教授埃米尔费舍尔在碳水化合物化学的工作。 - 埃米尔费舍尔的证明,糖的配置:百周年纪念
油炸w . Lichtenthaler
Angew。化学。Int。。1992年,31日(12),1541 - 1556
DOI:10.1002 / anie.199215413
非常可读的回顾从1992年开始,覆盖在碳水化合物化学与费舍尔教授的工作是深入到碳水化合物的立体化学作业。
你好,
我们如何确定d和l配置在循环糖?
己糖,你看(R)的c - 5异构中心e糖。当己糖画作为一个六元环C1-c2-c3-c4——顺时针编号(99%的情况下,即右侧颈- 1异头碳)如果c - 5 CH2OH点,D,如果点了它的L。
情况变得更加复杂,如果己糖画的吡喃糖的形式。你需要确定c - 5 (R)或(S)。
为戊糖,你必须看看c - 4手性中心。
假设非常先进的技术,如果人类是人为创造的但每手性分子在其相反的对映体“正常”,左、右手的人的百分比会逆转在这样一个人口?
我不知道,我们完全理解是什么让人类左或右撇子首先,所以你想和我的一样好。
为什么最后一个不对称碳原子,决定了D / L配置?
好问题。命名约定,所以在某种程度上,它变成了,“因为X这么说!”,而不是一个物理解释。
然而,它比至少有一个明智的选择。如果是最近的不对称碳* *确定D / L的醛,这将带来严重的问题,c - 2碳的配置可以改变通过“差向异构化作用”(即形成烯醇/烯醇化物其次是质子化作用)。“D”和“L”表示“绝对配置”,因此定义两个对映体,这将是一个糟糕的协议如果改变一个手性中心(如烙c - 2葡萄糖给甘露糖)导致切换的名字从D - L -。
我不知道这是否回答了你的问题,随时深入到更具体的东西。
你觉得化学厂商出售“D(+)蔗糖”吗?
(是的,谷歌它,有很多这种情况发生)。
D或L异构将由氨基
是的,这是正确的。
氨基酸苏氨酸、D和L会由羟基的位置而不是第二个手性中心的氨基羧酸盐(更远的)?同样,希望D或L异亮氨酸,由甲基/乙基远离比氨基羧酸盐?
嗨,亚伦,D和L是由氨基集团不是sidechain。
感谢分享神奇的工作。
这就跟你问声好!我确定提取l -半胱氨酸的R / S构型。我可以知道如果我的理解正确吗?
看手性碳,4组是氨基,羧基,H和CH2SH。我分配任务# 1氨基和# 4 H .然后其余组之间,羧基的碳是附加到O, O, O在碳CH2SH连着年代,H, H。我不总结时原子的基于“增大化现实”技术的分配优先级。年代,H, H是给定一个更高的优先级比O, O, O原子由于年代仅拥有更高的基于“增大化现实”技术比O原子。
因此,CH2SH # 2为主而羧基# 3。我说的对吗?
你的回复将非常感谢!
你是绝对正确的,格温。
为什么所有elible糖D形式而不是在L形式吗?
这是一个非常深奥的问题,可能是“冷事故”由于地球上的生命如何进化的怪癖。我们只是不知道。
葡萄糖和绘制不正确吗?
第一个图但末期。
最后,L-glucose画,葡萄糖的对映体。
问题,如果你把费舍尔投影的分子,例如苯丙氨酸。D / L -系统还适用还是…?
规则是你必须要有最氧化碳顶部的费舍尔。因此,费舍尔必须与顶部的羧酸。D, L -苯丙氨酸仍然适用。
如果有一个胺组和一组-哦?我们将如何命名为优先考虑
-哦- nh2吗?
我不知道你的意思。你必须提供一个示例。碳连接和-哦- nh2不会很稳定(动物)
伟大的文章。只是一个小小的更正:“L / D -系统允许的配置一个分子与多个手性中心总结了一个字母。“为己醛醣,字母本身只是缩小了立体化学的一个8配置;是字母+配置前缀(“gluco”),明确了具体的差向异构体。
我很喜欢D / L系统。它提醒我们,必须定义所有四面体立体化学相对的东西。与国际马铃薯中心相对于附件的订购一些规则在一本书里。与D / L D / L-glyceraldehyde的相对排序。各种文件格式的分子,它通常相对于原子的顺序文件。
谢谢诺尔,校正和评论。