构象和环烷
乙烷的交叉与重叠构象
最后更新:2022年12月13日|
交叉与重叠构象的乙烷,或者为什么纽曼是可怕的
三维形状的甲烷(CH4)在所有条件下都是一样的,但是乙烷(C2H6)和高烷烃可以假设不同的三维形状由于沿着碳碳键旋转。
本文简介:介绍构象异构体,交错重叠构象,纽曼式,二面角的扭转角,乙烷和旋转障碍(扭转应变)!
表的内容
- 回顾:甲烷(CH的四面体结构4)
- 乙烷的三维结构(C2H6)
- 乙烷的旋转以及碳碳键:构象异构体
- 乙烷的重叠和交错构象
- 乙烷的纽曼式
- 反角,或扭转角
- 映射的构象乙烷二面角
- 扭转应变
- 笔记
- 测试你自己!
- (高级)引用和进一步阅读
1。回顾:甲烷(CH的四面体结构4)
在以前的文章中我们讨论了我们知道甲烷CH4四面体(看到:我们怎么知道甲烷是四面体吗),这种形状的成键电子对之间的距离最大化。
我们也看到,CH4是一个完美的四面体,H-C-H键角109.5°。
描述甲烷在三维空间中,应该习惯画两个完整的线条来描绘的碳氢键的碳氢键页面的平面。碳氢键指向出页面的画,给人以“楔”(重型)债券,碳氢键指向成(后面)页面用一个“冲”键。
本公约借老艺术家的技巧:给的错觉的角度来看,描述对象在前台与高对比度(重线),较低的背景和对象对比(微弱的行)。
徘徊在一个弹出的形象。
这是两个“line-wedge”CH的图纸4。这两个图纸描述同一个三维对象。
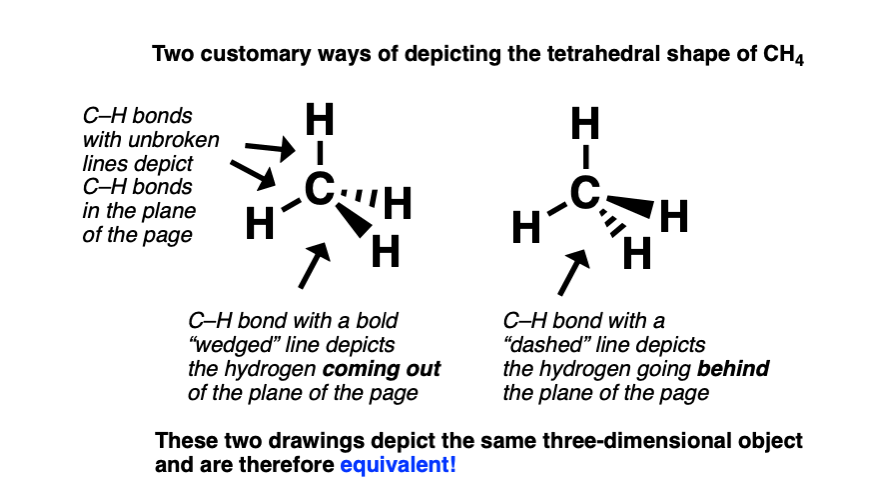
它不管下面画“楔形”债券或以上“冲”债券?
不。楔形画是否低于或高于dash只是一个角度,描述你会看到,如果你想要“对”或“到”CH4分子。
许多其他的透视图的甲烷是可能的,角度两个碳氢键在页面的平面最实用程序。它清楚地描述了所有关于中央碳原子排列四面体地需要最少的工作,因此往往是标准的方法来描述这些分子。
很少,是有用的其他视角的CH4。例如,你知不知道,当你看到一个碳氢键,它使其他碳氢键看起来由角度120°?

注意:很显然,H-C-H键角仍然109.5°。这里说的是什么从这个角度看三个氢画了一个圆,一个角度120°分离)。
更多详情。
2。乙烷的三维结构(C2H6)
如果这是甲烷的结构(CH4),那么接下来的结构是碳氢化合物,乙烷(C2H6)?
我们需要做的就是更换一个甲烷碳氢键的键CH3(甲基)片段。
两个碳四面体。
有几种方法来画使用粘结层图。其中两个是下面的画。
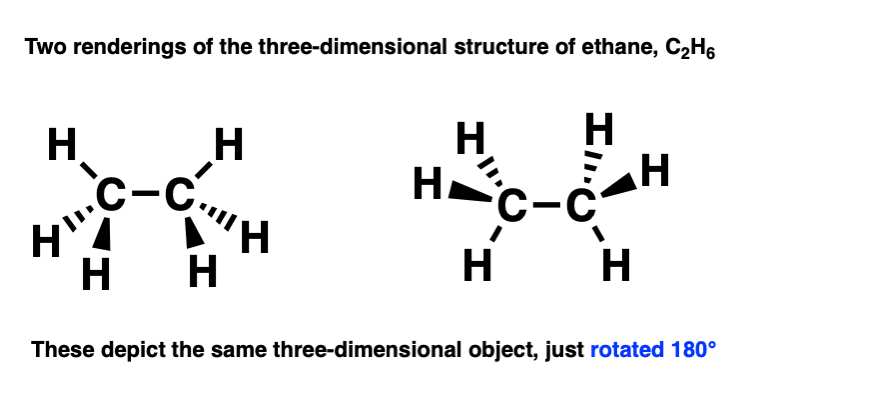
分子三维对象。注意,这些图纸两个描述相同的分子,但是从不同的角度所吸引。
这就清楚你的分子旋转180度。
通过建立的模型,通过一个旋转180度,我们可以发现他们是一样的。
很重要的一点:在化学,如果两个分子可以相互叠加,这意味着它们是相同的分子。
3所示。乙烷的旋转以及碳碳键:构象异构体
添加新的碳碳键的乙烷带来一些额外的并发症的有趣使有机化学(或者我们中的一些人喜欢说,“有趣的”)。
甲烷有相同的三维形状。我们可以从很多角度画,但它保留相同的形状。
这是不正确的乙烷!
这两个CH3由一个碳碳碎片了σ键。两个原子的连接通过一个σ键是连接两个乐高块通过一个“学生”和“管”。旋转可以发生在债券没有中断连接。
这个旋转的碳碳键可以产生各种三维形状。
这些不同的形状被称为”,构象”,或者,“构象异构体有时,“旋转异构体(旋转异构体)”。
这意味着第二个,完全有效,乙烷的方法了,是这样的:
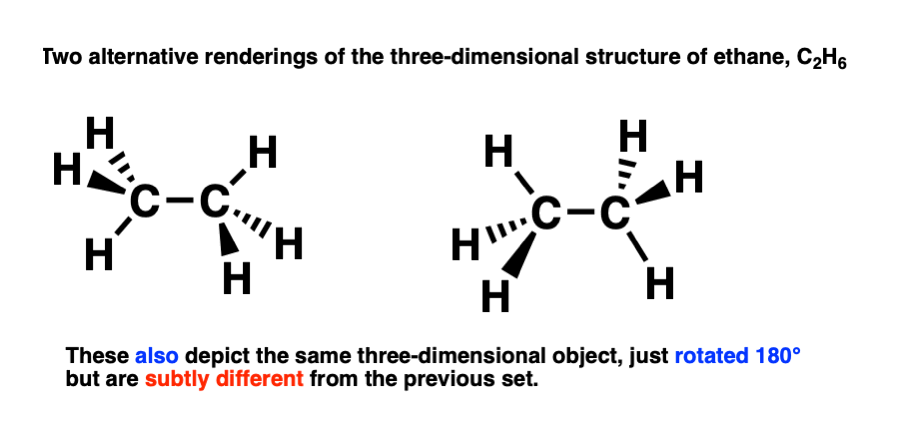
这是一个构象异构体乙烷的图纸我们以前(上图)。
区别很微妙!这两种构象可以互变异构体旋转的碳碳键60度,像这样:
所以这两个构象异构体代表相同的分子,但是不同的三维形状。
(这些形状也有微妙的差异,更多的能量时刻。]
4所示。乙烷的重叠和交错构象
如果它仍然是不明显的如何这两种形式的乙烷略有不同,它可能有助于看端点的。
乙烷的让我们看第一个图,看从右边沿碳碳键。为了展示这一点,我们经常使用小符号是为了看起来像一只眼睛,连同一个箭头显示的方向是“眼睛”。认为它是,“方眼”。
当应用这个“方眼”,我们得到:
注意,前面的三个氢碳正前方的三个氢原子在后面。
我们称之为“黯然失色“构象。
“端点的”视角的视频所示是一个纽曼式——更多详情。
现在让我们在第二个图的乙烷,看看从右边沿碳碳键。
在这种情况下,请注意,所有氢间距为60度。
这被称为“交错”构象。
一个重要的注意。当我们讨论“超越”和“交错”我们指的关系所有三个取代基的碳所有三个取代基的碳。
这是形成鲜明对比反角(如“syn”和“反”关系,下面讨论)我们比较的方向一个取代基碳就在前面一个取代基的碳。
5。乙烷的可视化交错vs重叠构象:介绍了纽曼式
正如您可能已经注意到的,“在端点的”观点交错、重叠构象在上面的短视频的方式。处理这些圆圈是什么?
这些都是纽曼的预测,一个有用的视觉援助比较构象异构体,命名他们的支持者,梅尔文美国俄亥俄州立大学的纽曼。(注2]
纽曼式是一个透视图的分子“结束”的债券。它并不是第一个建议注3)这个角度看,但这是成为行业标准。
“圆”是用来描述原子的前景模块视图在后台的碳。
对于乙烷,真的只有有趣的债券:碳碳键。
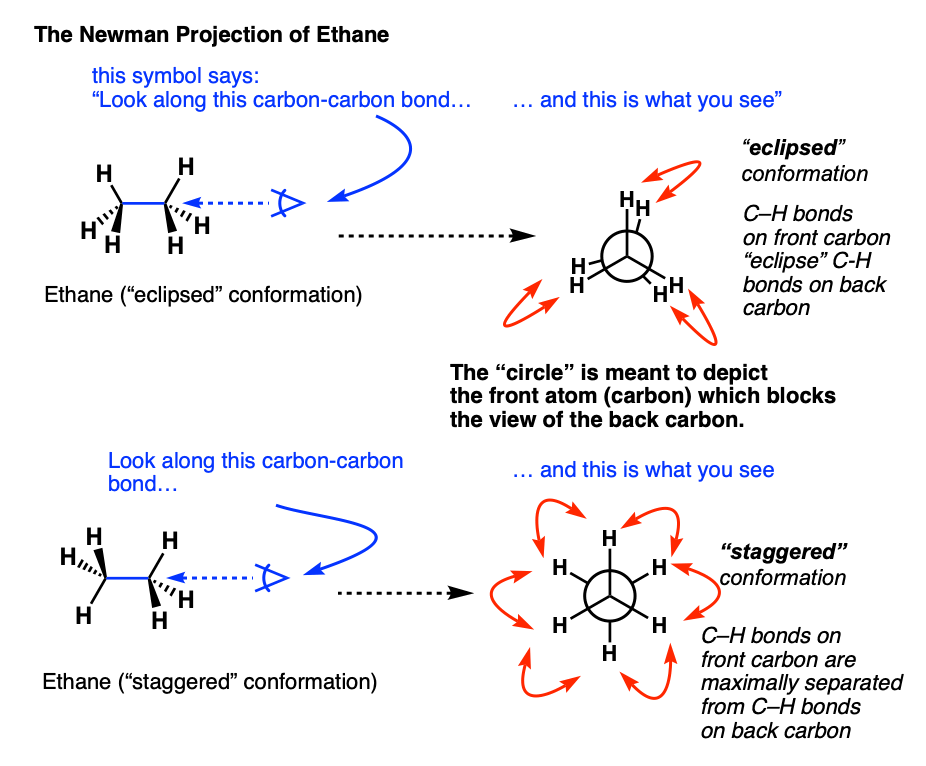
而不是考虑每一个构象(无限),它极大地简化了如果我们只考虑两个讨论极端乙烷-当相邻的碳原子上的碳氢键在他们互相最小距离(0°,重叠)或他们的最大距离彼此(60°,交错)。
6。双面角(或扭转角)
作为一个明智的人曾经说过,观点是价值80的智商。
纽曼式的天才是“端点的”的角度分析了前后之间的空间关系组更明显。
的反角[也:扭转角)被定义为四个原子之间的角度使a b c d时沿着c键。
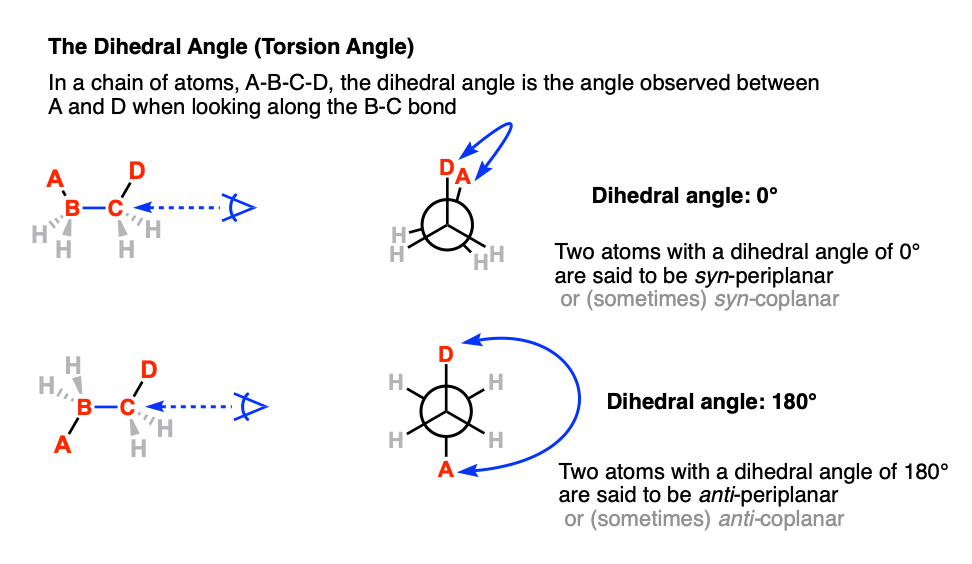
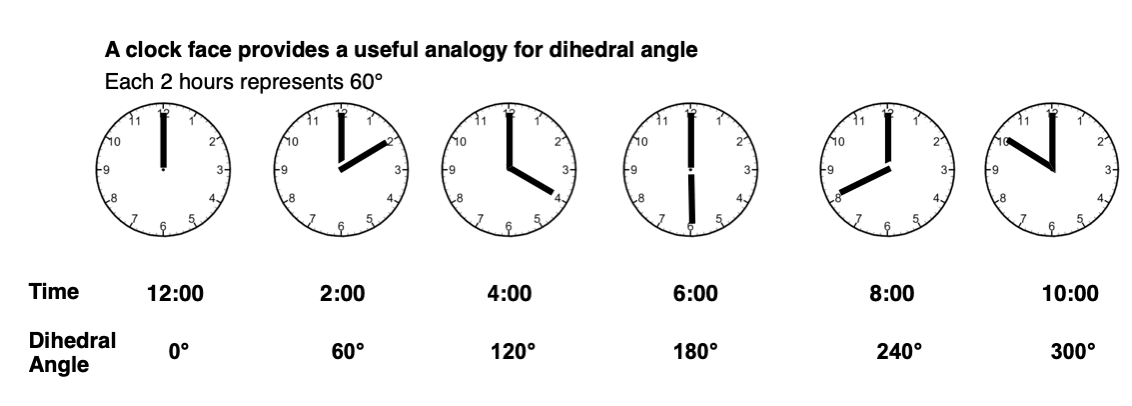
一个钟面是一个有用的类比。在12:00,二面角是0°。每小时代表30°。四面体碳的目的,30°不是很有趣(它不会导致一个能量最大或最小)让我们使用2小时的增量。
在所有可能的角度,这个术语syn是指当两个原子的情况同一侧的“赤道”(二面角+ 90°≥0°≤-90°)。和“反”是指当两个原子的情况赤道两侧(二面角(+ 90°≤180°≥-90°)
术语“periplanar”是指这种情况当两个原子的二面角是平行(0°,或12点在我们的时钟类比)或反平行的(180°,或者6点)。
7所示。映射的构象乙烷二面角
让我们尝试用乙烷。
为了定义一个扭转角,我们需要任意选择的两个相邻的碳原子上的碳氢键是我们的参考点。
先用红色高亮两个H原子,二面角的0°(12点在我们的时钟类比)。
如果我们从12点开始,保持前面CH3在同一个地方,同时旋转“返回”CH3在60度的增量,我们得到这样的:
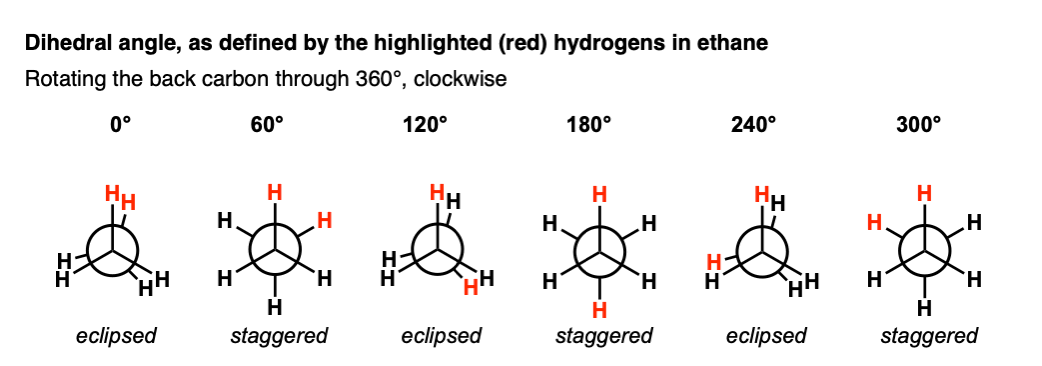
值得重复的是:交错和黯然失色是指的方向前3组关于回3债券。
这是不同的反角在这种情况下,这指的是角了H- - - - - -C- - - - - -C- - - - - -H当沿着碳碳键。
这里有一个快速的电影看起来像纽曼。
真的只有两个重要的构象的乙烷,他们重复3倍我们通过360°旋转碳碳键。
8。扭转应变
所以是两个重要的构象异构体乙烷等价的能量?
好问题!
没有他们不。1936年发现的坎普和比萨(裁判),这两个构象不同能源约为3.0千卡/摩尔和能量差可以测量通过各种技术(见这里)。
的交错构象的能量比低黯然失色构象。
这意味着有一个小旋转的障碍约为3.0千卡/摩尔。(注6)这一障碍不是足够大,以防止“免费”对碳碳键旋转,但它确实意味着交错、重叠构象存在于不同数量(交错主)。
(表示旋转的障碍的典型原因是范德华斥力相邻碳原子上的碳氢键的重叠构象。其他人支持一个“超共轭现象”的解释。进一步阅读的引用(12好奇]]。
手里拿着这些信息,我们可以做一个图的二面角和能源这样的:
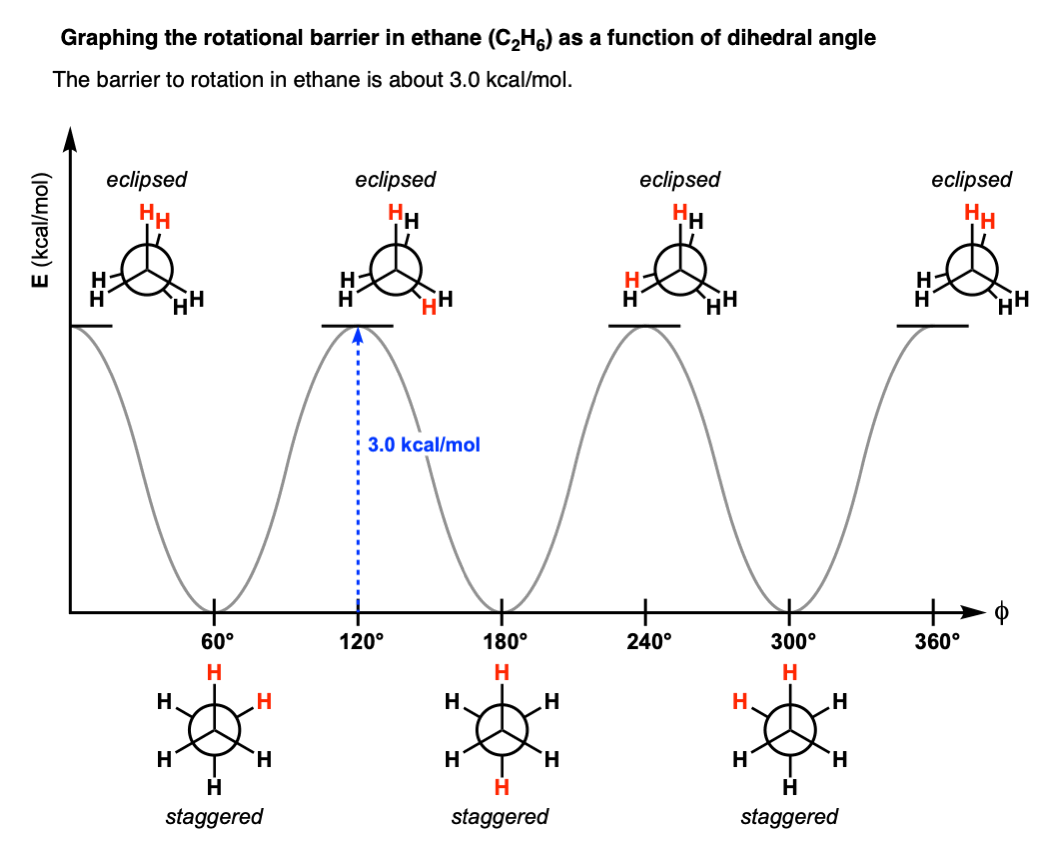
随着碳碳键进行旋转,这样分子从一个交错重叠构象,分子的经历应变。
这种类型的应变扭转应变,超过应变或比萨应变,这取决于你和谁说话。(注5]
“扭转应变”一词是一个比喻来扭转力的经历当你扭弹簧或(更常见)橡皮筋——例如,用橡皮筋驱动螺旋桨飞机。
迫使你觉得让弹性“放松”是扭转应变的一种形式。
9。丙烷和丁烷呢?
让我们总结一下:
- 分子三维物体像很多其他的事情在我们的日常经验
- 他们可以从不同的视角。改变不会改变分子的视角,但它可以帮助可视化某些特征。
- 两个分子是重合的相同分子!
- 复杂分子的描述更复杂的比甲烷是自由旋转的碳碳键的存在,导致构象异构体——分子相同,但不同的三维形状
- 通过债券旋转构象异构体是可互换的。互变现象发生的非常快,每秒几十亿次。
- 有两个重要的构象在乙烷:重叠和交错式
- 纽曼式是一个有用的概念构象可视化的工具
- 看着纽曼式时,二面角角度定义为是由两个指定原子之间前后碳。
- 交错、重叠的相对取向所有的债券在前面和碳所有的债券在碳。二面角及其包含的术语(syn、反periplanar)之间的关系一个人的债券在前面和碳一个人的债券在碳。
- 乙烷的障碍旋转约3.0千卡/摩尔交错式是最低构象
- 这个词用来指这旋转的障碍扭转应变
那么高烷烃呢?正如你期望,事情变得有点复杂…但这真的不是太坏的。
在下一篇文章中,我们来看看下一个烷烃构象,丙烷(CH3CH2CH3)
笔记
注1。CH的另一个描述4值得注意的是费舍尔投影,水平债券楔形,“出来拥抱你”,和垂直债券背后的“冲刺”,点页面。


这是本文的纽曼的预测。
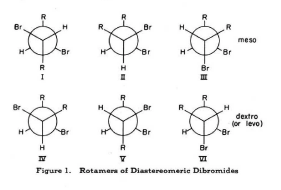
注3。纽曼不是第一个试图证明这个观点。出于某种原因,何曼思和比肖夫预测从未起飞。源。

注意4。从技术上讲,二面角(IUPAC)指的是两个平面之间的夹角,扭转角(IUPAC]的二面角是a - b - c和四项债券B-C-D飞机系统a b c d。二面角是一种更广泛的定义。对于我们的目的,我们将把它们作为等效项。
注5。IUPAC决定取代“扭转应变”和“比萨应变”和“超过应变”。这防止人们使用这些术语的机会在日常实验室的说法是零。
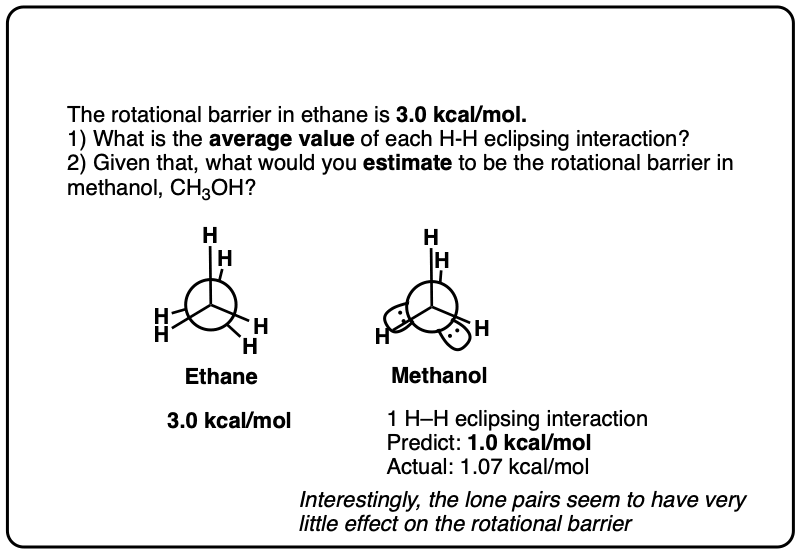
注6。自乙烷扭转应变约为3.0千卡/摩尔,这将意味着每个碳氢键超过交互价值约1.0千卡每摩尔。在CH3nh2上面的重叠构象是1.98千卡/摩尔交错式,和CH3-哦上面的重叠构象是1.07千卡/摩尔交错式,所以这些结果大致同意“每超过1千卡每摩尔碳氢键”的结果。
测试你自己!
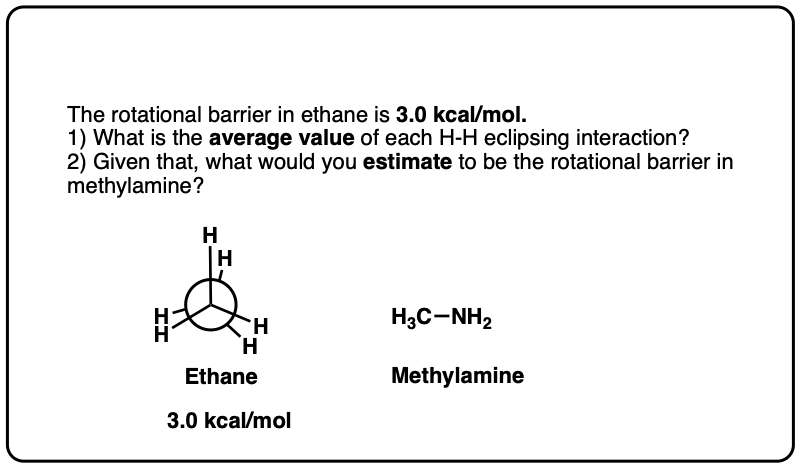 点击翻转
点击翻转
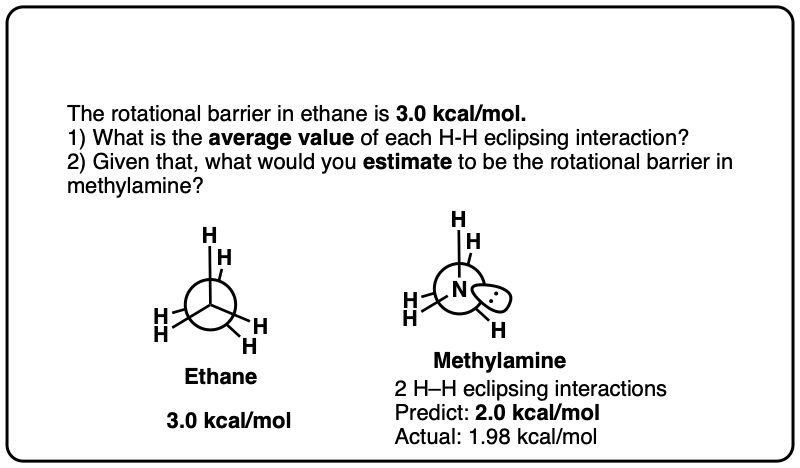
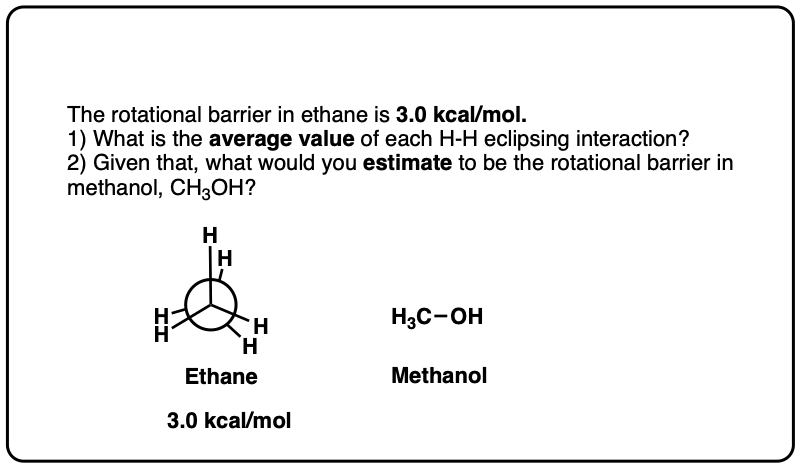 点击翻转
点击翻转
(高级)引用和进一步阅读
- C2H6的红外光谱
林肯·g·史密斯
j .化学。理论物理。17,139,(1949年)
DOI:10.1063/1.1747206
本文是首次确定乙烷的交错式是能量最低的轨道,通过测量红外光谱。 - 内部旋转乙烷计算障碍
Pitzer和威廉·r . m . s .以至于
j .化学。理论物理。39,1995年(1963年)
DOI:10.1063/1.1734572第一个理论计算旋转势垒的乙烷,从未来的诺贝尔奖获得者威廉s以至于。 - 乙烷的内部旋转的障碍
罗素·m·比萨
的化学研究1983年16(6),207 - 210
DOI:10.1021 / ar00090a004
回顾的历史决定旋转障碍在乙烷,估计约为2.90千卡/摩尔在写作的时候(1983年)。注意,这是不比萨谁写的1936年首次报道障碍旋转在乙烷(K.S.),但由他的儿子罗素,他的同一领域作出了重要贡献。 - 旋转和反演起源的障碍
理查德·f·w·巴德j . r . Cheeseman k . e . Laidig k . b . Wiberg, c . Breneman
美国化学学会杂志》上1990年112年(18),6530 - 6536
DOI:10.1021 / ja00174a012
理论研究旋转势垒的乙烷,甲醇和甲胺,说明旋转势垒的起源不符合之间的斥力碳氢键!(尽管他们没有提到这个词,“超共轭现象”,这里是隐含的)。 - 符号研究某些立体化学问题
梅尔文·纽曼
《化学教育1955年32(7),344年
DOI:10.1021 / ed032p344
原文由纽曼描述他同名的投影。还介绍了术语,“旋转异构体”。 - 超共轭不立体排斥导致乙烷的交错结构
Pophristic诉;古德曼,L。
自然411年,565 - 5682001年
DOI:10.1038 / 35079036
旋转势垒的起源的观点乙烷是由于超共轭。 - 的空间排斥导致乙烷的交错式
Bickelhaupt, F.M.& Baerends e . J。
Angew。化学。Int。。42岁,4183 - 41882003年
DOI:10.1002 / anie.200350947
应对上述纸。
谢谢你的材料
赞美太阳:D
好的,谢谢,现在我明白了:
所以“我们”确实是增加能源系统:)
感谢
是的,但是为什么呢?
我给原因应该防止旋转。
让我们假设一个分子在重叠构象,然后转向交错式(如果可能的话)
这个分子如何回到重叠形成?它需要能量。
这种能量从何而来?
如果我们不添加任何外部能源系统,随着时间的推移,所有分子都应该在交错式。这意味着这种差异应该防止旋转,但它不是。这是为什么呢?
在绝对零度(0 K)就没有能量和分子将被锁定在一个交错式,它将无法摆脱。
在0 k所有分子运动停止。
随着温度的增加,更多的热能可用,分子碰撞和旋转最终将成为有足够能量的分子打破浅势能三千卡每摩尔的“嗯”和其他假设构象。
长话短说,在室温下,一个好的经验法则是大约20千卡每摩尔的热能用于反应发生在一个合理的利率。
所以在室温下有足够能量用于乙烷在不断旋转的碳碳键之间的重叠和交错构象。
为什么这些构象之间的能量差不防止旋转?
因为:
如果分子想要最低的能量随着时间的交错式应该赢,随着时间的推移,所有的分子都应该有这种构象。
设想着,当然,我们没有添加任何能源系统。
如果是这样,任何差异,无论多小,应该防止旋转。
你是正确的,能量差*不*防止旋转。
在任何给定的时间交错式中的分子的人口将高于分子重叠构象,因为它是低能量约3千卡每摩尔。
你好詹姆斯!
标题扭转应变下,你有提到旋转,碳碳键的障碍不是自由旋转。但不是一个碳碳键意味着自由旋转?我们只限制在双键旋转对吧?提前谢谢。
好问题,好点。我改变这句话更明显,仍然是免费的,但旋转交错和重叠构象不同人群,他们的相对能量成正比。谢谢!