烯烃的反应
烯烃添加模式#3:“协同”途径
最后更新:2022年11月28日|
“协调”机制烯烃加成反应:硼氢化、氢化、环氧化、二羟基化、西蒙斯-史密斯环丙烷化。
相比之下烯烃的加成反应碳正离子的途径和三元环路径,我们在前两篇文章中看到烯烃的硼氢化反应S是反常的。反应的区域选择性为anti-Markovnikov而加成的立体化学是syn”。
我们还看到,“同步”立体化学是由于协调机制的性质提出了这个反应。
还有其他反应吗烯烃生产类似的结果硼氢化反应?
的产物syn之外作为一个结果协同机制?
当然有!
目录
- 烯烃加成反应中的协同机制
- 烯烃与氢的氢化反应2和金属催化剂,如Pd-C
- 烯烃与过氧酸的环氧化反应元-Chloroperoxybenzoic酸
- 四氧化锇(OsO)对烯烃的二羟基化作用4)
- 用Simmons-Smith试剂进行烯烃环丙烷化(锌铜偶)
- 烯烃与氯仿和碱的二氯环丙烷化反应(给二氯苯)
- 烯烃加成反应中的协同途径
- 笔记
- (高级)参考资料和进一步阅读
1.烯烃加成反应中的协同机制
回顾一下之前的文章,这是硼氢化反应过渡态的图烯烃显示产生的一致机制syn加法。
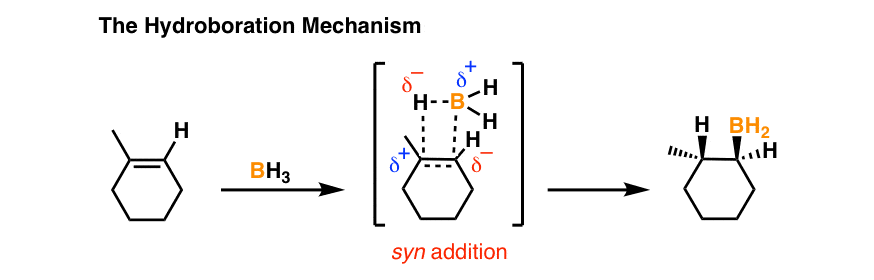
其他一些反应烯烃通过协调一致的过渡状态进行的有:
- 氢化反应(Pd-C, H2)
- Dihydroxylation (OsO4)
- 环氧化作用(有数3.H;元-chloroperoxybenzoic酸,m -CPBA是这个家族中常见的试剂)
- 摘要(CH2我2Zn-Cu)
- Dichlorocyclopropanation (CHCl3.KOH)
虽然每个反应的确切机制不一定相同,但每个反应都经过一个过程协调一致的过渡态和加成的立体化学是syn.这里需要注意的重要一点是,不同于硼氢化反应,每个反应都是给每个碳加上相同的原子烯烃,因此,“区域选择性”的问题是没有意义的.
事实上,反应产物有这些共同的特征(如果不是确切的机制)仍然允许我们将它们组合在一起,作为一个松散连接的“家族”——如果你愿意,也可以称之为“协调通路”。
让我们一个一个来看看:
2.烯烃与氢的氢化反应2和金属催化剂,如Pd-C
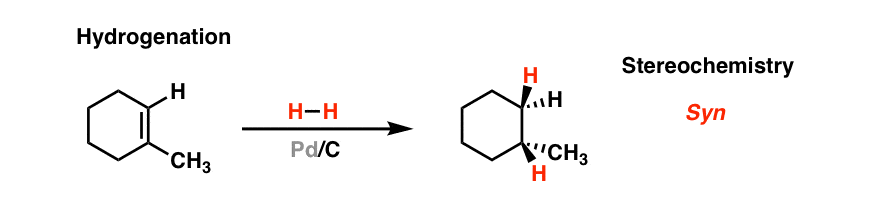
治疗烯烃使用氢气和"贵重"金属催化剂,如钯(Pd)或铂(Pt) [镍、铑、钌和其他金属也有用途]的结果是两个氢原子加到物体的同一表面上烯烃.在这些条件下,烯烃而氢气都是"广告吸附在金属表面。
在反应的过渡态中,两个氢原子都被转移到烯烃.反应速率取决于表面积:将金属分散在细碳(木炭)上可大大提高反应速率,因此使用木炭(细碳)。[注1]
3.烯烃与过氧酸的环氧化反应元-氯过氧苯甲酸(米-CPBA)
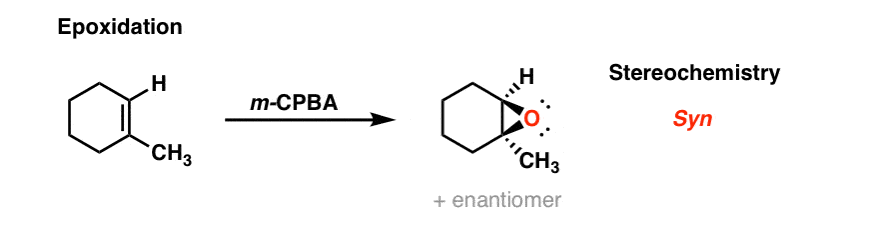
治疗烯烃用过氧酸,比如米-CPBA结果形成一个环氧(环氧乙烷)。这也可以通过协调的过渡状态发生: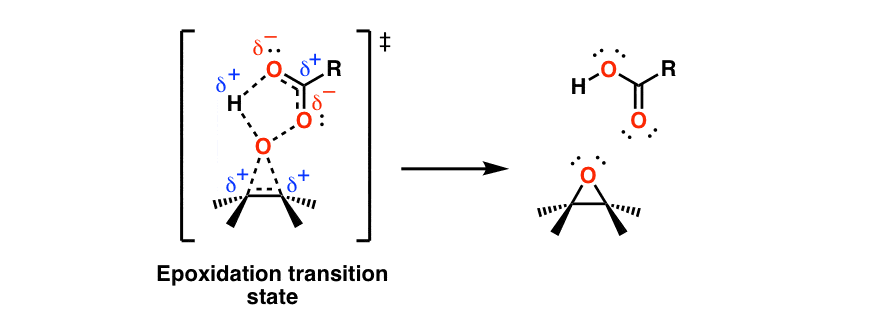
注意,当(弱)O-O键断裂时,过氧酸中的质子被(弱)O-O键带走。羰基氧气。
4.四氧化锇(OsO)对烯烃的二羟基化作用4)
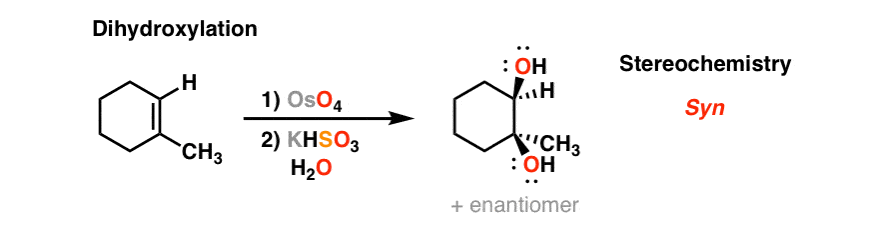
四氧化锇,OsO4,(见文章:四氧化锇OsO4)会增加烯烃形成两个新的碳氧键。立体化学也是syn.
这个反应的中间产物是一种含锇的环状化合物,称为锇酸osmate酯.第二步显示为灰色(KHSO3.H2O)导致O- os键断裂并形成醇。这被称为“水解”。KHSO3.是一个还原剂以及在检测有毒锇时的艾滋病。
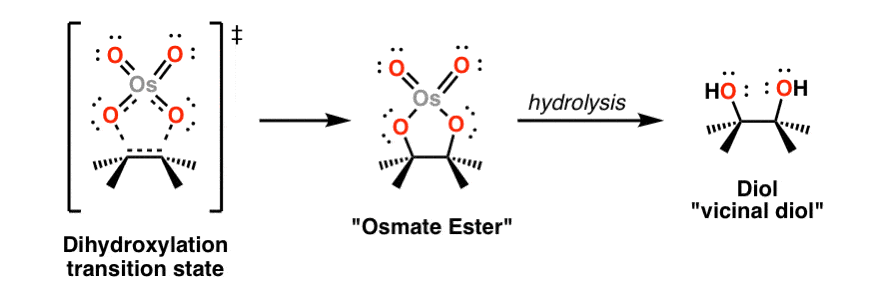
5.用Simmons-Smith试剂进行烯烃环丙烷化(锌铜偶)
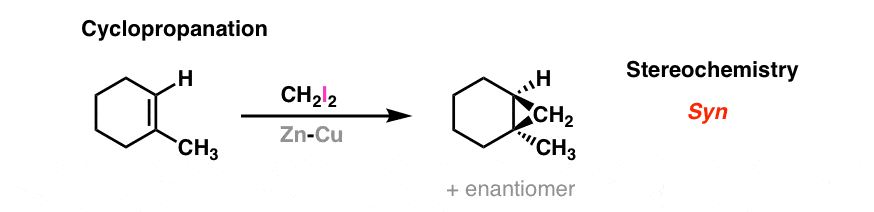
在一个有时被称为“西蒙斯-史密斯反应”的反应中,二碘甲烷(CH2我2)和锌铜偶(“Zn-Cu’”)形成碳烯”(实际上,一个carbenoid更准确地说).烯烃加入这个物质就得到了环丙烷。加成的立体化学是syn.下面是这个反应的过渡态:
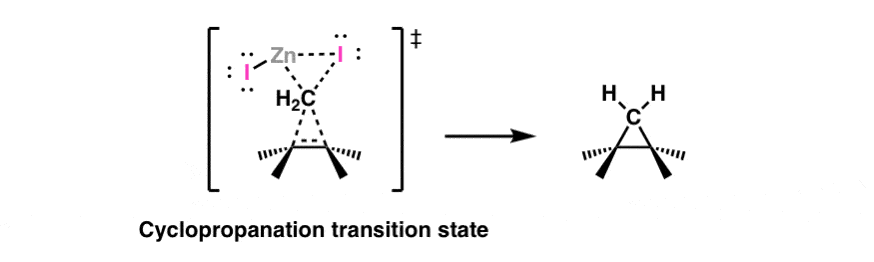
6.烯烃与氯仿和碱的二氯环丙烷化反应(给二氯苯)
当用强碱处理时,氯仿(CHCl3.)是去质子化的共轭碱.从这个物种中氯离子的损失导致Cl2C:又称“二氯苯”。在上面的反应中,烯烃加到碳烯上得到环丙烷。反应通过这个过渡态进行(空的p轨道和包含孤对电子的轨道叶没有显示出来)
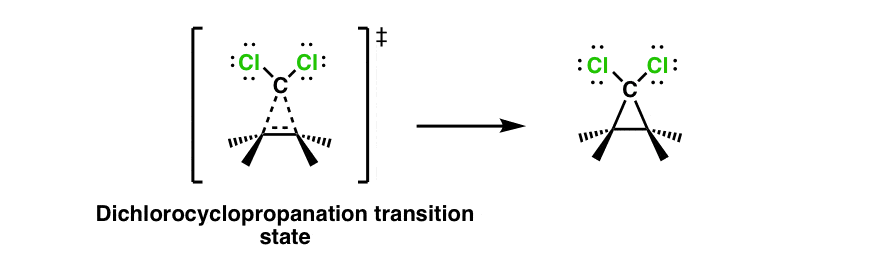
7.烯烃加成反应中的协同途径
总之,这篇文章中的每一个反应都是通过一个协调一致的过渡态给出产物syn立体化学。立体化学烯烃被保存在立体化学的产物中(即它们都是立体定向反应)。区域化学在这些情况下都不相关除了硼氢化反应,这是anti-Markovnikov.
那么我们如何画出这些反应的推箭机制呢?问得好!在下一篇文章中会有更多关于这个困境的内容。
笔记
注1:这假设使用了“多相”催化剂,如Pd/C、Pt/C等,这些催化剂不是溶解在溶液中,而是悬浮在溶液中。氢化也有“均相”催化剂,如威尔金森的催化剂.由于这种试剂涉及到d区金属的机理,本博客不打算深入讨论。[但迈克喜欢!]
(高级)参考资料和进一步阅读
Simmons-Smith反应:
- 不饱和化合物中的环丙烷,亚甲基碘化物和锌铜偶
西蒙斯,h.e.;凯恩斯,t.l.;弗拉杜奇克;你好,美国。反应1973年,1 - 133
DOI:10.1002/0471264180. or020.01
本章有机反应有你需要知道的关于西蒙斯-史密斯反应的一切,包括机理研究,实验程序,和底物范围。 - NORCARANE
D.史密斯和H. E.西蒙斯
Org。Synth。1961,41, 72年
DOI:10.15227 / orgsyn.041.0072
的西蒙斯-史密斯反应的详细程序有机合成,包括Zn-Cu偶对的制备。氯化碳二氯环丙烷化2: - 二氯苯的加入烯烃
威廉·冯·多林和a·肯塔罗·霍夫曼
美国化学学会杂志195476(23), 6162 - 6165
DOI:10.1021 / ja01652a087
原论文描述了从二氯环丙烷的合成烯烃氯仿和KOtBu,由传奇人物威廉·冯·埃格斯·多林制作。 - 1, 6-Methano[10]轮烯
E.沃格尔,W.克鲁格和A.布鲁尔
Org。Synth。197454, 11
DOI:10.15227 / orgsyn.054.0011
本程序的第二步是合成二氯环丙烷,方法是将二氯苯加到二氯环丙烷上烯烃.Dihydroxylation的烯烃与KMnO4: - 高锰酸钾在中性溶液中氧化油酸制备9(10),10(9)-酮羟基硬脂酸的改进
约瑟夫·e·科尔曼,c·里丘蒂,丹尼尔·斯维恩
美国化学学会杂志1956年,78(20), 5342 - 5345
DOI:1021 / ja01601a050 - 高锰酸盐氧化机理。的羟基化作用烯烃及相关反应
Kenneth B. Wiberg和Klaus A. Saegebarth
美国化学学会杂志1957年,79(11), 2822 - 2824
DOI:1021 / ja01568a042
二羟基化的机理研究烯烃与KMnO4.第一篇论文也是由斯维恩氧化的斯维恩驰名!KMnO的缺点4它会使底物过度氧化,产生酮。在碱性溶液中进行氧化可以最大限度地减少这种情况。 - dl-GLYCERALDEHYDE乙缩醛
维策曼,Wm。劳埃德·埃文斯,亨利·哈斯,e·f·施罗德
Org。Synth。1931,11, 52岁
DOI:10.15227 / orgsyn.011.0052
an二羟基化的典型过程烯烃与KMnO4.这个过程突出了使用KMnO的困难之一4氧化;尽管它很便宜,但以化学计量量使用它会形成等量的MnO2,很难从理想的产品中分离出来。Dihydroxylation的烯烃与OsO4: - 锇Tetraoxide独联体不饱和底物的羟基化
施罗德,M。
化学。牧师。198080, 187年
DOI:10.1021 / cr60324a003
本文就二羟基化的机理作一综述烯烃通过OsO4(包括催化和化学计量变体),说明了各种Os配合物,并描述了反应的底物范围。 - 催化四氧化锇的氧化烯烃:独联体1, 2-CYCLOHEXANEDIOL
范雷宁,查达镛,W. M.哈特利
有机合成,科尔。第6卷,第342页(1988);第58卷,第43页(1978)。
DOI:10.1021 / orgsyn.058.0043
一种可靠的Upjohn二羟基化方法有机合成.请注意,这个名字来自密歇根州卡拉马祖的Upjohn公司(后来被辉瑞收购),这是它最初被开发的地方。环氧化作用的烯烃与米CPBA: - 间氯过苯甲酸环氧化反应
Nelson N. Schwartz和John H. blumberg
有机化学杂志196429(7), 1976 - 1979
DOI:1021 / jo01030a078
本文介绍了有关的机理研究米-CPBA表明离子中间体不参与反应,反应速率对溶剂极性不敏感的氧化反应。 - 环氧化过渡态的实验几何
Daniel A. Singleton, Steven R. Merrigan,刘健,K. N. Houk
美国化学学会杂志1997119(14), 3385 - 3386
DOI:1021 / ja963656u
结合实验和理论研究环氧化过渡态,表明两者C-O键形成事件几乎同步。 - 环氧化的机理烯烃通过高酸
V. G.德鲁克
四面体体积32第23期1976第2855-2866页
DOI:10.1016 / 0040 - 4020 (76) 80137 - 8
叙述了作者在环氧化反应动力学研究方面的工作烯烃用过酸来确定确切的机理。
你确定烯烃和炔烃的氢化反应是一致的吗?
第一步,将氢和钯添加到多个键上(氢钯化)。第二步(还原性消除)保留了碳的立体化学。由于氢化反应通常超出了有机化学入门的范围,因此说氢化反应是一致的并不过分。
伟大的网站。我经常读书已经有一段时间了。非常有用和清晰的内容。非常喜欢,先生!