烯醇和烯醇酯
Keto-Enol互变现象
最后更新:2022年9月21日|
酮烯醇互变异构现象
许多酮和醛都有另一个自我"烯醇的形式,其化学性质与我们熟悉的“酮”形式完全不同。在这篇文章中,我们将探索这种结构和性质。烯醇"形式,通过酮的反应机制烯醇并描述了一些影响酮-的关键因素烯醇平衡。
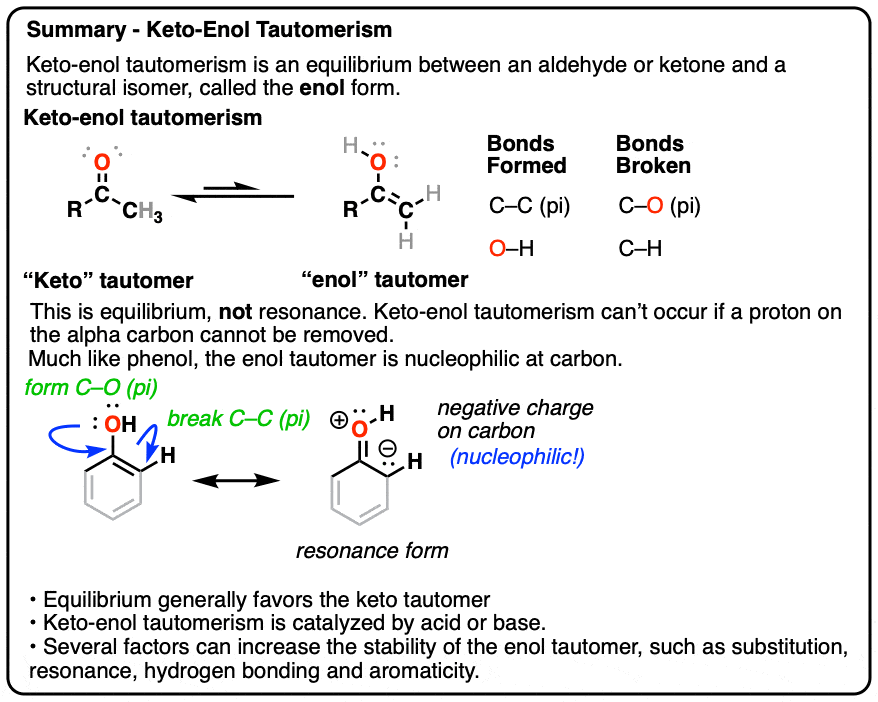
*主要是醛和酮,尽管它也可以发生在其他物种中(例如酸卤化物)
注:这是一篇题为“Keto-”的旧文章的2022年更新烯醇互变异构:关键点.
目录
- 当酮成为亲核试剂
- Keto-Enol互变现象
- 酮烯醇互变异构的例子
- 烯醇的性质
- 酮烯醇互变异构:机制
- 影响酮烯醇平衡的四个因素
- 因素1:替代
- 因素2:共轭/共振
- 因素3:氢键
- 因素4:芳香性
- 重温一个奇怪的“非酮类”反应
- 总结与结论
- 笔记
- 测试你自己!
- (高级)参考资料和进一步阅读
1.当酮成为亲核试剂
醛和酮的反应:到目前为止,我们已经都看过了。对吧?
我的意思是羰基醛和酮的碳是亲电试剂.所以他们的反应或多或少都遵循相同的模式。
- 一个亲核试剂攻击碳,形成C-Nu,打破C-O键,生成an醇盐(O- - - - - -)这是亲核加成。
- 加入温和的酸使其质子化醇盐形成O-H。(参见:醛和酮- 14相同机理的反应]
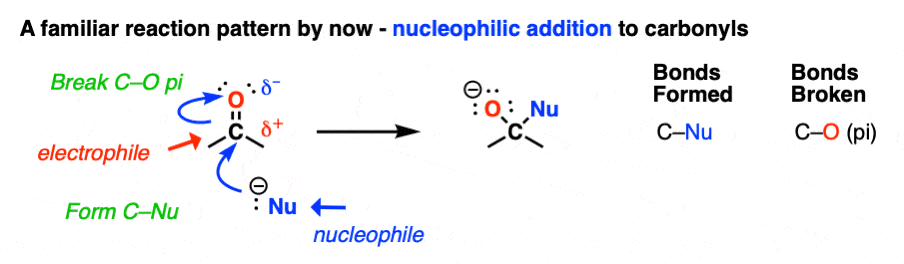
这就是醛酮反应的全部内容。情况下关闭?
不完全是。在这篇文章中,我们发现醛和酮有双重生命.

白天,它们是可观的亲电试剂,与亲核试剂加在一起。但到了晚上,也许在月圆之时,它们会转变成完全不同的野兽——具有不同的结构、属性欲望.
这里有一个反应的例子,它不符合正常的“两步”模式。治疗酮酸和溴2给……一个新的碳溴键羰基碳呢?
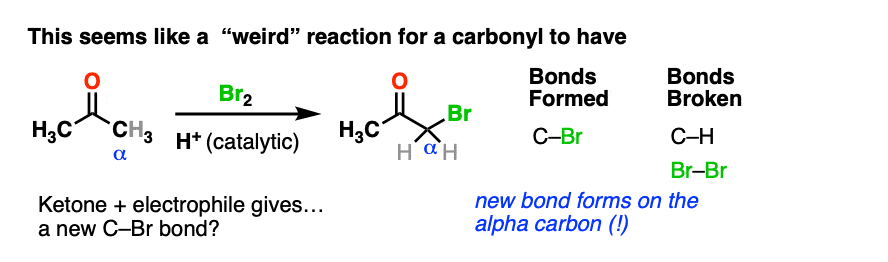
这似乎是肯定的联合国-酮的地方。回忆一下Br2是亲电的(记住它是如何反应的富电子烯烃而且芳香环).
w我们的"亲电性"到底是什么酮和另一个人在一起嬉戏亲电试剂?在....上形成化学键一个完全不同的地方?
2.Keto-Enol互变现象
这种异常化学行为的线索不是由变狼癖提供的,而是由其中含有许多醛和酮的事实提供的平衡一种结构异构体叫做烯醇形式(部分碱烯,部分酒精ol).
这种行为被称为酮烯醇互变异构现象.
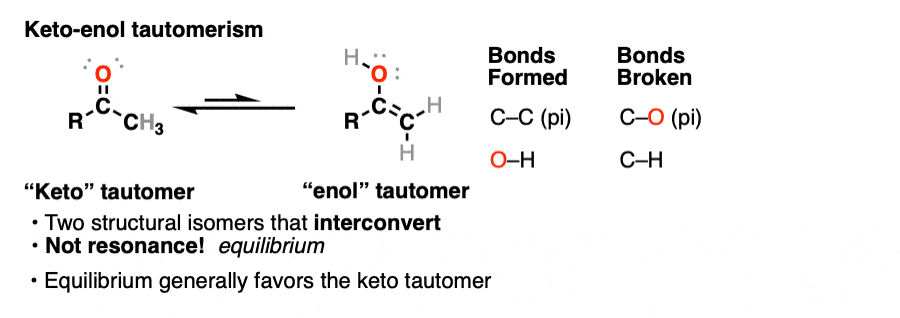
酮和烯醇形式是不共振形式![注1他们是结构同分异构体它们可以相互转换。这个属性叫做互变异构现象.酮烯醇互变异构是最常见的互变异构类型,尽管还有其他类型。[注2]
这意味着酮和烯醇不同的形式,如果分离,具有非常不同的物理和化学性质,这一点马上就会变得很重要。[注3]
实际上我们遇到过酮烯醇之前讲过互变异构。你们可能还记得炔烃用HgSO处理4水给了烯醇中间产物,然后互变异构成a酮.同样的,炔烃经过硼氢化氧化得到烯醇,烯醇可以互变性成醛。[看到炔的硼氢化和氧汞化反应]
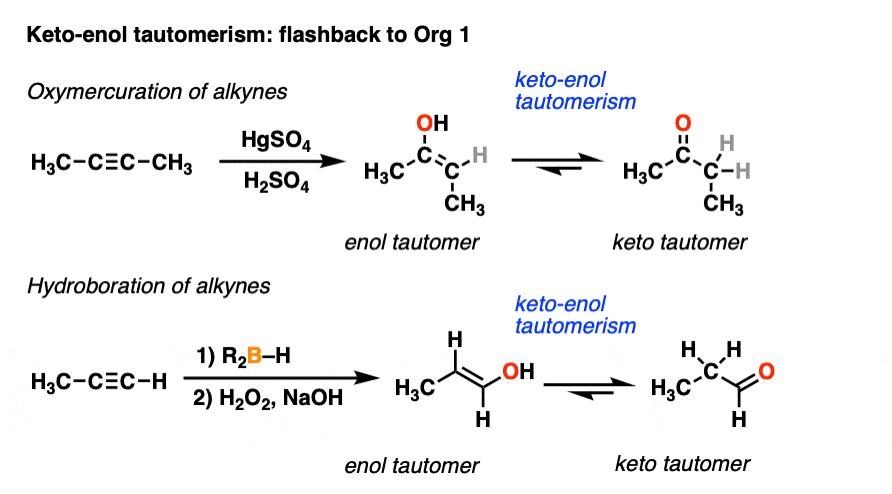
你的导师可能在那个时候掩盖了互变异构的部分,说一些类似于“你会在组织2学到更多关于这个的东西。”好吧,这个时刻已经到来。
3.酮-烯醇互变异构的一些例子
这里还有一些酮的例子烯醇互变现象。
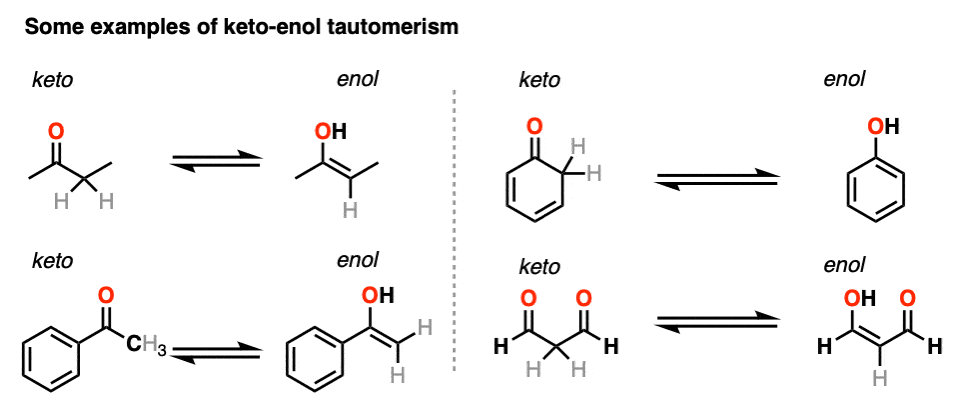
你们可能还记得一开始我说过酮烯醇互变异构发生在一些醛和酮。为什么是“一些”而不是“全部”?因为它不可能在没有氢的情况下发生α碳.[注意4]
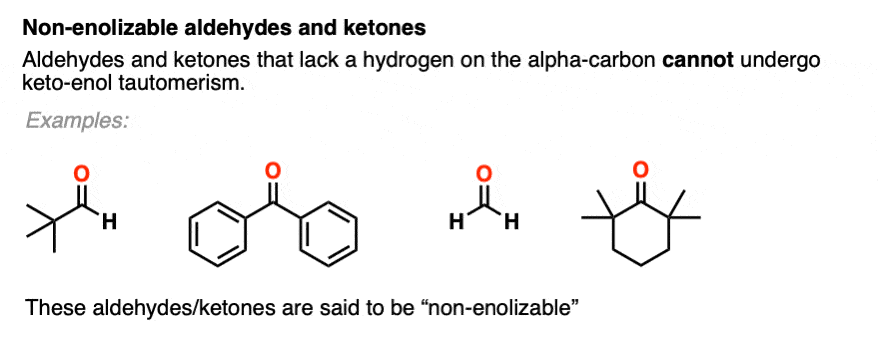
这些醛和酮被称为“非”enolizable"醛和酮。
4.烯醇的性质
可能这烯醇我们刚才说的醛和酮的那些“奇怪”反应是由什么引起的呢?
[旁白:你觉得呢? ?不然他为什么要提这个?]
仔细看看烯醇形式可以帮助我们理解它的一些性质。
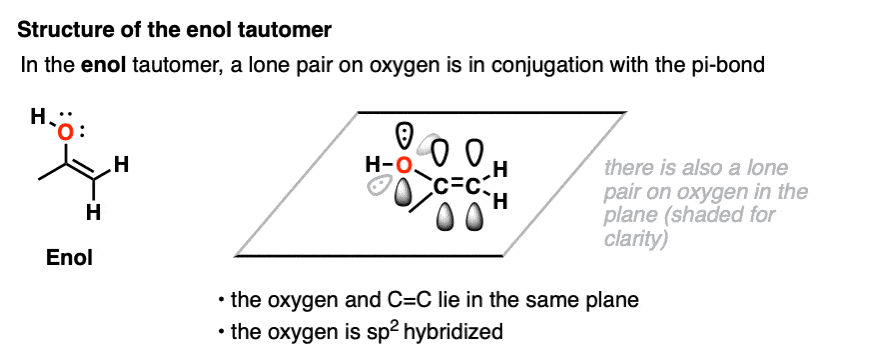
乍一看,我们可能认为有一个带电负性的氧连在an上烯烃可能会让它的电子更少,因为它通过C-O键吸走了电子密度。
但是,我们也可以画出一个共振形式,氧上的孤对连着π键捐赠一对电子朝向环,形成一个新的C-O键。
在这个过程中,碳碳键上的电子对移动到相邻碳上成为孤电子对。
这被称为pi-donation它的作用是使PI键更富电子,因此更多的亲核。[看到帖子:Pi-Donation]
总的来说,pi-donation来自氧气的影响往往是更强大的而不是由电负性引起的感应效应。
你可能还记得OH是a强烈激活亲电芳香族取代基团。(参见:激活和取消激活组你可能还记得画出的共振形式,它显示了电子密度向昊图公司-而且帕拉-的位置。
如果你还记得,我有个好消息。烯醇的行为完全相同!
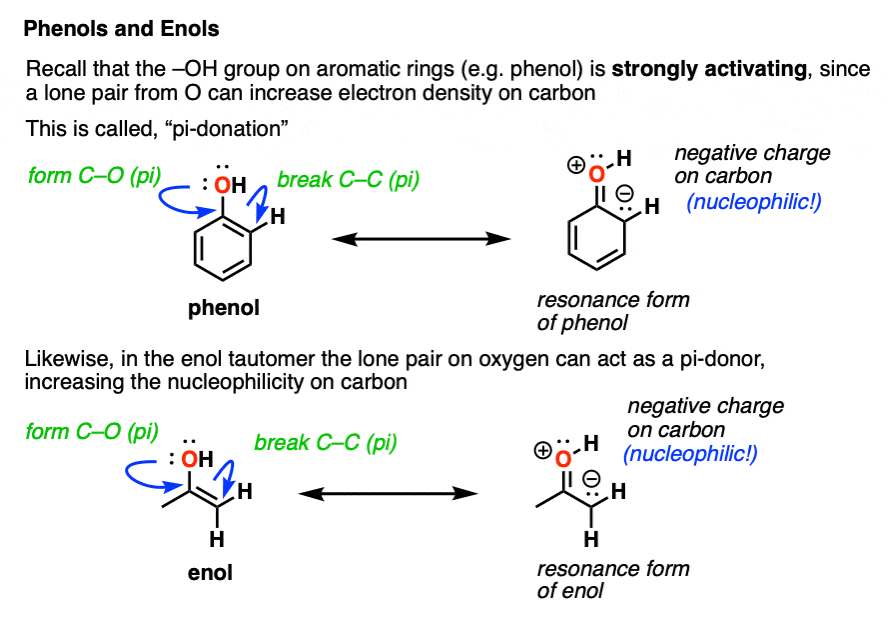
一个附着的-OH基团可以使碳氧键附近的碳更富电子,因此更亲核!
这有助于解开为什么新的C-Br键形成于“α碳在我们上面的例子中。在一个烯醇,α碳是强亲核的!
5.酮烯醇互变异构:机制
这引出了一个问题。如果酮和烯醇互变异构体不是共振形式,那么一定存在某种相互转换的过程。那么这是怎么发生的呢?
展示如何做这件事可能会有启发意义错误的方式第一。
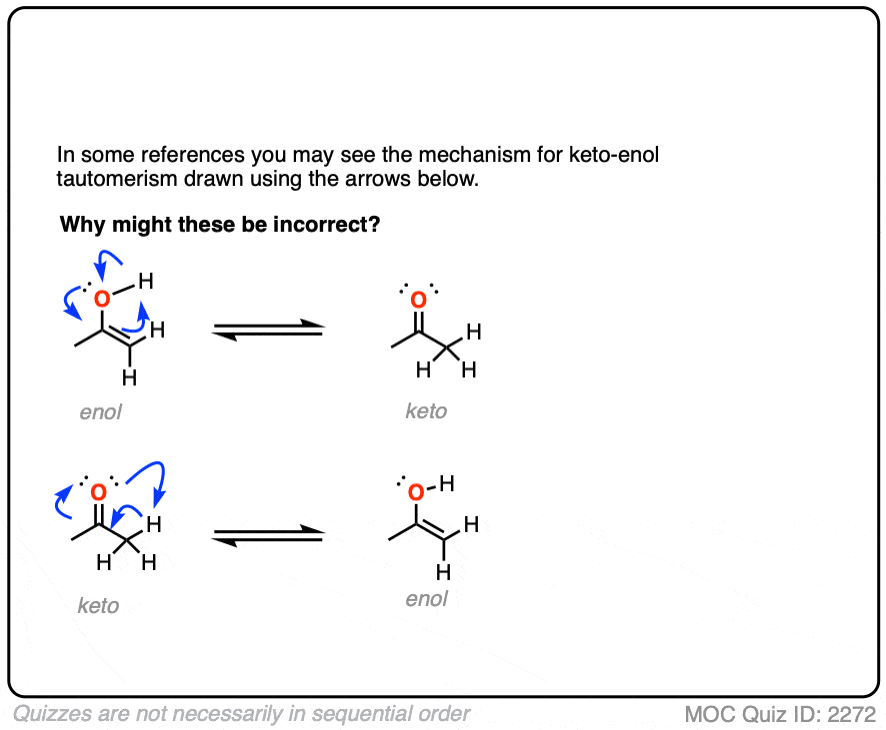 点击翻转
点击翻转
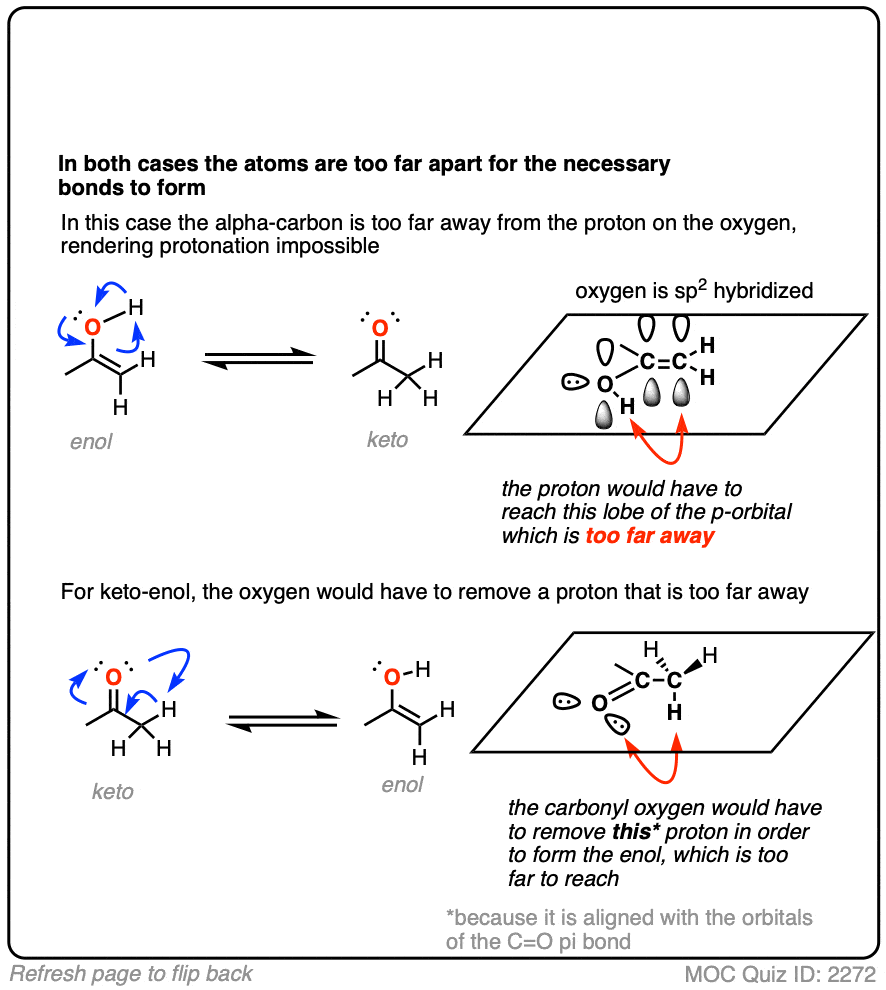
等一等。它看起来太糟糕了诱人的把它作为一个协调一致的过程来制定。这怎么可能是错的?
这是错误的,就像你不能用左手抓你的左肘部一样。它们相距太远,无法接触。
所需要的是一个“辅助”分子来将质子从分子的一部分运输到另一部分。水很好。[注5]
除了水,酮的相互转化和烯醇互变异构体酸或碱的存在极大地辅助。[注6]
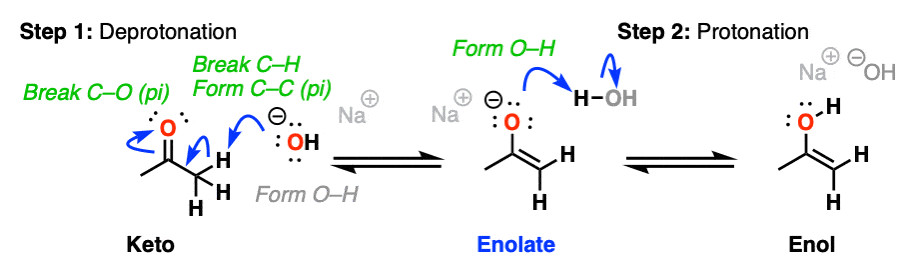
在酸的存在下羰基氧被质子化(步骤1,形成O-H)。然后,在缓慢的一步,α碳是去质子的烯醇(第二步,打破C-H,形成C-C (pi),打破C-O (pi)。).这给了我们烯醇.
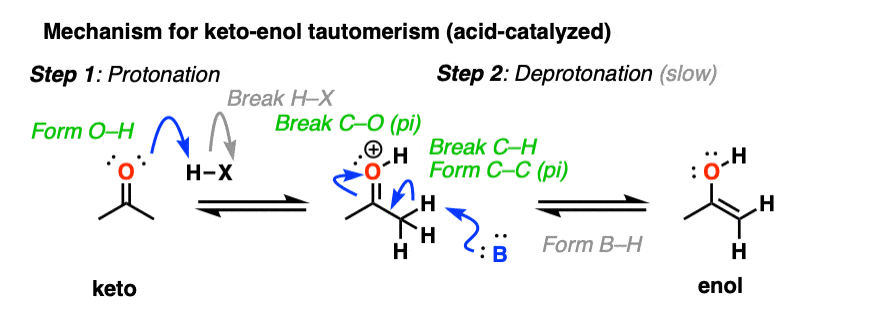
用于酸催化转化烯醇酮,徘徊在这里然后会弹出一张图片或者点击这个链接.
酮烯醇碱也有助于相互转化。这里,去质子化α碳(步骤1,打破C-H,形成C-C (pi),打破C-O pi)是慢步骤,氧的质子化(步骤2,形成O-H)是快步骤。
6.影响酮烯醇平衡的四个因素
对于大多数醛和酮来说,平衡态强烈倾向于酮态,通常是酮态的10倍4或者更多。这主要与键强度的差异有关(C-O pi是比C-C pi更强的键,详情见请注意7).的烯醇对于羧酸和酯类.[注8]
也就是说,至少有4个关键因素可以显著影响酮:烯醇比率。了解它们很重要,因为它们是很好的考试材料。
它们的影响力从弱到强依次为:
因素1:替代
还记得扎伊采夫规则?消元化倾向于形成更多的取代基烯烃,因为它们在热力学上更稳定?(参见:烯烃的稳定性]
同样的趋势也适用于烯醇!
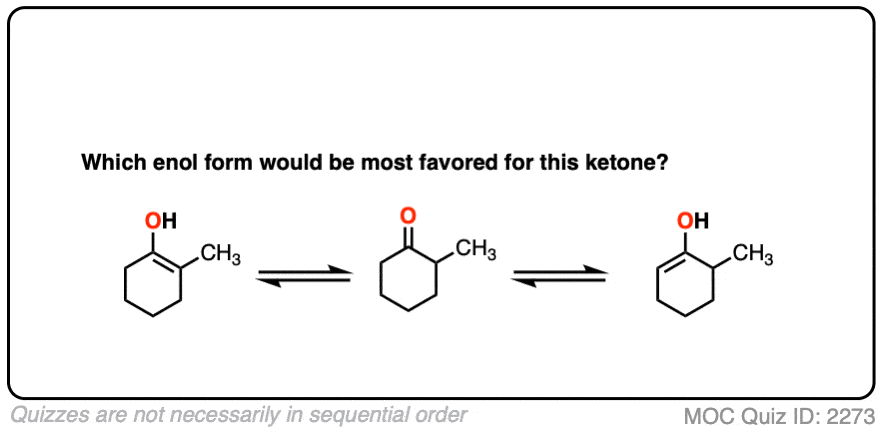
例如,烯醇你认为它在平衡时更有利吗?
 点击翻转
点击翻转
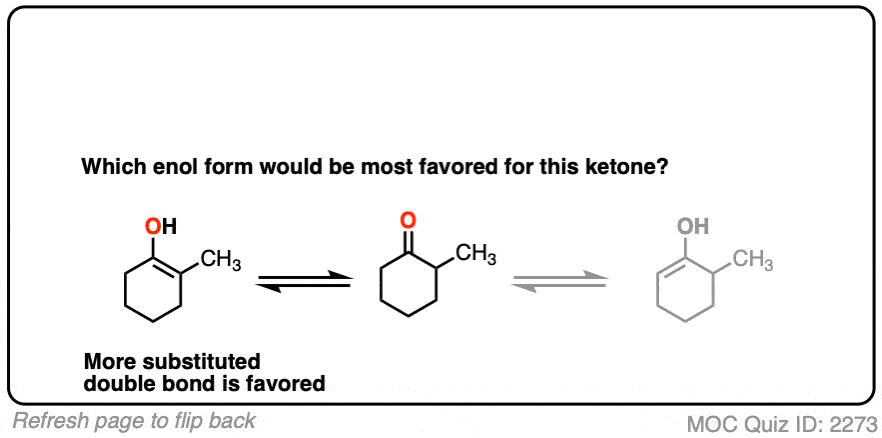
取代的越多烯醇它的热力学稳定性就越高。这种差异通常并不大(1-2千卡/摩尔),但回想一下,即使1千卡/摩尔的差异也意味着平衡比例约为80:20。[计算在这里]
(这实际上是一个需要注意的重要趋势,因为你可能很快就会形成对比动力学烯醇和热力学烯醇.)
比较下面的稳定性醛烯醇:
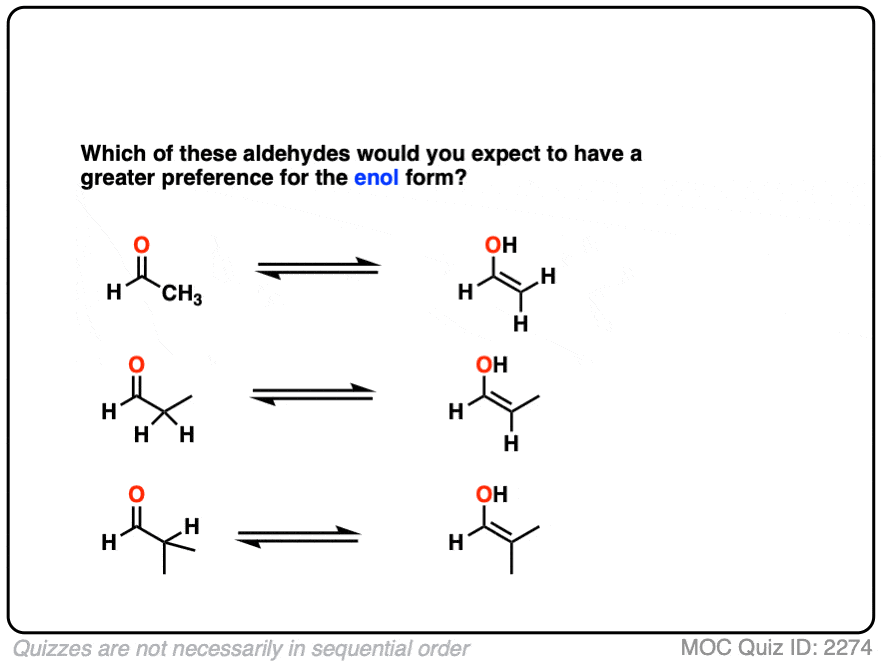 点击翻转
点击翻转
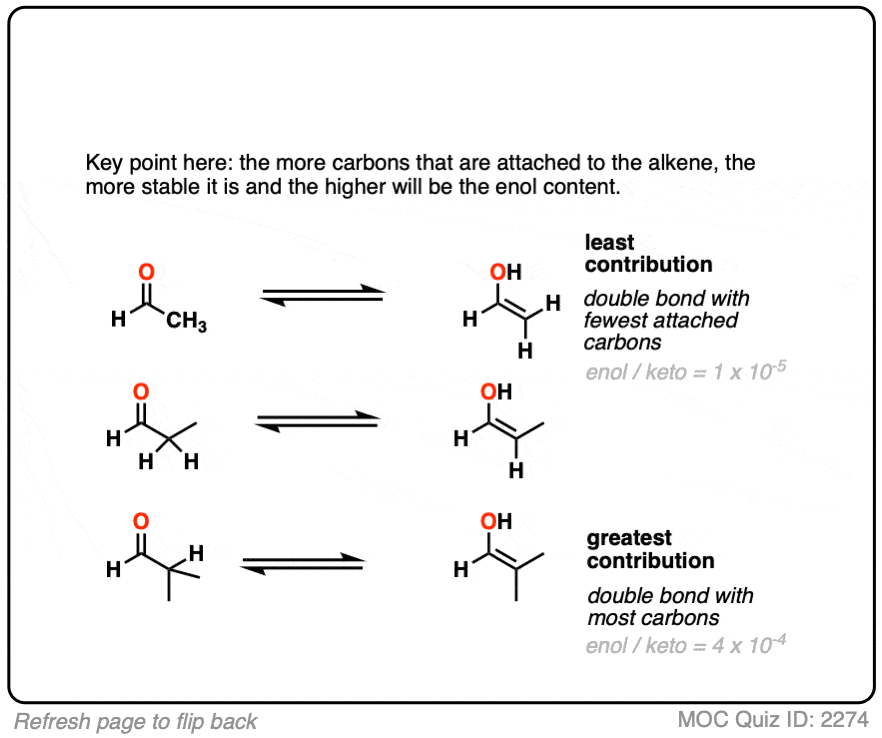
因素2:共轭/共振
π键有点像牛奶中的Cheerios:它们连接在一起比孤立地悬挂更稳定。
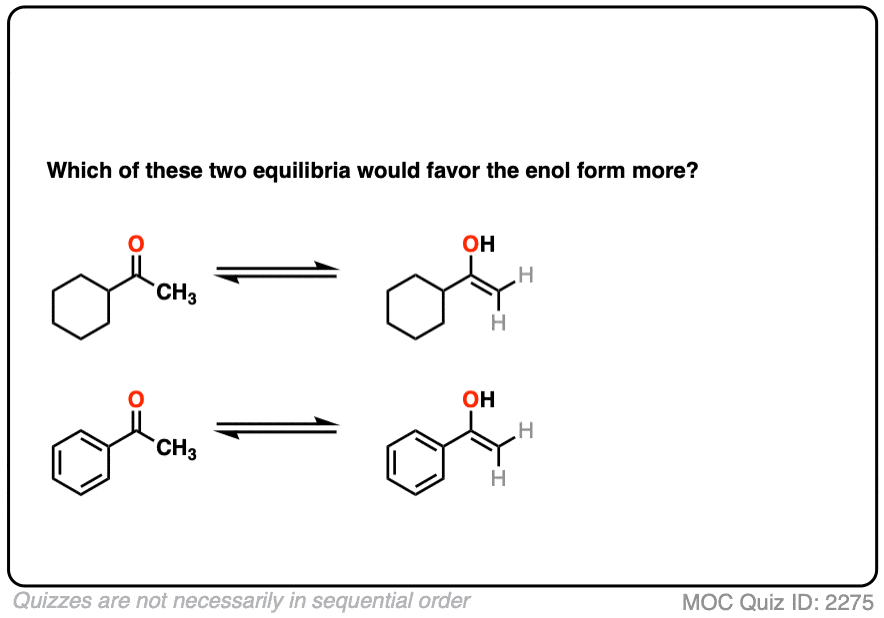
这就引出了一个问题这两个酮中哪一个更倾向于烯醇形式?
 点击翻转
点击翻转
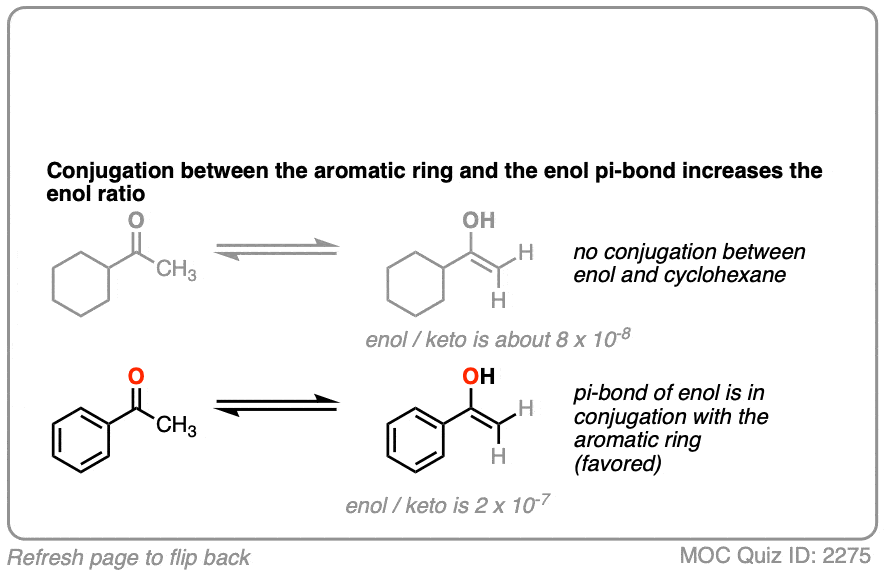
越有利烯醇形式将允许共轭与相邻的PI系统。
因素# 3:氢键
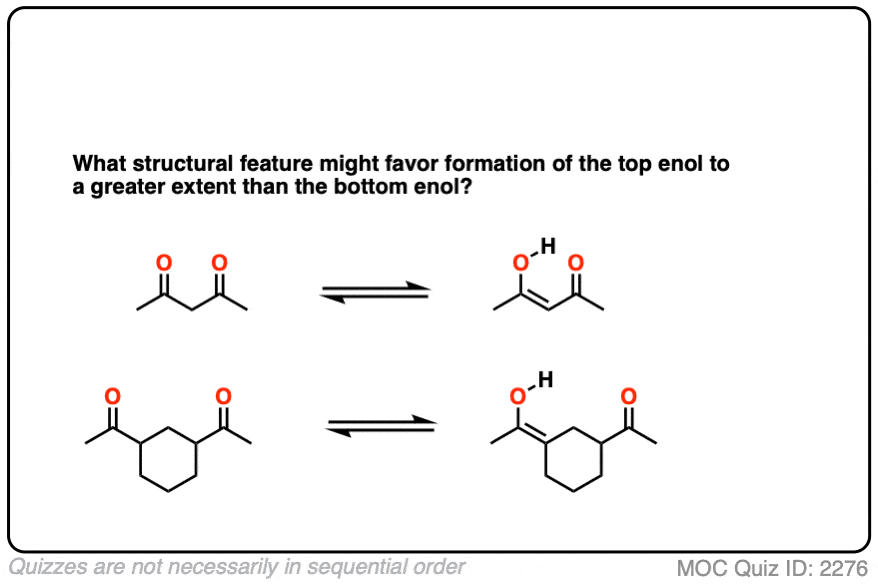
这是一个有趣的问题。烯醇有一个O-H键,高度极化;氢带部分正电荷,能形成氢键。如果一个路易斯碱(例如a的氧羰基)在附近存在,则会产生分子内氢键,从而稳定烯醇的形式。
 点击翻转
点击翻转
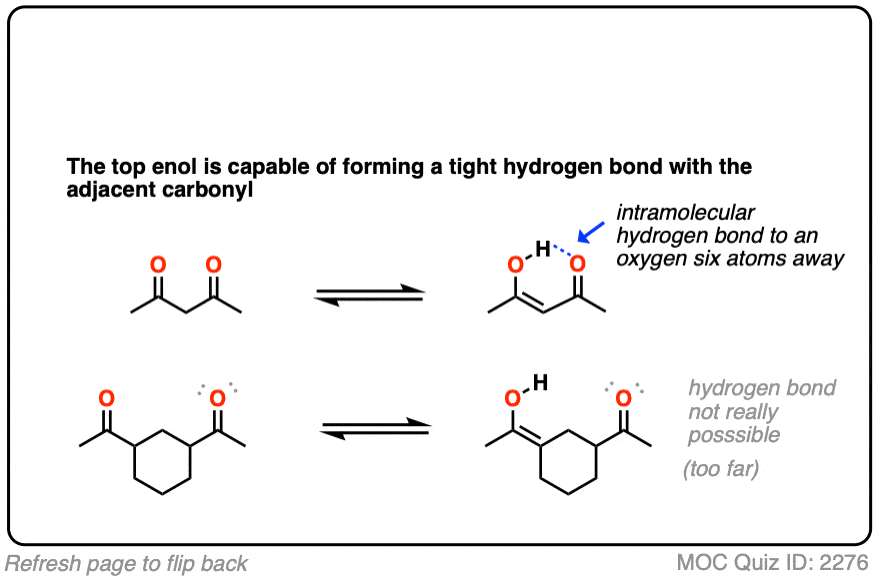
的比例在某些情况下烯醇形式可以等于或甚至大于溶液中酮互变异构体的量。
(例如,2,4-戊二酮的核磁共振谱显示酮和戊二酮约1:1的混合物烯醇互变异构体)悬停图像
[这和溶剂有关.看到注意9]
因素4:芳香性
最强大的推动力是支持烯醇互变异构体是芳香性.
对比这两个酮。这将有利于烯醇互变异构体更多?
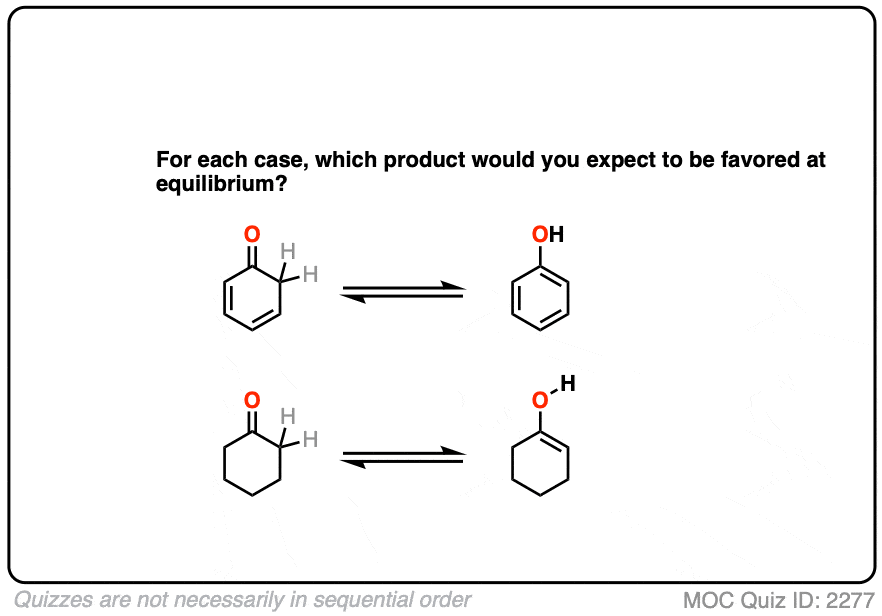 点击翻转
点击翻转
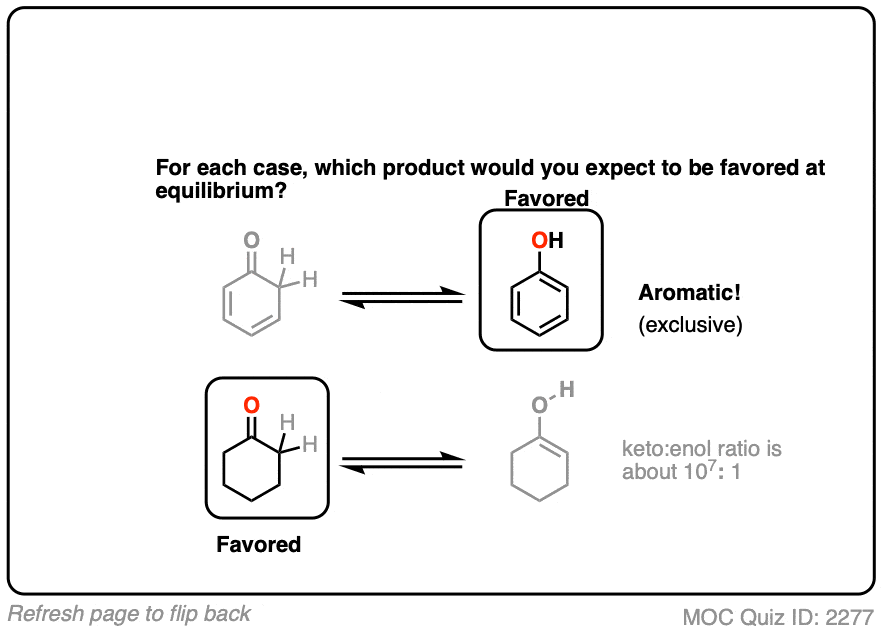
希望你能看到苯酚的芳香性(其共振能量为>20千卡/摩尔)极大地有利于烯醇形式。酮互变体在溶液中检测不到!
11.与Br的“非酮样”反应2
在我们探索了这么多之后,我想我们已经准备好回到这个“奇怪”的反应酮再来一次。
这种反应是如何发生的呢?
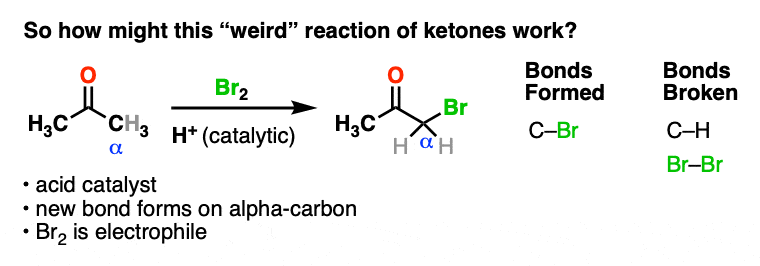
我们加入酸,形成一个新的键到亲电试剂在α碳.我想我们可以肯定地说第一步是酸催化的酮烯醇互变现象。
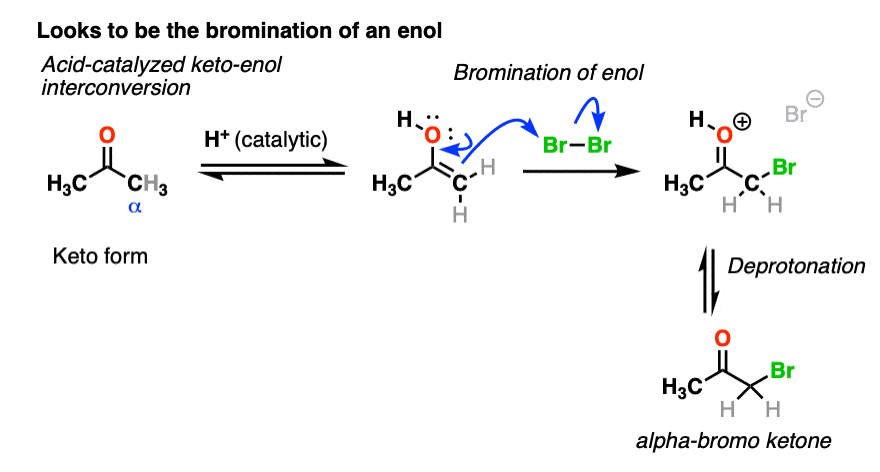
这给了我们一个亲核试剂烯醇,然后与Br反应2形成新的碳溴键。去质子作用会产生中性的-溴酮.
12.总结与结论
那么我们学到了什么呢?
- 有一个质子的醛和酮α碳可以参加酮烯醇互变异构现象,其中两个结构异构体之间存在平衡-酮和烯醇形式。处于平衡状态的结构异构体被称为"互变异构体”。
- 的烯醇互变异构体是亲核在C-OH键附近的碳上(α碳),并与亲电试剂发生反应
- 酮烯醇互变异构可以用酸或碱催化。
- 一般来说酮互变异构体在平衡时是有利的。
- 许多结构性因素稳定烯烃如替换,动词的词形变化,以及参与芳环也可能有助于稳定烯醇的形式。此外,烯醇互变异构体可以被相邻的氢键受体(如a酮)
笔记
有代表性的酮烯醇比率(从Carey & Sundberg而且三月份的高级有机化学)
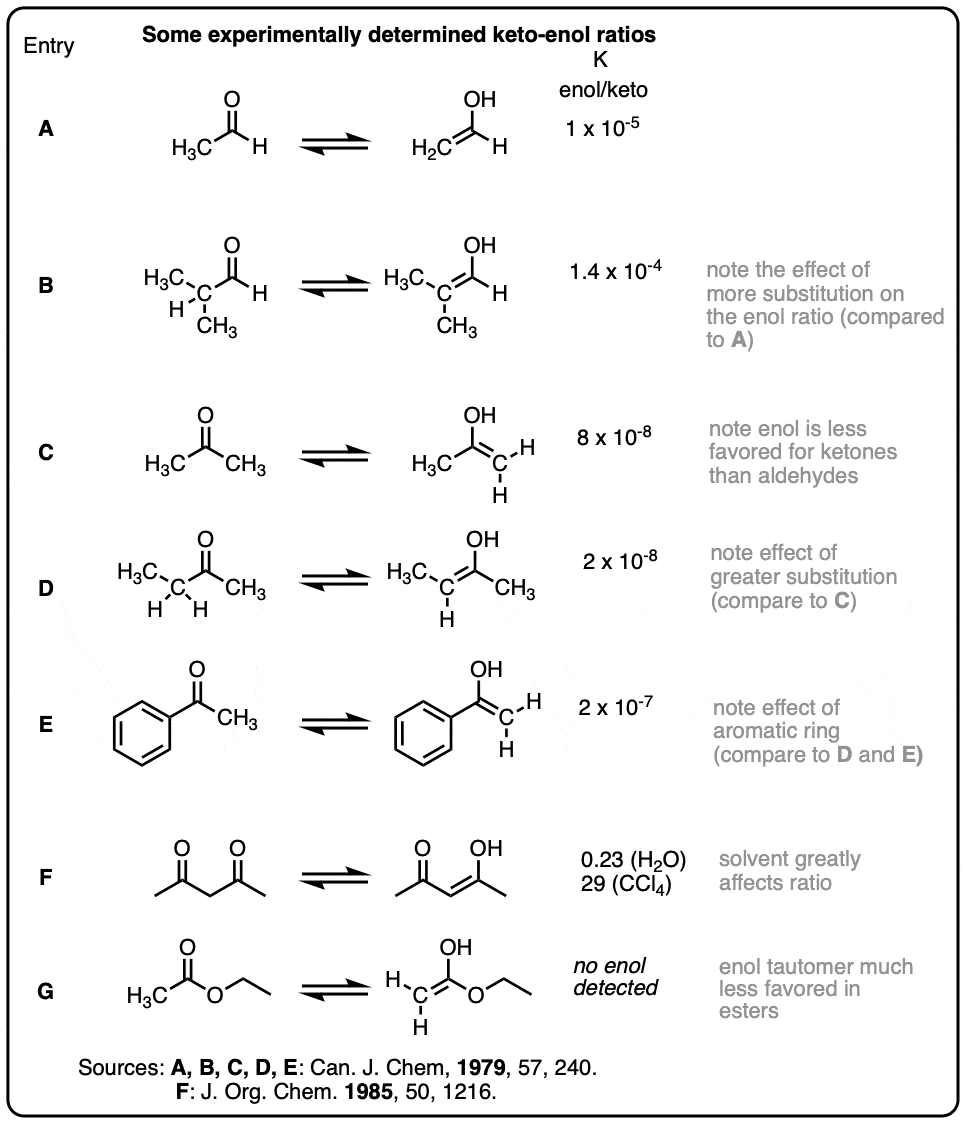
注1回想一下,共振形式彼此之间不是平衡的——它们只是表示分子中π电子分布的方式,而分子的真实结构最好被认为是共振形式的加权混合。(参见:共振结构]
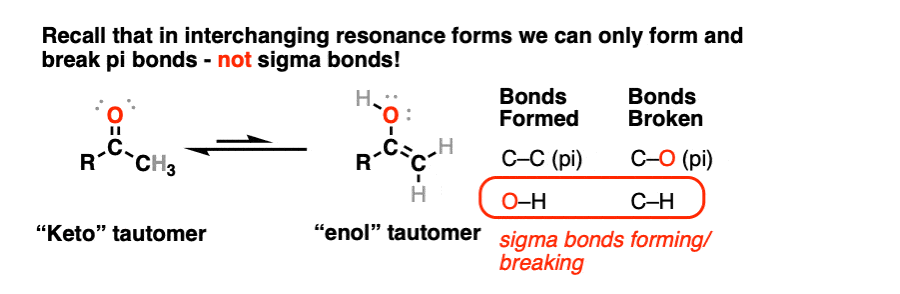
酮变成an的过程烯醇-形式,C-H sigma键和C-O键断裂,O-H sigma键和C-C键形成。这就是为什么它们不是共振形式的另一个原因我们不能打破键来转换共振结构.
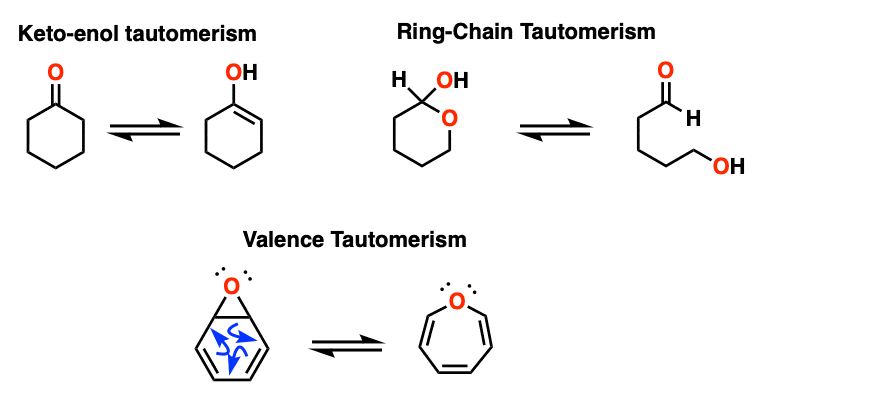
注2 -酮烯醇互变异构是互变异构最突出的类型之一。Ring-chain互变现象这种情况经常发生在糖中,是另一个原因。(参见:糖中的环链互变异构].第三种是价互变,它发生在某些缺乏固定结构的分子中。
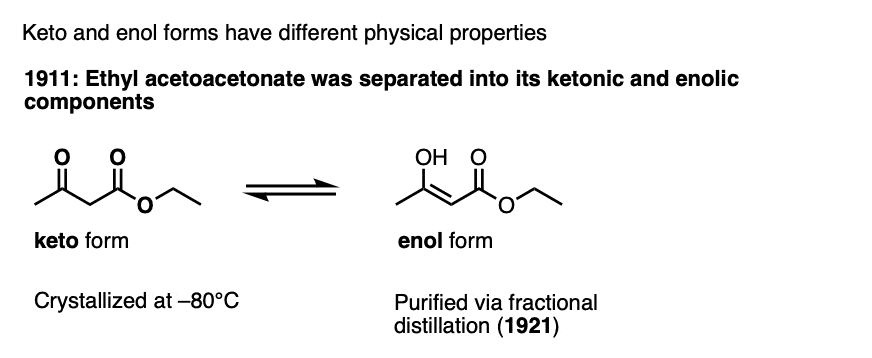
注3-酮和烯醇某些酮的形式已被分离。第一个例子是乙酯。
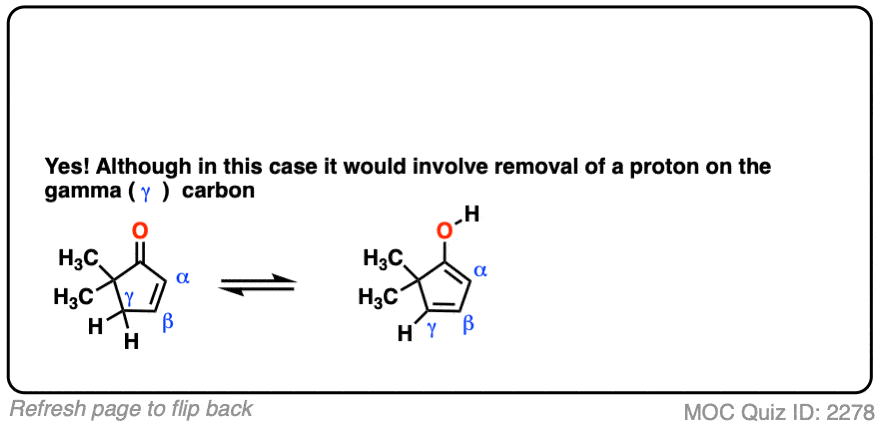
注4 -有可能某些α, β不饱和酮出现“非enolizable"在γ位置被烯化。
 点击翻转
点击翻转
请注意5 -在某些情况下,可以制备“纯”烯醇,不受其酮互变异构体的污染。在这些情况下,研究人员非常小心地排除了水,水可能作为“质子穿梭器”相互转换烯醇酮酮形式。
注6 -看到Ref 1有关酸如何加速酮的生成速度的更多细节烯醇互变现象。
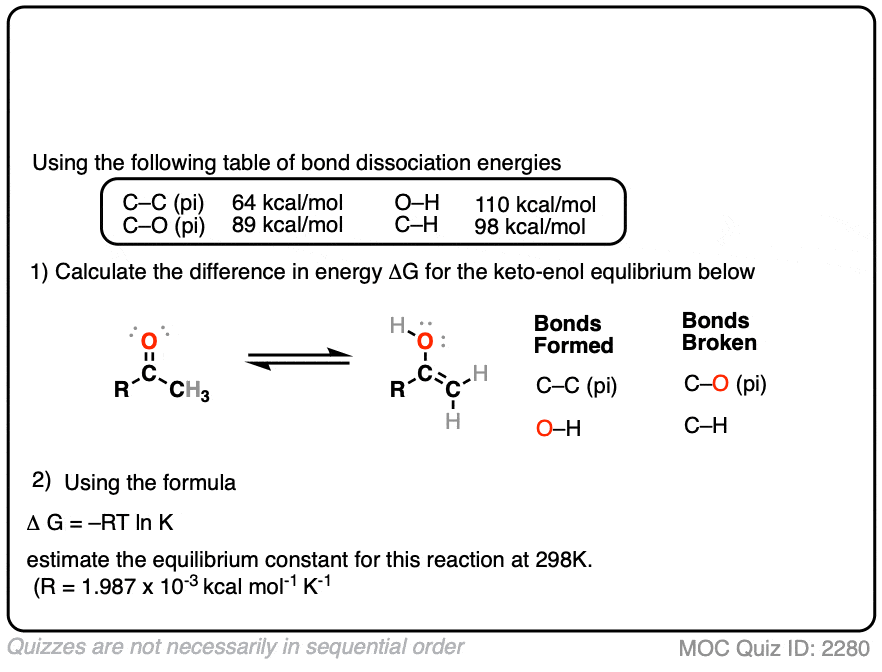
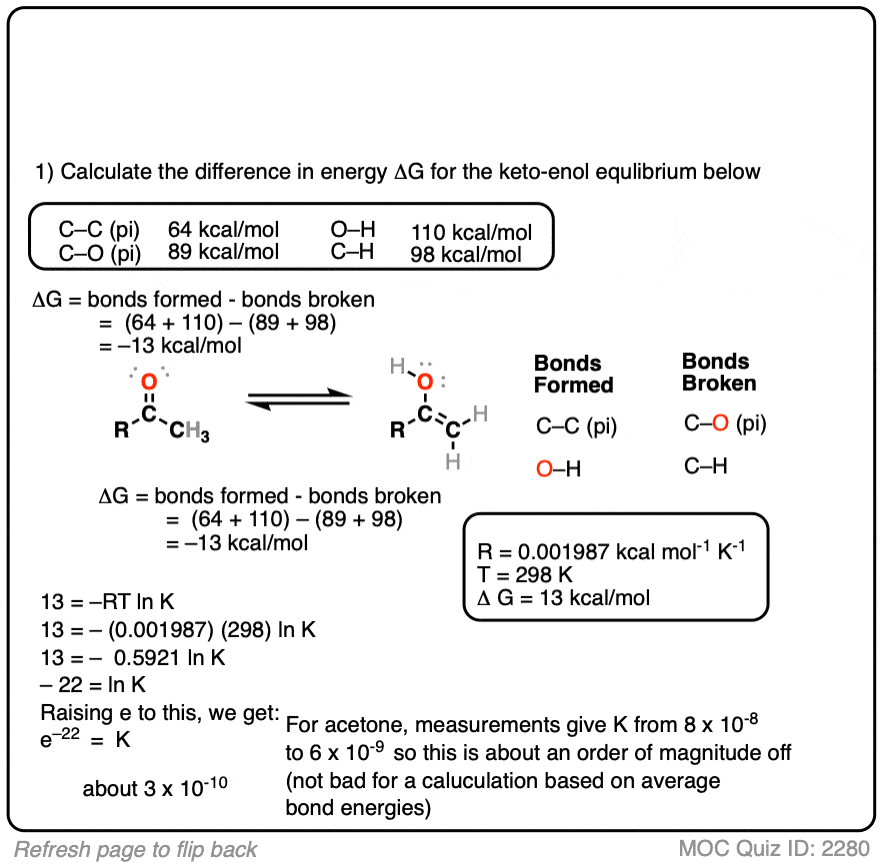
注7 -使用键解离能的平均值对形成和断开的键进行快速制表,显示酮和酮之间至少有10千卡/摩尔的差异烯醇互变异构体大多数情况下更倾向于酮类。看到这个测试举个例子。
注8。的比例烯醇在乙酸乙酯溶液中发现的互变异构体小于千万分之一——比酮的发现低几个数量级。
注意9。酮有一定的溶剂依赖性烯醇比率。在非氢键溶剂(如四氯化碳)中烯醇乙酰乙酸乙酯的酮比测定为98:2左右。然而,在像水这样的氢键溶剂中,在接受氢键方面存在更多的“竞争”烯醇:酮比降至约1:4。(见Ref 5)
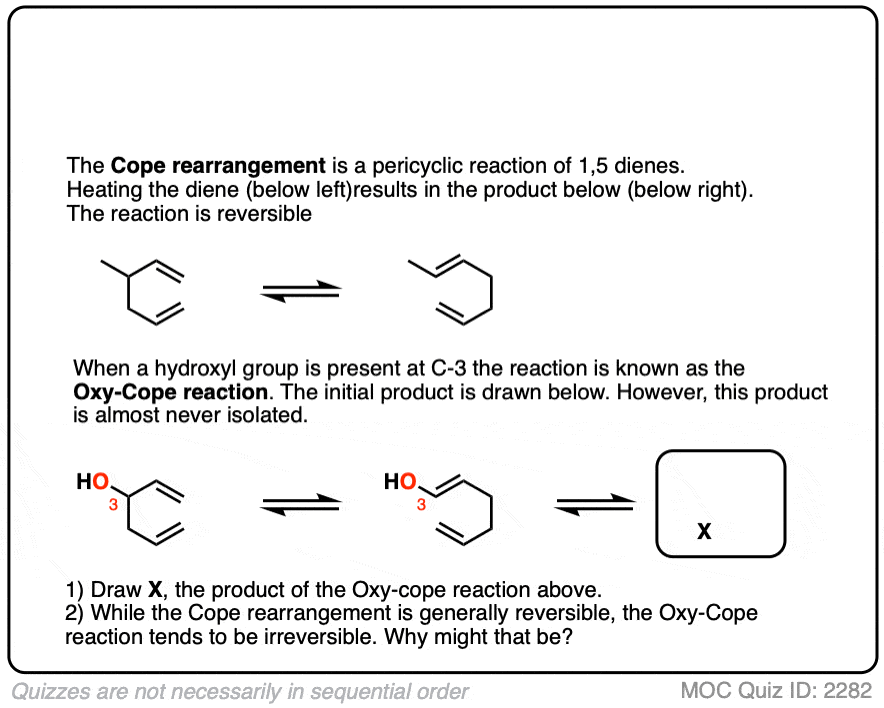
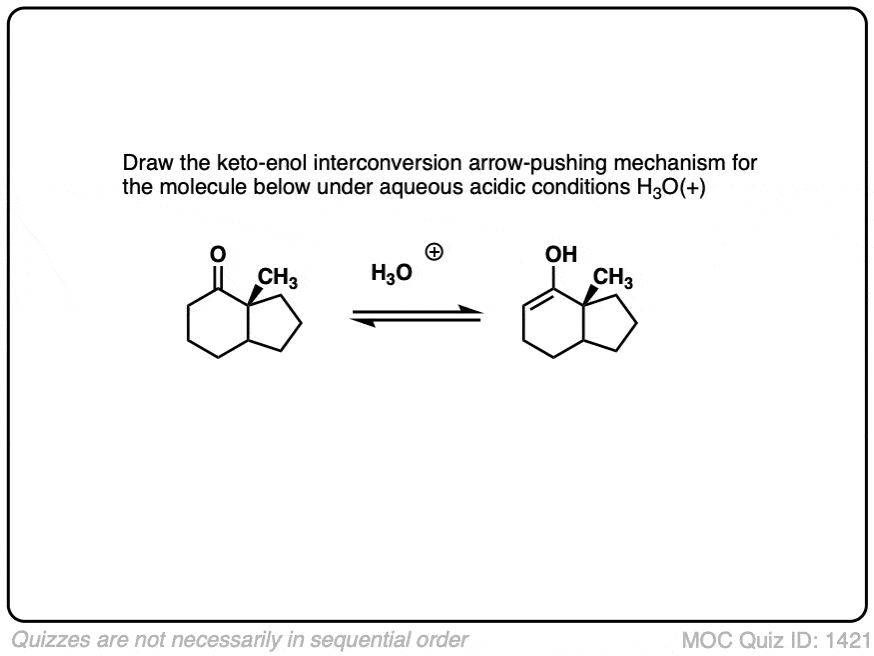
测试你自己!
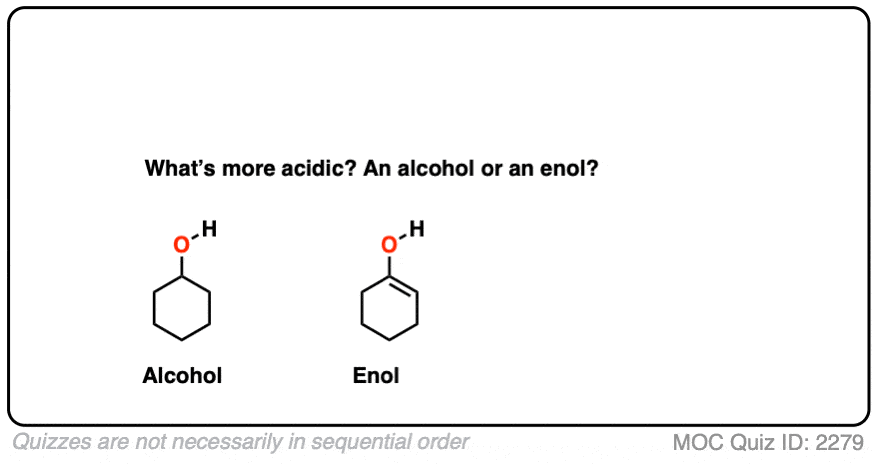 点击翻转
点击翻转
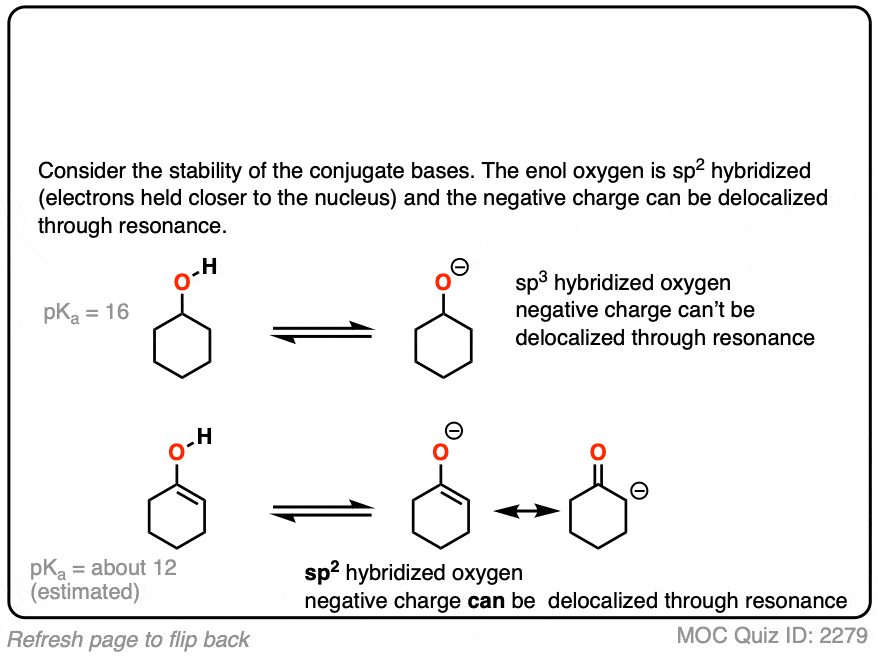
 点击翻转
点击翻转
 点击翻转
点击翻转
 点击翻转
点击翻转
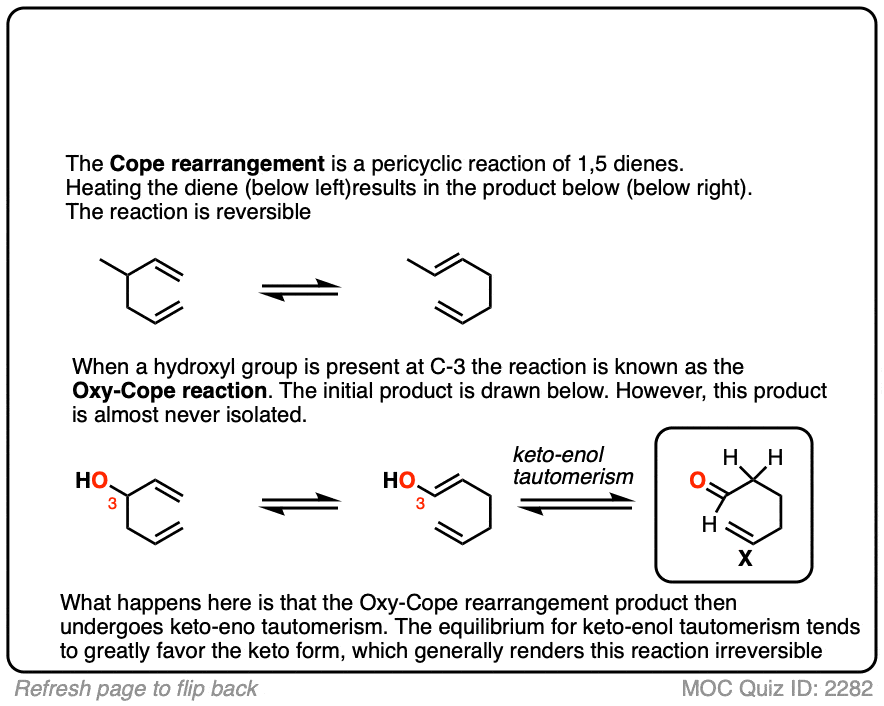
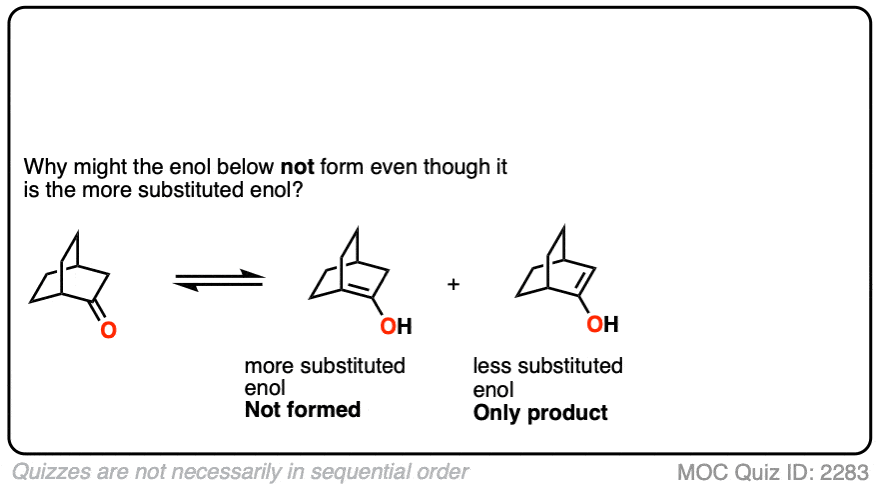 点击翻转
点击翻转
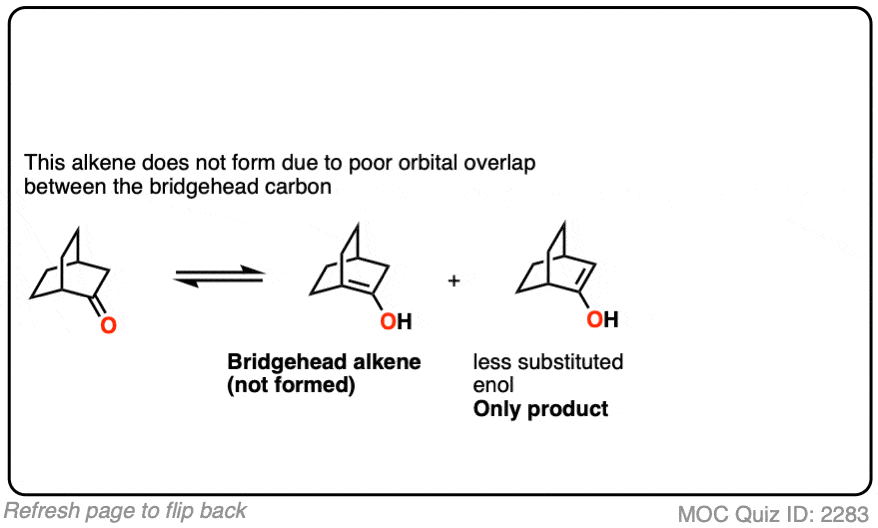
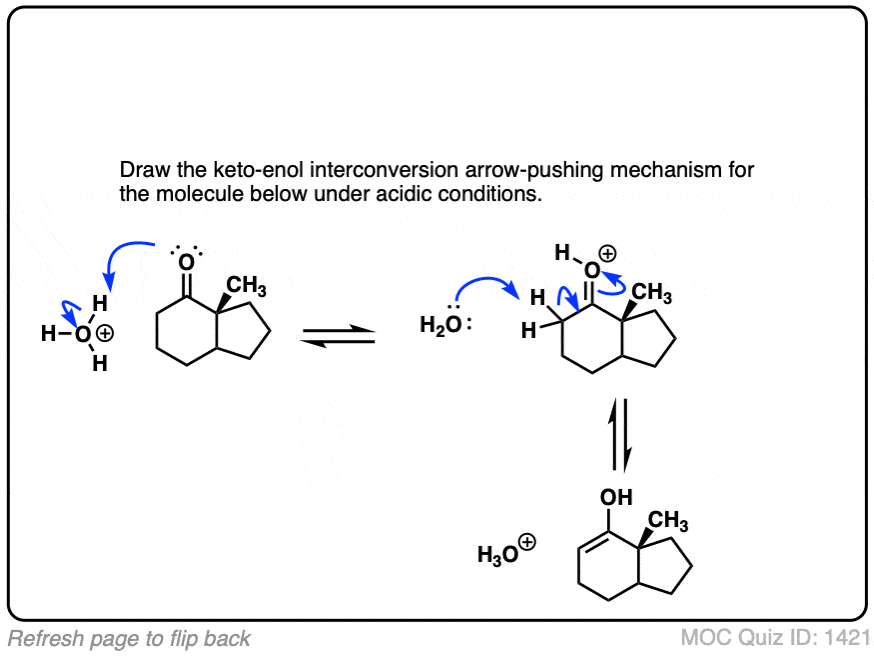
 点击翻转
点击翻转
(高级)参考资料和进一步阅读
从历史角度看互变异构,有机化学的结构与机理“,英戈尔德的书很有帮助。
例如,英戈尔德指出,“互变异构”一词是由拉尔(Berichte,1885, 648年而且Berichte,1886, 19,730),但提到拉尔不相信酮和烯醇形态是独立的物种。[https://chemistry-europe.onlinelibrary.wiley.com/doi/abs/10.1002/cber.188601901165]
后来,通过将乙酰丙酮乙酯分离为酮酮和烯酚组分,使其在-80°C下结晶为酮酮形式,并表明它可以转化为酮酮形式(Berichte1911,44, 1138年).纯的蒸馏(更容易挥发)烯醇表格稍后报告(Berichte,1921, 54,579).
1.酸催化酮烯化反应机理研究
Gustav E. Lienhard和dong - chia Wang
美国化学学会杂志196991 (5), 1146-1153
DOI:10.1021 / ja01033a019
对酮的研究烯醇环己酮的反应平衡支持酸催化反应存在速率限制步骤烯醇→酮互变异构是β -碳的质子化(基于与水解速率的相似烯醇醚)。酮→的速率决定步骤烯醇互变异构是碳的脱质子反应。
2.乙酰乙酸中的互变异构平衡
凯伦·d·格兰德和斯图尔特·m·罗森菲尔德
有机化学杂志198045 (9), 1626-1628
DOI:10.1021 / jo01297a017
摘要:“乙酰乙酸中的互变异构平衡已经用1氢核磁共振,发现是强烈的溶剂依赖。值烯醇D的互变异构体范围小于2%2O到49%的CCl4.化学位移数据表明烯醇互变异构体在极性较低的溶剂中是内部氢键的,而这种内部氢键对于酮互变异构体来说并不重要。”
3.碱金属烯醇在水溶液中生成简单烯醇。异丁醛的一些化学反应烯醇
Y.蒋,A. J.克雷斯基,P. A.沃尔什
美国化学学会杂志1986108 (20), 6314-6320
DOI:10.1021 / ja00280a032
给出了酮的平衡常数的估计值烯醇异丁醛的相互转化K= 1.37 × 104,并估计pK一个的烯醇形式为11.63和pK一个酮的含量是15.49。
4.酮的动力学和热力学烯醇简单的互变异构羰基化合物:一种基于低卤素浓度卤化动力学研究的方法
雅克·埃米尔·杜布瓦,莫希丁·埃尔-阿拉维和让·图勒克
美国化学学会杂志1981103 (18), 5393-5401
DOI:10.1021 / ja00408a020
包含各种酮在水溶液中烯化的速率和平衡常数(见表2,第5396页),特别是环烷酮和取代苯乙酮。
5.酮的溶剂作用烯醇平衡:定量模型的检验
桑德·g·米尔斯和彼得·比克
有机化学杂志198550 (8), 1216-1224
DOI:10.1021 / jo00208a014
关于几种不同酮的有趣研究烯醇互变异构体对。有趣的注释来自摘要:“一般来说,对于异构体对,其中烯醇不能形成内部氢键,这种平衡似乎完全由溶剂的氢键碱性所控制(重点是我的)。
6.丙二醛(3-羟基-2-丙二醛)的微波光谱研究。2.结构、偶极矩和隧穿
Steven L. Baughcum, Richard W. Duerst, Walter F. Rowe, Zuzana Smith和E. Bright Wilson
美国化学学会杂志1981103 (21), 6296-6303
DOI:10.1021 / ja00411a005
丙二醛是最简单的羰基醛.本研究利用微波光谱法测定了丙二醛内部氢键结构的键长烯醇互变异构体。
7.气相酸和生成2,4-和2,5-环己二烯-1-酮的热互变异构体苯酚的
Christopher S. Shiner, Paul E. Vorndam和Steven R. Kass
美国化学学会杂志1986108 (19), 5699-5701
DOI:10.1021 / ja00279a006
作者制造了二酮互变异构体(通过回溯Diels-Alder反应!)并研究了它们的酸度和生成热。苯酚[2H]-互变异构体的生成热比苯酚高约6千卡/mol,而[4H]-互变异构体的生成热比苯酚高约10千卡/mol。
请帮我准备iit jee。你的网站和努力是非常好的。我非常喜欢它。我想知道我应该多注意哪些反应。
打开凯莉和桑德伯格的A部分并学习它!!
谢谢- C&S A绝对是这个话题最好的资源。非常全面,有清晰的实验例子。
这不是一个典型的印度网站,只关注IIT-JEE或此类考试。
这个网站是关于o-chem的,你可以如何简单地解释o-chem中最困难的领域。如果你学好了这门学科,你可以解决任何问题,雷竞技下载最新版这就是印度理工学院寻找的人,而不是一个只是通过考试的人.......所以学习并享受o-chem吧
你好,
烯醇化合物能单独分离吗?
我的产品在酸性条件下以烯醇形式存在。键能偏向烯醇侧。但是当我把它变成中性时它又会变成酮。
我想分离产物,当它是烯醇的时候。
为此,我想试试你的想法。1)芳构化。[请让我知道该怎么做]
2)共轭加法。
我如何在我的院子里做这些过程。请让我知道....我非常欢迎来自外部....的回复
“harish@synthite.com”
如果你把酮化合物和碱反应,比如说氢化物,你会得到烯醇和氢气,氢气会从溶液中冒出来,根据勒夏特列耶原理,它会继续完成,你会得到完全的烯醇.....我相信…我不确定.....还没有在实验室试过....但你应该考虑一下,它可能会给你想要的产品:-)
脱质子反应会得到烯酸酯,而不是烯醇。他对中性烯醇产物感兴趣。一旦质子化,两种形式之间就会再次达到平衡。
首先,谢谢你。你的文章写得很好,消除了我的许多疑虑。请帮我回答这个问题:1,3环己二酮容易发生碱或酸催化的氘交换,而二环[2,2,2]辛烷-2,6-二酮则不会。
这是因为桥头堡碳的杂化变化受到限制,后期α氢的数量较少吗?
是的,我认为桥头堡碳有一些限制。我记不太清楚了,但我猜对于小的双环化合物来说不可能有一个带电的桥头堡碳
是的,这是因为布里德特法则,它说任何环小于6的双环化合物,在桥头位置不能有电荷或π键
酮烯醇形成的基本条件是什么? ?
酮或醛至少有一个碳上有一个碳氢键!
酮类的高键能比烯醇类的低键能更稳定?这似乎有违直觉。这是真的吗?
更高的键能意味着“更强的键”,因此“更难断裂”。明白吗?
再加上,是否可以这样说酮的键能比烯醇的键能高,但总能量(酮的G)更低,使得它在热力学上更稳定?
澄清一下,烯醇化和酮烯醇互变异构具有相同的机制,对吧?谢谢你!
请告诉我哪种是1,3环己二酮最稳定的形式,为什么
为什么当路易斯基在烯醇附近时,烯醇形式通过内部氢键稳定.....??如果是路易斯酸而不是路易斯碱呢?
我有一个问题为什么开式酮测试仪的烯醇含量几乎为零为什么烯醇含量会急剧增加当你把酯换成苯基时?两种情况下不是都有双键共轭吗那么烯醇含量是多少呢。酮酯中较少
我能检查一下酮醇和烯醇的比例是正确的吗?在第一种情况下,在第2点下,酮:烯醇的比例是24:76。在第二种情况下(相同的二酮和相同的溶剂,见情况3),酮:烯醇的比例为81:19。如果第一个比例是正确的,那么苯作为溶剂的比例(情况3)也会是错误的。
任何帮助在这方面将非常感激。
你好,你有一个很棒的网站!
我只是想知道;烯醇互变异构时,它是和取代最多还是最少的相邻碳形成双键?
非常感谢
酮烯醇互变异构中温度是如何控制烯醇含量的
你能澄清我的疑问吗?我想知道为什么在乙酰乙酸中右边的碳(附在甲氧基上的碳)没有发生互变异构,而只有另一个碳发生互变异构,这是一种影响吗?先谢谢你
一般来说,醛的烯醇含量最高,酮的烯醇含量降低,酯的烯醇含量基本检测不到。
我的理解是,在没有其他因素(如氢键、共振、芳香性)的情况下,烯醇形式的有利性与控制烯烃热力学稳定性的因素密切相关。基本上,碳碳π *键上有相邻取代基的超共轭供体。吸电子基团会降低π *轨道的能量,而给电子基团(如OR)会提高π *轨道的能量,使得这些稳定的相互作用不那么重要,降低了烯烃(烯醇)形式的稳定性。
解释得很好!!