有机试剂
试剂星期五:叔丁醇钾[KOC(CH3)3]
最后更新:2020年1月29日|
叔丁醇钾(KOt-Bu)是一个笨重的底座
在一个明显的插入试剂指南和试剂应用程序在美国,每周五我都会分析Org 1/ Org 2中常见的不同试剂。
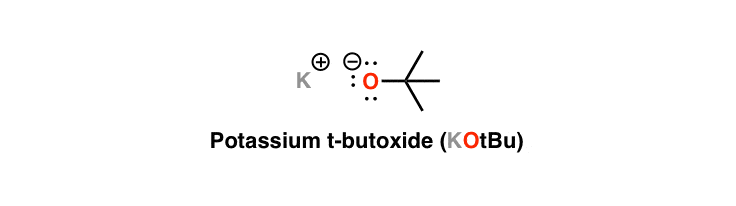
在普通化学课上,你(希望)学过氢氧根离子(HO-)是强碱。这是一个共轭碱也就是说,当我们从水里抽走一个质子(H+)后,水就剩下了。同样地,醇(ROH)也是强碱——一旦你去掉质子就会得到共轭碱(RO)。与氢氧根离子的强度相似,它们被称为醇盐.
钾叔醚(KOt-Bu)是一个笨重的底座
今天的试剂,叔丁醇酸钾(kt -bu),是一种像所有醇酸一样的强碱,但它有一些特殊之处。如果你以前遇到过叔丁基,你应该能记住一件主要的事情:它真的很讨厌脂肪(尽管在这个更加敏感的时代,“笨重”是首选的术语)。而作为共轭碱的t-丁醇t醚的庞大的基础就像我们的老朋友一样乔治。.(注意,“钾”在这里不是那么重要,我们可以省略它,或者用钠或锂代替它——我们真正关心的是“t-丁氧”部分。)
丁氧钾就像一个愤怒的相扑手。它以凶猛而坚定的决心攻击外面的东西。然而,任何需要通过一个狭窄的开口(如门口)进行导航的事情都是困难的。在化学意义上,这意味着叔-丁氧化物对空间相互作用非常敏感。(什么是“空间相互作用”?想想4个饥饿的相扑选手试图挤进你的小餐桌)。更具体地说,空间相互作用是电子云之间的排斥相互作用,当原子“碰撞”到彼此时发生。
钾叔由于空间位阻,-丁醇比其他醇氧化合物亲核性差
那么这对丁氧化t的化学反应意味着什么呢?两件事。
首先,叔-丁氧是较差的亲核试剂在亲核取代反应(如SN2)。为什么?因为年代N2对空间相互作用非常敏感,叔丁醇体积较大。
作为基地,叔-丁氧化物在消除反应中倾向于Hofmann产物的“非zaitsev”
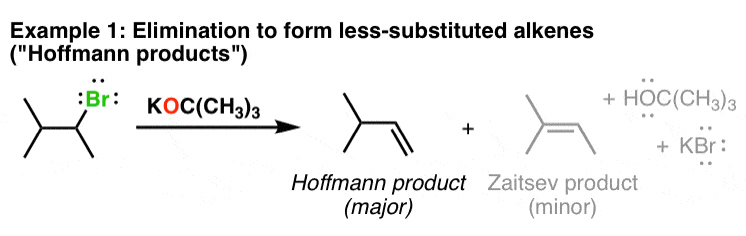
- 叔-丁氧可用于形成“较少取代”。烯烃在消去反应中E2,特别是)。大多数时候,消除反应倾向于"更多取代"烯烃——也就是扎伊采夫的产品。然而,当使用叔丁醇时,它会优先从较小的基团中去除质子。这就产生了所谓的“霍夫曼“产品.让我们看一看。
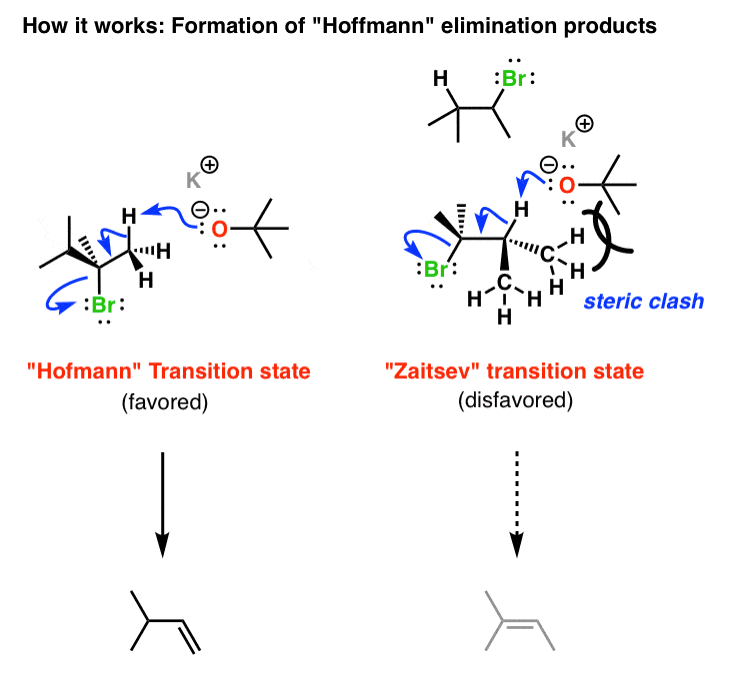
机理:利用烯烃形成叔-丁氧基
附注:你可以在“有机化学试剂指南”中阅读关于KOtBu和其他80多种本科有机化学试剂的化学知识,可以在这里下载PDF文件.试剂应用程序也可用于iPhone,点击下面的图标!
(高级)参考资料和进一步阅读
- Einwirkung der Wärme auf die氨basen
w·霍夫曼
化学。的误码率。1881年,14(1), 659 - 669
DOI:10.1002 / cber.188101401148
霍夫曼的原始论文是关于一种新方法烯烃合成。他是19世纪一位多产的有机化学家th世纪和他的名字已经连接到各种转化,包括酰胺降解,异腈合成,和其他一些。
- 烯烃从胺:霍夫曼消去反应而且胺氧化热解
阿瑟·柯普;埃尔默·R·特朗布尔
反应。1960,11, 317 - 493
DOI:10.1002/0471264180. or011.05
有机反应,由ACS有机化学部门出版和维护,是有机化学中各种转变的综合评论的来源。这篇特别的评论是由Cope教授(麻省理工学院的Cope重排)写的。最后给出了详细的实验步骤。 - 唑类化合物n-烷基化的hofmann型消去:咪唑和苯并咪唑
安德拉斯霍
合成1994;1994(1): 102 - 106
DOI:1055 / s - 1994 - 25414
将氰乙基取代的唑烷化,然后用强碱加热,经霍夫曼消除制得丙烯腈。 - Clarke-Eschweiler甲基化过程中的环化
Arthur C. Cope和W. Dickinson Burrows
有机化学杂志196530.(7), 2163 - 2165
DOI:1021 / jo01018a011
本文给出了两种含化合物的Hofmann消去法5而且7.
我很想知道,如果离去基和氢不是反平面的,那么分子能不能被旋转从而发生E2反应。
是的,只要它们不在一个不能旋转的环上(比如环烷烃)
t-丁醇,而不是t-丁醇,能参与E1反应吗?
是的,如果反应是加热的。
当你说“它会优先把质子从较小的基团上带走”时,你是指取代基最少的基团吗?扎伊采夫规则也指出“越穷越穷”(在氢中),这就是为什么它倾向于“更多取代烯烃”的原因吗?(更少的氢=更多的官能团=更多的取代基)?
是的,在KOtBu的情况下,氢应该从取代基最少的基团(例如CH3 vs. CH2CH3)中除去。
扎伊采夫偏爱“最取代烯烃”,因为这些烯烃在热力学上更稳定。原因需要一段时间来解释——它涉及到超共轭。这里我就不详细讲了。
即使叔丁基空间上很大,如果离去基是伯的,它能进行Sn2反应吗?如果是这样,这是否意味着叔丁醇实际上是强亲核试剂,只是如果底物是次级的,它就不是亲核试剂。
是的,它可以进行SN2反应如果离去基是主的。它的亲核试剂没有体积较小的醇酸那么好,但还是可以的
我们可以用叔丁醇来去除-OH基上的氢吗?
是的,当然。
在戊醇上的氢被除去后,会形成双键还是氧会带-1电荷?
氧带-1电荷。没有什么能让O- left形成双键了!
叔丁醇可以用来去除仲醇中的质子吗
是的,但你会在二醇盐和丁醇盐之间建立平衡。所以一定要多加点。
仲丁醇也应该考虑为大碱吗?
不是真的。
你说阳离子没有影响(Li, Na, K),如果钠比钾便宜这么多,为什么t-丁氧化钠在文献中没有被更多地提到?
*就我们的目的而言*阳离子没有影响。为了介绍有机的目的。对于*实际*工作,KOtBu具有较弱的O-K离子键,更容易解离,在有机溶剂中具有更好的溶解度,并且倾向于至少在小规模实验室工作中最受欢迎的选择。
我想用这种试剂进行二氯二酸的消除反应,生成卤代烯酰,我不确定用什么温度。加成过程是否在很低的温度下进行然后反应温度升高以促进消除?如果是,我应该增加到哪一点?rt是个好主意吗?
这是一个实验程序。
亨利·n·c·王,彼得·j·高拉特和弗朗茨·桑德海默
美国化学学会杂志1974 96 (17),5604-5605
DOI: 10.1021 / ja00824a066
溶解叔丁醇钾的溶剂除了水还有什么?
叔丁醇是制备丁氧化钾的最佳溶剂。所有其他醇都会形成醇/醇氧化合物的混合物。
我们可以用叔丁醇来去除环化合物中的硫吗?
机制保持不变吗?
你必须附上你要做的事情的照片。
如何从1-丁醇中得到丁氧化钾
在乙醚或四氢呋喃等溶剂中溶解,然后加入氢化钾。
网上最好的有机化学概念网站。非常感谢!
很高兴你发现它有用,Vivek!
丁氧化钾能用于1,2-二溴丙烷合成丙烯吗?比如双重消去,去掉溴原子形成丙基?
是的,有KOtBu形成乙炔的先例。我没有丙烷本身的参考资料,但你可以查看本文中的3.3节:2。芳香族乙炔的消除策略
Orita h;Otera,化学。Rev. 2006, 106, 5387
DOI: 10.1021 / cr050560m
本综述第3.3节介绍了由副二溴烷烃通过双脱氢溴化反应合成炔
我有一个问题。
我在THF溶液中看到与indanone, NaH, Diethylcarbonate的反应,它需要回流条件。
此外,我发现一些反应可以在室温下进行,加入催化量的kt - bu。
我很好奇KOt-Bu在这种反应中可能起什么作用。是什么让这个反应在室温下进行。
我正在找一些资料,但是不容易找到确切的原因。
谢谢
这里发生的事情是,第一个等量的KOTbu使丹酮氢脱质子,然后当酯形成时(通过与碳酸盐反应),EtO(-)被排出。这是下一个反应的碱。换句话说,他们选择了一种能自己生成碱的试剂。如果用氯甲酸乙酯,就不行,因为它会激发Cl(-)而Cl(-)不是强碱。
我想用Et-Br/ KOC(CH3)3在乙酰乙酸乙酯的α位置上选择性地烷基化(乙基化[单乙基化])。这有用吗?实际上我想避免二烷基化。它是合适的底座吗?
我不知道你说的" α位置"是什么意思但如果你想把CH3烷基化,你需要加两个等量的碱。1) KOtbu 2) n-BuLi。最后烷基化。
当使用丁醇时,哪个反应是E1或E2 ?
在强碱如丁醇的存在下,反应几乎肯定是E2。
亲爱的詹姆斯博士
你举了一个2-溴-3-甲基丁烷的例子。如果我们少用2 -溴-丁烷支化卤代烷基会发生什么?我问你是因为特拉维夫大学的一个学生读了你的开场白后和他的讲师发生了争论。讲师说,只有卤代烷也与2 -溴-丁烷发生早午餐反应时,才会产生Zeitsev产物
如果我用1-丙醇和t-丁醇再加CH3I会发生什么?
我想你的意思是1个等价物。丁醇在这里不是一个很好的碱。由于丙醇和t-丁醇的酸度非常接近,丙醇的共轭碱和丙醇脱质子生成的t-丁醇之间会有一个平衡。你可能会产生副产物t-丁基甲基醚,我猜这不是你想要的。
t-丁氧与1-氯-2-甲基丙烷的表达率是多少?它的速率= k[烷基卤化物][bulkybase]吗?
是的,这是正确的。
如果叔丁醇钾作用于3-溴戊烷上会产生什么?
2-戊烯会是扎伊采夫产物吗?
在这种情况下,只有一种可能的产品,没有“扎伊采夫”或“霍夫曼”产品。
所以反应进行需要离去基,对吧?
你当然需要!
3-溴环己烯用什么处理会得到什么产物
叔丁醇钾?
1, 3-hexadiene。
叔丁醇有没有可能更适合扎伊采夫的产品而不是霍夫曼的?