有机试剂
试剂星期五:二异丙基酰胺锂(LDA)
最后更新:2020年10月16日|
二异丙基酰胺锂(乔治。),一种坚固的立体阻碍碱
在一个明显的插入试剂指南,每周五我都会介绍Org 1/ Org 2中常见的不同试剂。上周刚刚发布了1.2版,进行了大量更正,并增加了新的页面索引。
如果NaNH2是一条食人鱼,那么今天的试剂——锂diisopropylamide(乔治。)就像双髻鲨。它的咬合力也很强,但那独特的长鼻可能会碍事。所以乔治。不能像NaNH一样伸进狭小的空间2可以。
与LDA形成较少阻碍(“动力学”)烯醇化
换句话说:乔治。是一个坚固、笨重的底座。最常见的用法乔治。是在形成的烯醇化物.在下面的例子中,注意到碳=O两边的碳都有碳氢键吗?乔治。会选择性地把质子从被取代的碳中移走
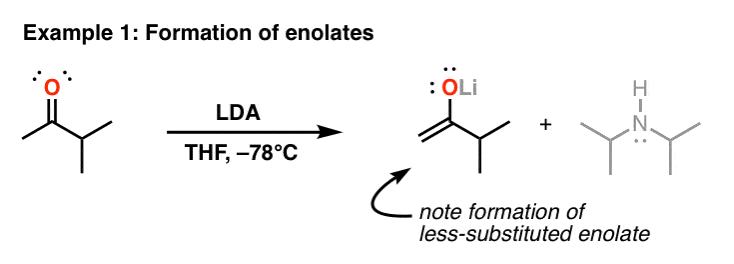
还要注意温度(-78°C)。- 78°相对于- 72°或- 60°并没有什么特别的作用——只是低温提高了选择性,而- 78°C恰好是一个非常便宜的冷水浴(干冰和- 60°)的温度丙酮).常见的溶剂是四氢呋喃(四氢呋喃).
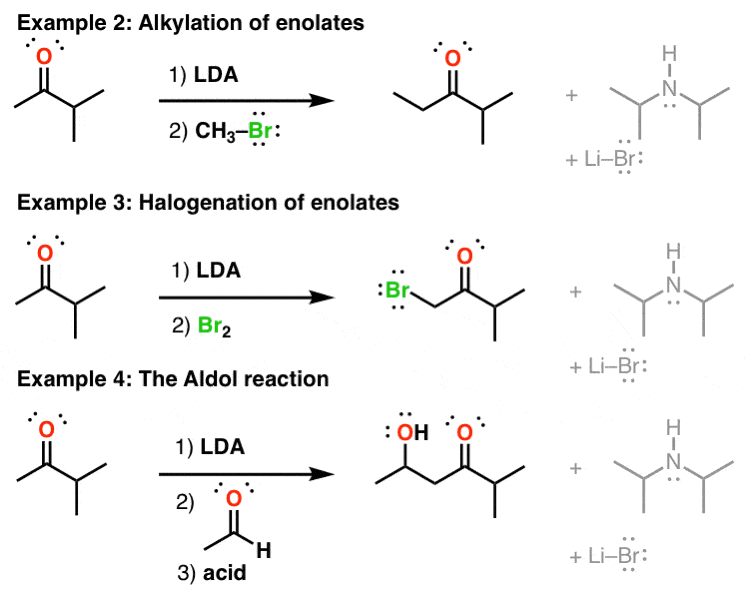
二异丙酰胺锂烯醇酯的烷基化、卤化和醛醇反应
为什么乔治。有用吗?烯醇酯非常有用ucleophiles,能够参与年代N2反应与烷基卤化物以及醛醇反应(在许多其他事情中)。如果我们用NaNH2形成一个烯醇化物像这样,我们可能会得到一个混合物两种烯醇酯的反应,会形成产物的混合物。的选择性乔治。在形成较少取代物时烯醇化物非常有用。
消除反应中少取代烯烃(“非扎伊采夫”或“霍夫曼”产物)的形成
虽然不太常见,乔治。也可以用来形成“霍夫曼消去反应中的产物。通常的底数是钾t-butoxide,但乔治。也可以做到:
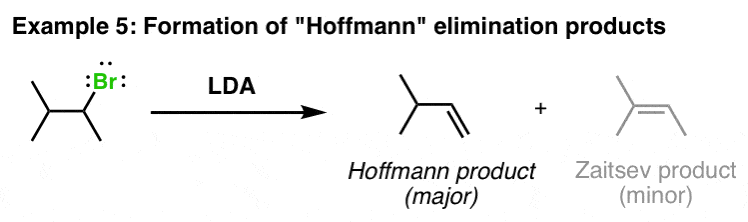
LDA生成少取代烯醇酯的机理
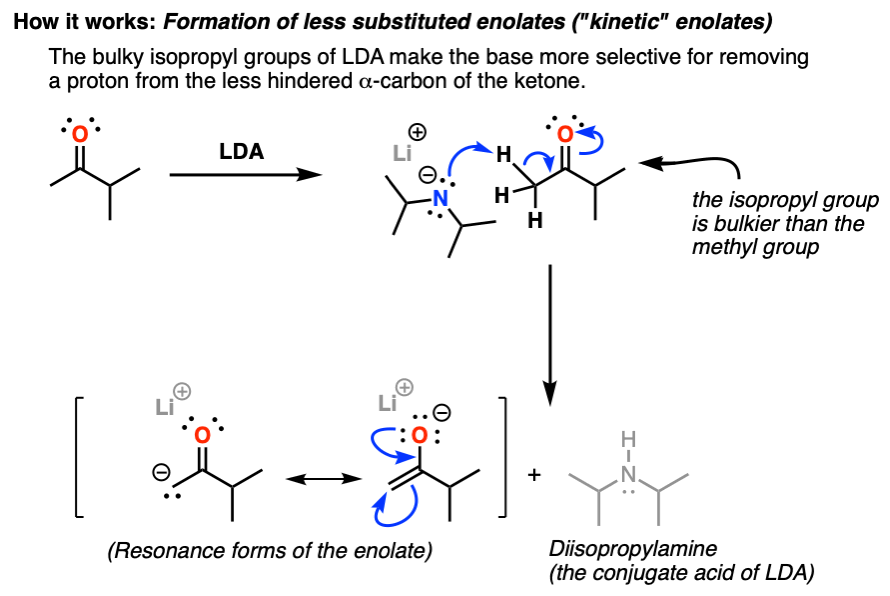
工作原理:
下面这张图显示了两者之间的反应乔治。和酮.注意正在形成的键(N-H, C-C)和正在断裂的键(C-H, C-O)。的烯醇化物形成了一个共振异构体其中负电荷在碳上。在某些方面,这是更“重要”的共振形式,因为碳往往是更好的共振形式亲核试剂烯醇酯反应中比氧多。
附注:你可以读到化学乔治。以及《有机化学试剂指南》中的80多种本科有机化学试剂,可以在这里下载PDF文件.
(高级)参考资料和进一步阅读
- α,β-不饱和酮的锂-氨还原反应中烯醇酯的α-烷基化
吉尔伯特·斯托克,佩里·罗森,诺曼·l·戈德曼
美国化学学会杂志1961年,83(13), 2965 - 2966
DOI:10.1021 / ja01474a051
这篇论文是对动力学最早的描述之一烯醇化物文献中的形成——”诱捕成功了烯醇化物离子IV取决于烷基化反应比最初产生的平衡反应快烯醇化物IV通过质子转移到更稳定的II与一些最初形成的中性烷基化酮.” - 第25号四面体报告:酮烯醇酯:地区特有的制剂和合成用途
吉恩·d天使
四面体1976,32(24), 2979 - 2990
DOI:10.1016 / 0040 - 4020 (76) 80156 - 1
这篇综述涵盖了各种方法烯醇化物形成,并有各种资料组成酮-烯醇化物在动力学和热力学条件下形成的混合物。H. O. House(麻省理工学院,然后是佐治亚理工学院)发表了一系列关于碳离子的论文烯醇化物化学,研究动力学和热力学烯醇化物形成的细节。以下是这些论文的精选: - 碳原子的化学。五、由不对称酮衍生的烯醇酯
赫伯特·欧·豪斯和维拉·克拉玛
有机化学杂志1963年,28(12), 3362 - 3379
DOI:10.1021 / jo01047a022 - 碳原子的化学。9由环酮衍生的烯醇酸钾和锂
赫伯特·欧·豪斯和巴里·m·特罗斯特
有机化学杂志196530.(5), 1341 - 1348
DOI:10.1021 / jo01016a001 - 碳原子的化学。十五。4-叔丁基环己酮烷基化立体化学研究
赫伯特·o·豪斯,本·a·特费勒,休·d·奥姆斯特德
有机化学杂志1968年,33(3), 935 - 942
DOI:10.1021 / jo01267a002 - 热力学和动力学控制烯醇化物:一个以问题为导向的实验课程计划
小奥古斯丁·西尔韦拉,迈克尔·a·诺普,和金钟
化学教育杂志1998年,75(1), 78
DOI:1021 / ed075p78
一篇来自j .化学。艾德。这涵盖了如何演示的概念动能而且热力学烯醇化在本科实验室会议。
阿申赫斯特博士,你说" LDA最常见的用途是烯醇酯的形成。在下面的例子中,注意到碳=O两边的碳都有碳氢键吗?LDA会选择性地从被最少数量的氢取代的碳中去除质子,但它表明π键与α碳相连,而β碳与更多的氢相连。所以LDA会从氢最多的碳上去除质子,即霍夫曼产物。
错误,修正了。谢谢你给我这个位置。
在共振形式中,原子不运动。你看到的锂离子在甲烷原子旁边然后靠近氧化物原子的图实际上是一个动态平衡。(自由烯酸盐的图片代表共振。)这是一个重要的区别,因为根据软硬酸碱理论,硬LI+更紧密地结合在硬O-上,使得甲烷更容易被攻击,而在KDA中,软K+优先结合在软甲烷上,使得氧化物更容易被攻击。
在例4中,醛醇反应,不会是Li+而不是LiBr吗?
反应物这边没有溴。
上面的鲨鱼的例子是令人震惊的。我一下子就了解了试剂。
很高兴听你这么说!
先生,解释得很好。但我有一个疑问。如果异丙基的末端碳连着像NO2这样的强-I基团会发生什么?那么氢离子会被LDA从异丙基的叔碳原子中抽离出来吗?
这个试剂没有什么意义。
为什么你给试剂命名为星期五试剂。?????
因为这是谈论反应物的一种有趣的方式,仅此而已。
LDA的碱性足以从叔醇中提取质子吗?我也见过使用壬胺,但由于不溶性,反应只能在壬胺和叔醇的界面上进行。
我还看到了一些最近的工作,其中三氟化铒被用作从醇生成醚的催化剂。有道理,但甲基化剂的选择由于溶解度问题变得更加有限。
哦,当然。叔醇的pKa约为18,二异丙胺的pKa约为36。
问题是为什么要用LDA?NaH很好,特别是在THF这样的飘渺的溶剂中,它可以与钠配合。
在什么条件下LDA亲核?我有一本书(合成科学,Houben-Weyl)说它发生在没有弱酸性质子供体的情况下。例如,它可以通过与锂的双键的1,2加成来还原烯烃膦酸酯。但是它没有进一步的细节,我不确定弱酸性质子供体与这个反应有什么特别的关系。你知道LDA作为亲核试剂的作用吗?谢谢!
基本上LDA有助于反马氏反应机制和霍夫曼消去?如果是这样的话,那么在例2中CH3不是应该在3度碳上吗(这是反马氏反应)
在LDA中没有CO - NH键,但是为什么在名称中称为酰胺?
它们都被称为“amide”。我知道这很让人困惑。
这可能是因为制备它的母体化合物是一种酰胺
NaNH2叫sodamide, LiNH2叫lithium amide
在LDA中,两个氢被异丙基取代,因此称为二异丙酰胺锂
神奇的解释,谢谢!还有一个问题,为什么LDA和LCHIA对醛都不起作用?
它们加到醛碳上而不是去质子化碳。
1)在-20℃等高温条件下制备LDA效果如何?
2) LDA在-20℃时是瞬时形成的吗?
在-20°C下,LDA的形成基本上是瞬时的。事实上,在零度以下的温度下制作LDA,然后将其冷却到-78,然后再使用它来形成烯酸盐,这并不罕见。
这可能有点离题。我的课本上提到烯醇酸锂不能参与共轭加成,只能直接参与羰基加成,因为锂与亲电试剂的羰基氧配合,反应通过循环椅状过渡态进行。你们对此有什么见解吗因为我有一堆与此相符的作业
不*
TL: DR:你的课本是相当正确的。“不能”是一个非常强烈的词,因为总是有例外,但总的来说,这是一个很好的经验法则。
更详细地说:这取决于羰基的性质。不饱和醛,例如,几乎总是会进行1,2次加成。对于不饱和酮,尤其是不饱和酯,有很大的回旋余地。[1,4加到酯中比12加到更有利,因为你是从酮烯酸盐变成(不太稳定的)酯烯酸盐。羰基周围的空间位阻和位置也很重要,溶剂的选择也很重要。因为你面对的可能是一本高级教材,我将使用更高级的术语“硬”和“软”。
烯酸锂是一种相对“硬”的亲核试剂,更可能在“硬”羰基亲电位点发生反应。锂离子配位有助于实现这一目标,促进聚合的溶剂(例如THF和Et2O等空灵溶剂)也是如此。
有可能通过使用具有更大、更不协调的反离子的碱(如钾而不是锂)和极性非质子“共溶剂”(如HMPA)来促进1,4的加成,这将打破聚集。这些反应倾向于通过开放的过渡态而不是你提到的齐默尔曼-特克斯勒六元过渡态。
*例外?当然。比如,如果你在一个分子中形成一个烯酸锂它也含有一个不饱和酮,1,4-加成会形成一个5或6元环。在这种情况下,比1,2加法快得多,因为环闭合速率。
另一个例子是位阻酮。
我在3月(第5版)第15章关于碳碳多键的加成,并没有提到在1,4加成中禁止烯酸锂,但很常见的是人们使用Mukaiyama-Michael反应或Sakurai反应(在硅基烯醇醚存在的情况下使用Lewis酸)来进行1,4加成,而不是烯酸锂,可能是你提到的原因。
谢谢你的好问题。
LDA如何与庚二腈或cn-ch2-ch2-ch2-ch2-ch2- ch2-ch2-cn反应
去质子化CN附近的碳
NaNH2在脱氢卤化过程中也会产生像LDA一样的Hoffmann产物吗?
不,因为NaNH2很小,我希望它能给出扎伊采夫产品。
你好,詹姆斯,
我爱你的网站!我基本上了解了LDA的工作原理,非常感谢。我确实有个情况问题需要更好地理解。我知道如果你把卤代烷加到羰基化合物上它会加到取代最少的碳上。但是,如果加一个二卤化烯烃,烷基化合物会附着在哪里呢?它仍然是被取代最少的吗(由于体积大)?总是卤化物末端吗?IE:如果是1,2二溴丁烯,它会附着在1号碳上吗因为它总是附着在末端?或者1号碳,因为它被取代最少?或者是2号碳,因为双键会被打乱? Or a mixture because both are likely to happen? Does it matter if the butene is cis or trans (since that makes the 2 carbon more or less accessible)? Thanks, just trying to understand better how this mechanism works.
烯醇酯与卤代烃的烷基化反应是SN2反应,SN2反应只发生在sp3杂化碳上。在你描述的反应中,只有1-碳是sp3杂化的,因此烯酸盐会在C-1上进行取代。C2处的C-Br键不受影响。抱歉这么久才给你回电话。
虽然没有酰胺基团,为什么LDA被命名为二异丙基酰胺锂?
令人困惑的是,术语“酰胺”既指脱质子化胺,也指具有氮取代基的羰基衍生物。
在室温下反应的机理会发生变化吗?
不,但是选择性会发生变化。在较高的温度下,它对取代较少的烯酸酯没有那么强的选择性。
你好,
你知道在什么情况下我们使用n-BuLi而不是LDA吗?
为什么LDA, NaNH2即使没有酰胺的功能也被称为酰胺。谢谢你!
因为化学家用“酰胺”这个词来描述两个完全不同的官能团:胺的共轭碱(如酰胺钠)和与羰基相邻的氮的羧酸衍生物。事情就是这样。
如果酮的两边都有相等的取代,LDA会怎样?有可能通过数碳来确定取代最少的碳吗(如果我们有甲基和乙基,而不是异丙基,例如在#2中)。在这种情况下,加成会发生在甲基的一侧吗?
甲基和乙基不确定,但甲基和初生烷基的比例是95:5,只要它保持在-78并且烯酸不能达到平衡。
如何分解LDA?
为什么要分解它?只需在冰浴中冷却,(慢慢地)加入饱和的NH4Cl作为温和的酸。
嗯,NaNH2和末端炔反应。内炔能与NaNH2反应吗?
三键附近CH3的pKa至少是40,所以没有明显的加热。
为什么它最后有酰胺,即使在LDA中没有酰胺连接?
令人困惑的是,你所说的酰胺键的名称和胺的共轭碱的名称都是“酰胺”。一些化学家对这两个词的发音不同,但这并不能真正翻译成书面单词。在提到共轭碱时使用术语“金属酰胺”是有帮助的-这将它与(中性)官能团区分开来。