首页/有机化学学习提示:如何使用“学习伙伴”
有机化学学习小贴士
有机化学学习提示:如何使用“学习伙伴”
最后更新:2022年9月12日|
我不能把这个想法归功于自己,但不幸的是,我也不记得是在哪里读到的。
这里有一个有用的和快速的方法来利用学习伙伴。
假设你已经学会了一长串的反应,但是你需要练习你的合成技能。你可以这样做。
你和你的搭档都可以写出一个你知道的貌似合理的反应序列。它可以是两到三步——如果你喜欢,甚至更长(或更短)。包括试剂。保持相对简单。不要担心会让事情变得困难。坚持你所知道的。如果你对任何事情都不确定,那就不要去做。
我只是在想一些简单的事情,比如:
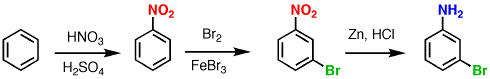
这是你的副本。现在把原料和成品抽出来,交给你的搭档。

当你看到所有的答案在你面前时,看起来很容易。现在看起来有点难了,不是吗?
通过这样做,你不仅可以练习在前进的方向上做出反应,你还可以学习如何向后思考。
这里有一个Org 1版本的例子。
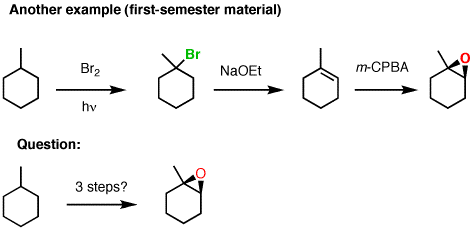
01键合、结构和共振
- 我们怎么知道甲烷是四面体?
- 杂化轨道和杂化
- 如何确定杂交:一条捷径
- 轨道杂化和化学键强度
- Sigma键有六种:Pi键有一种
- 关键技能:如何计算形式电荷
- 部分电荷提供了电子流动的线索
- 四种分子间力及其如何影响沸点
- 3种影响沸点的趋势
- 如何利用电负性来确定电子密度(以及为什么不相信形式电荷)
- 共振简介
- 如何使用曲线箭头交换共振形式
- 计算共振形式(1)-最小电荷规则
- 如何利用电负性找到最佳共振结构
- 评价带负电荷的共振结构
- 评价带正电荷的共振结构
- 探索共鸣:派捐赠
- 探索共振:pi受体
- 总结:评价共振结构
- 绘制共振结构:要避免的3个常见错误
- 如何应用电负性和共振来理解反应性
- 键杂化实践
- 结构和结合练习测验
- 共振结构实践
02酸碱反应
03烷烃和命名法
04构象和环烷烃
05有机反应入门
- 学习一种新反应时最重要的问题
- 组织中的4类主要反应
- 学习新的反应:电子如何移动?
- 电子如何(为什么)流动
- 学习一个新的反应时要问的第三个最重要的问题
- 有机化学中稳定负电荷的7个因素
- 有机化学中稳定正电荷的7个因素
- 常见错误:形式上的指控会产生误导
- 亲核试剂和亲电试剂
- 曲线箭头(用于反应)
- 弯曲箭头(2):最初的反面和最后的正面
- 亲核性与碱性
- 三类亲核试剂
- 什么是好的亲核试剂?
- 什么是好的离去基?
- 3个稳定碳正离子的因素
- 碳正离子不稳定的三个因素
- 什么是过渡态?
- 哈蒙德的假设
- 格罗斯曼的统治
- 先画丑的版本
- 学习有机化学反应:核对表(PDF)
- 加成反应简介
- 消除反应简介
- 自由基取代反应导论
- 氧化裂解反应导论
06自由基反应
07立体化学和手性
08置换反应
09消除反应
11SN1 SN2 / E1、E2的决定
12烯烃的反应
- 烯烃的E、Z表示法(+ Cis/Trans)
- 烯烃的稳定性
- 加成反应:消去的反义词
- 选择性vs.特异性
- 烯烃加成反应的区域选择性
- 烯烃加成反应的立体选择性:Syn与Anti加成
- 烯烃中盐酸的马氏加成法
- 烯烃加氢卤化机理及其对马氏规则的解释
- 箭推和烯烃加成反应
- 添加模式#1:“碳正离子途径”
- 烯烃加成反应中的重排
- 烯烃的溴化
- 烯烃的溴化反应机理
- 烯加成模式#2:“三元环”途径
- 硼氢化反应——烯烃的氧化
- 烯烃的硼氢化氧化机理
- 烯烃添加模式#3:“协同”途径
- 溴离子的形成:一个(次要)推箭困境
- 第四种烯烃加成模式-自由基加成
- 烯烃反应:臭氧分解
- 概述:烯烃反应机理的三个关键家族
- 钯对碳(Pd/C)催化加氢
- OsO4(四氧化锇)用于烯烃的二羟基化
- 间氯过氧苯甲酸
- 合成(4)-烯烃反应图,包括卤代烷基反应
- 烯烃反应练习题
13炔的反应
14醇,环氧化合物和醚
- 醇。命名法和性质
- 酒精可以充当酸或碱(以及为什么它很重要)
- 醇类-酸性和碱性
- 威廉姆森醚合成
- 威廉姆森醚合成:规划
- 烯烃、叔烷基卤化物和烷氧汞的醚
- 醇通过酸催化合成醚
- 醚与酸的裂解
- 环氧化物-醚家族中的异类
- 用酸打开环氧化物
- 环氧环开口与基地
- 从醇中制取烷基卤化物
- Tosylates和Mesylates
- PBr3和SOCl2
- 醇的消除反应
- POCl3消除醇生成烯烃的研究
- 酒精氧化:“强”和“弱”氧化剂
- 揭开酒精氧化机制的神秘面纱
- 醇和醚的分子内反应
- 酒精保护团体
- 硫醇和硫醚
- 计算碳的氧化态
- 有机化学中的氧化与还原“,
- 氧化梯子
- 醇制卤代烃的SOCl2机理:SN2 vs SNi
- 酒精反应路线图(PDF)
- 酒精反应练习题
- 环氧反应测验
- 氧化还原练习测验
15有机金属化合物
16光谱学
17Dienes和MO理论
- 有机化学中会发生什么
- 这些分子是共轭的吗?
- 有机化学中的共轭与共振
- 成键和反键轨道
- 烯丙基阳离子、烯丙基自由基和烯丙基阴离子的分子轨道
- 丁二烯的分子轨道
- 二烯反应:1,2和1,4加成
- 热力学和动力学产物
- 更多在1,2和1,4添加到双烯
- 顺式和反式
- Diels-Alder反应
- Diels-Alder反应中的环二烯和亲二烯
- Diels-Alder反应的立体化学
- Exo vs Endo产品在Diels Alder:如何区分他们
- Diels Alder反应中的HOMO和LUMO
- 为什么Endo vs Exo产品在Diels-Alder反应中更受青睐?
- Diels-Alder反应:动力学和热力学控制
- 复古Diels-Alder反应
- 分子内Diels Alder反应
- Diels-Alder反应中的区域化学
- Cope和Claisen重排
- Electrocyclic反应
- 电循环环开启和关闭(2)-六(或八)π电子
- Diels Alder练习题
- 分子轨道理论实践
19芳香分子的反应
- 亲电芳香族取代:简介
- 亲电芳香族取代反应中的激活和失活基团
- 亲电芳香族取代反应机理
- 亲电芳香族取代中的邻位、对位和元位董事
- 理解Ortho, Para和Meta director
- 为什么卤素是正对位的?
- 双取代苯:最强电子供体“胜出”
- 亲电芳香族取代(1)-苯的卤化
- 亲电芳香族取代(2)-硝化和磺化
- EAS反应(3)- Friedel-Crafts酰基化和Friedel-Crafts烷基化
- 分子内Friedel-Crafts反应
- 亲核芳烃取代(NAS)
- 亲核芳香族取代(2)-苄基机制
- “苄基”碳的溴化与氧化反应
- Wolff-Kishner, Clemmensen和其他羰基还原
- 芳香族侧链上的更多反应:硝基还原和拜耳Villiger反应
- 芳香族合成(1)-“操作顺序”
- 苯衍生物的合成(2)-极性反转
- 芳族合成(3)-磺酰基阻滞基团
- 桦树减少
- 合成(7):苯及相关芳香族化合物的反应图谱
- 芳香族反应与合成实践“,
- 亲电芳香取代的实践问题
在第二个例子中,NaOMe不是比KOtBu更好的选择吗? KOtBu可以通过Hoffman机甲产生大量的亚甲基环己烷。
固定的。谢谢你给我这个位置。
你对KOtBu(大体积基)作为非扎伊采夫消去条件了解多少?我想我是我校园里唯一一个教这个的人,当其他人使用KOtBu作为常规的Zaitsev E2淘汰时,我感到震惊。我愿意接受非扎伊采夫消除不是KOtBu被接受的用法,但网上似乎没有一致性。
cf用于非zaitsev使用KOtBu:
http://www.chem.siu.edu/chem341/c341lectures/c341eliminations.pdf(pg3)
http://pages.towson.edu/jdiscord/WWW/331_problem_sets/Chapter10_11/Reactions_of_Alkyl_Halides.pdf(pg12)
http://chm233.asu.edu/notes/halides/halides.html(# 7)
http://www2.chemistry.msu.edu/faculty/reusch/virttxtjml/alhalrx3.htm(就在Bredt规则标题前)
实际同行评议文章:
http://dx.doi.org/10.1021/ja00499a021
好问题。纵观C&S第4版(第387页),有一个明显的“趋势”,即大基生产更多的非扎伊采夫产品,尽管它高度依赖于离去基。例如,对于2-碘丁烷在DMSO中的反应,乙氧基生成17%的1-丁烯,而-OtBu生成21%的1-丁烯(没有给出反离子)。另一方面,OTs衍生物是35%的1-丁烯(以乙醇为单位),61%的1-丁烯(以DMSO为单位)。
还有另一个例子- 2-碘4-甲基戊烷,KOtBu给出39%的终端烯烃,而KOPr给出25%。
我得把3月份的数据挖出来再看一看。
这很难说是一个主导趋势,但它是真实的。我把它归为“善意的谎言”,即我们告诉学生的用来掩盖真实数据混乱的谎言。
我查了3月。这说明不了什么。在这个问题上非常模糊。
如果你看一下,它是在Ch17(第5版)的双键取向部分的开头,在它概述了基本的消除机制(#4)之后:
“在进一步的实验中,大量不同种类的碱被证明在碱度和霍夫曼消去率之间服从线性自由能关系……”(尽管引用的论文没有测试醇酸碱……)http://dx.doi.org/10.1021/jo01337a018)
你在JACS(1979)上给全文的引用也是C&S引用的。我感兴趣的是,它第一次出现在入门教材中是什么时候——我看到KOtBu在全国各地的课程中被称为非扎伊瑟夫淘汰的“庞大基础”。
有人应该花几周的时间把这个(和SN1/SN2!)的一套很好的实验结果放在一起,用于教学目的....如果我们打算每年向成千上万的入门级学生提供这些数据,有硬数据集就太好了。
“有人应该花几周的时间把这个(和SN1/SN2!)的一套很好的实验结果放在一起,用于教学目的....如果我们打算每年向成千上万的入门级学生提供这些数据,有硬数据集就太好了。”
SciFinder吗?不会太难的。
数据在那里,但经常有奇怪的小块缺失,比如溶剂或反离子略有不同。这是一床拼布被子。我只是想看看我们在课程中讨论的所有实验都被应用的研究,并将结果制成表格。你抽的是我抽的烟吗,随意挥舞的家伙?
是啊,这篇论文写起来会很有趣。当然,谁会出版这样的作品呢?j .化学。我觉得艾迪是最合适的人选。
而且,为了正确地做这件事,你需要相当多的资源,比如500美元的化学品和高效液相色谱。嗯。
学术界不太可能会觉得它很有趣,这是可以理解的。但考虑到二年级学生每年花在理解SN2反应上的总时间至少要几百人年,J. Chem。有可能是艾德。如果我有自己的实验室,一些时间,还有几千美元,我想把它弄个水落石出。有一天,希望,在我亚历山大·舒尔金启发的晚年....
有趣的是,马奇是如何解释“典型”情况下(如NMe3或SMe3离开基团)的霍夫曼消除的:
“向正电荷离去基的变化导致机制向光谱的E1cB端转移,那里有更多的C-H键断裂,酸度更重要(CH3氢比RCH2氢更酸)。
...
因此,从CH3CH2CH2CHXCH3中获得的1-烯的百分比如下(X按大小顺序排列):Br-, 31%;我- 30%;TsO, 48%;SMe2, 87%;SO2Me, 89%;NMe3, 98%。(KOEt为基,http://dx.doi.org/10.1021/ja01591a049)
大体积的碱基产生Hofmann(非zaitsev)产物是有道理的——拥挤产生类似sm的TS,所以更有E1cb机制。我们通过比较霍夫曼和扎伊采夫来教授这一点,离去基是决定机制的关键因素。赛克斯(http://www.amazon.co.uk/Guidebook-Mechanism-Organic-Chemistry-Peter/dp/0582446953)有点过时,但处理得很好。
伊恩·古尔德在亚利桑那州立大学的网站链接不起作用。还有其他的联系吗?
谢谢,删掉了。